Кислород
Газ без цвета, без запаха, составляет 21% воздуха.
Общая характеристика элементов VIa группы
От O к Po (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.
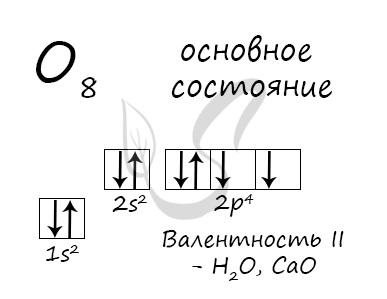
Основное состояние атома кислорода
У атома кислорода (как и атомы азота, фтора, неона) нет возбужденного состояния, так как отсутствует свободная орбиталь с более высоким энергетическим уровнем, куда могли бы перемещаться валентные электроны.
Атом кислорода имеется два неспаренных электрона, максимальная валентность II.
Природные соединения
Получение
В промышленности кислород получают из сжиженного воздуха. Также активно применяются кислородные установки, мембрана которых устроена как фильтр, отсеивающие кислород (мембранная технология).
В лаборатории кислород получают разложением перманганата калия (марганцовки) или бертолетовой соли при нагревании. Применяется реакция каталитического разложения пероксида водорода.
На подводных лодках для получения кислорода применяют следующую реакцию:
Химические свойства
Является самым активным неметаллом после фтора, образует бинарные соединения со всеми элементами кроме гелия, неона, аргона. Чаще всего реакции с кислородом экзотермичны (горение), ускоряются при повышении температуры.
Во всех реакциях, кроме взаимодействия со фтором, кислород проявляет себя в качестве окислителя.
F + O2 → OF2 (фторид кислорода, O +2 )
В реакциях кислорода с металлами образуются оксиды, пероксиды и супероксиды. Реакции с активными металлами идут без нагревания.
Известна реакция горения воды во фторе.
Все органические вещества сгорают с образованием углекислого газа и воды.
Процесс можно остановить на любой стадии в зависимости от желаемого результата.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Кислород: химия кислорода
Кислород
Положение в периодической системе химических элементов
Кислород расположен в главной подгруппе VI группы (или в 16 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение кислорода
Электронная конфигурация кислорода в основном состоянии :
+8O 1s 2 2s 2 2p 4 1s 

Атом кислорода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 2 неподеленные электронные пары в основном энергетическом состоянии.
Физические свойства и нахождение в природе
Озон О3 — при нормальных условиях газ голубого цвета со специфическим запахом, молекула которого состоит из трёх атомов кислорода.
Кислород — это самый распространённый в земной коре элемент. Кислород входит в состав многих минералов — силикатов, карбонатов и др. Массовая доля элемента кислорода в земной коре — около 47 %. Массовая доля элемента кислорода в морской и пресной воде составляет 85,82 %.
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе.
Способы получения кислорода
В промышленности кислород получают перегонкой жидкого воздуха.
Лабораторные способы получения кислорода:
Разложение перманганата калия:
Разложение бертолетовой соли в присутствии катализатора MnO2 :
2KClO3 → 2KCl + 3O2
Разложение пероксида водорода:
2HgO → 2Hg + O2
Соединения кислорода
| Степень окисления | Типичные соединения |
| +2 | Фторид кислорода OF2 |
| +1 | Пероксофторид кислорода O2F2 |
| -1 | Пероксид водорода H2O2 Пероксид натрия Na2O2 и др. |
| -2 | Вода H2O Оксиды металлов и неметаллов Na2O, SO2 и др. Соли кислородсодержащих кислот Кислородсодержащие органические вещества Основания и амфотерные гидроксиды |
Химические свойства
При нормальных условиях чистый кислород — очень активное вещество, сильный окислитель. В составе воздуха окислительные свойства кислорода не столь явно выражены.
1.1. Кислород реагирует с фтором с образованием фторидов кислорода:
С хлором и бромом кислород практически не реагирует, взаимодействует только в специфических очень жестких условиях.
1.2. Кислород реагирует с серой и кремнием с образованием оксидов:
1.3. Фосфор горит в кислороде с образованием оксидов:
При недостатке кислорода возможно образование оксида фосфора (III):
Но чаще фосфор сгорает до оксида фосфора (V):
1.4. С азотом кислород реагирует при действии электрического разряда, либо при очень высокой температуре (2000 о С), образуя оксид азота (II):
N2 + O2→ 2NO
1.5. В реакциях с щелочноземельными металлами, литием и алюминием кислород также проявляет свойства окислителя. При этом образуются оксиды:
2Ca + O2 → 2CaO
Однако при горении натрия в кислороде преимущественно образуется пероксид натрия:
2Na + O2→ Na2O2
А вот калий, рубидий и цезий при сгорании образуют смесь продуктов, преимущественно надпероксид:
K + O2→ KO2
Переходные металлы окисляются кислород обычно до устойчивых степеней окисления.
Цинк окисляется до оксида цинка (II):
2Zn + O2→ 2ZnO
2Fe + O2→ 2FeO
4Fe + 3O2→ 2Fe2O3
3Fe + 2O2→ Fe3O4
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
Алмаз горит при высоких температурах:
Горение алмаза в жидком кислороде:
Графит также горит:
Графит также горит, например, в жидком кислороде:
Графитовые стержни под напряжением:
2. Кислород взаимодействует со сложными веществами:
4FeS + 7O2→ 2Fe2O3 + 4SO2
Ca3P2 + 4O2→ 3CaO + P2O5
2.2. Кислород окисляет бинарные соединения неметаллов:
2H2S + 3O2→ 2H2O + 2SO2
Аммиак горит с образованием простого вещества, азота:
4NH3 + 3O2→ 2N2 + 6H2O
Аммиак окисляется на катализаторе (например, губчатое железо) до оксида азота (II):
4NH3 + 5O2→ 4NO + 6H2O
CS2 + 3O2→ CO2 + 2SO2
2CO + O2→ 2CO2
2.3. Кислород окисляет гидроксиды и соли металлов в промежуточных степенях окисления в водных растворах.
Кислород окисляет азотистую кислоту :
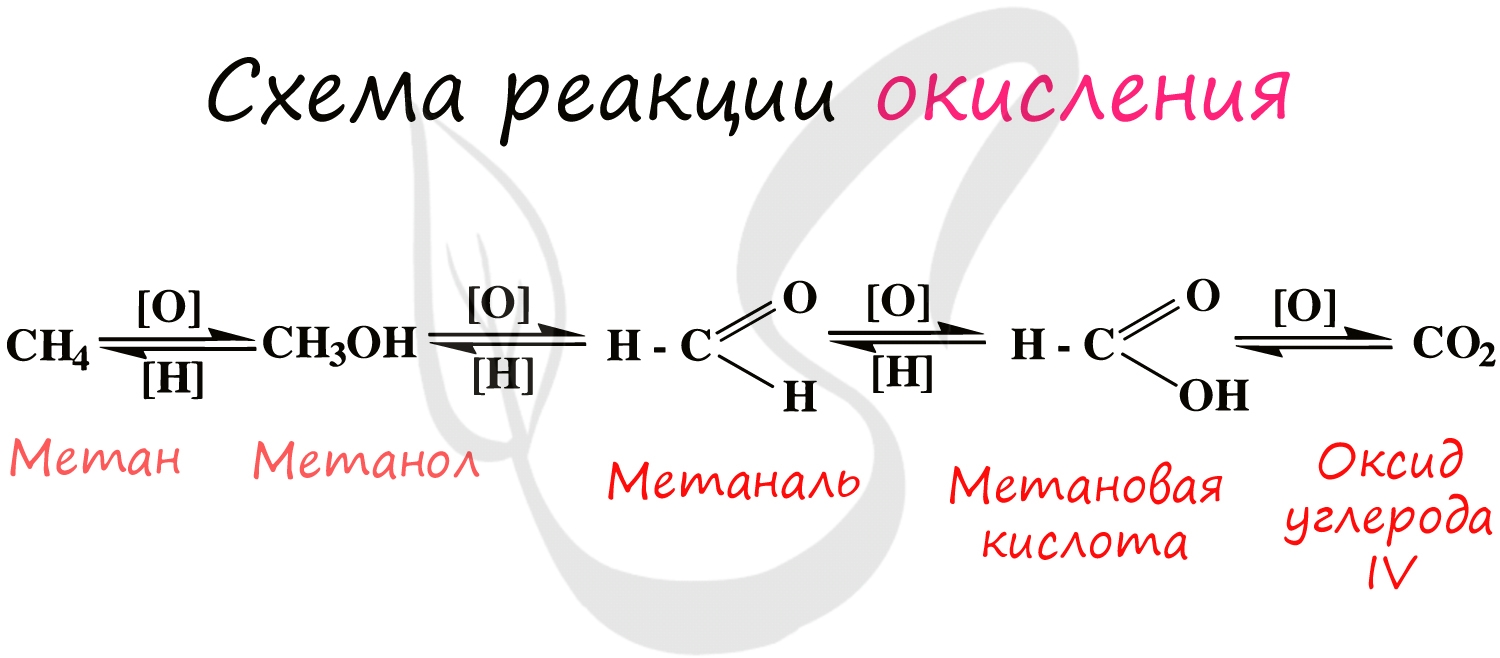
2.4. Кислород окисляет большинство органических веществ. При этом возможно жесткое окисление (горение) до углекислого газа, угарного газа или углерода:
CH4 + 2O2→ CO2 + 2H2O
2CH4 + 3O2→ 2CO + 4H2O
CH4 + O2→ C + 2H2O
Также возможно каталитическое окисление многих органических веществ (алкенов, спиртов, альдегидов и др.)
Кислород, свойства атома, химические и физические свойства
Кислород, свойства атома, химические и физические свойства.
15,99903-15,99977* 1s 2 2s 2 2p 4
Кислород — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 8. Расположен в 16-й группе (по старой классификации — главной подгруппе шестой группы), втором периоде периодической системы.
Атом и молекула кислорода. Формула кислорода. Строение кислорода:
Кислород – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением О и атомным номером 8. Расположен в 16-й группе (по старой классификации — главной подгруппе шестой группы), втором периоде периодической системы.
Кислород самый лёгкий элемент периодической таблицы химических элементов Д. И. Менделеева из группы халькогенов.
Кислород – химически активный неметалл.
Кислород обозначается символом О.
Как простое вещество кислород (химическая формула O2) при нормальных условиях представляет собой двухатомный газ без цвета, вкуса и запаха. В жидком состоянии кислород имеет светло-голубой цвет, а в твёрдом – представляет собой кристаллы светло-синего цвета.
Молекула кислорода двухатомна. Также встречается аллотропная модификация кислорода – озон, молекула которого состоит из трёх атомов кислорода.
Химическая формула кислорода O2 (или O3 – озон).
Строение атома кислорода. Атом кислорода (наиболее распространенный из трех изотопов кислорода (99,757 %) – 16 8О) состоит из положительно заряженного ядра (+8), вокруг которого по атомным оболочкам движутся восемь электронов. При этом 2 электрона находятся на внутреннем уровне, а 6 электронов – на внешнем. Поскольку кислород расположен во втором периоде, оболочки всего две. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внешняя оболочка представлена s- и р-орбиталями. Два спаренных электрона находится на 1s-орбитали, вторая пара электронов – на 2s-орбитали. На 2р-орбитали находится два спаренных и два неспаренных электрона. Поэтому во всех своих соединениях кислород проявляет валентность II. В свою очередь ядро атома кислорода состоит из восьми протонов и восьми нейтронов. Кислород относится к элементам p-семейства.
Радиус атома кислорода (вычисленный) составляет 48 пм.
Атомная масса атома кислорода составляет 15,99903-15,99977 а. е. м.
Кислород – самый распространённый химический элемент на Земле. В земной коре на его долю в составе различных соединений приходится около 46 % массы. Морские и пресные воды содержат по массе 86 % кислорода (если быть точнее – 85,82 %). В человеке его содержание составляет по массе 61 %. В атмосфере содержание свободного кислорода составляет 20,9476 % по объёму и 23,15 % по массе. На Солнце – 0,9 %, а во Вселенной – 1 %.
При высокой температуре молекула кислорода О2 обратимо диссоциирует на атомарный кислород. При 2000 °C на атомарный кислород диссоциирует 0,03 % молекулярного кислорода, при 2600 °C – 1 %, при +4000 °C – 59 %, при 6000 °C — 99,5 %.
Изотопы и модификации кислорода:
Свойства кислорода (таблица): температура, плотность, давление и пр.
| 100 | Общие сведения* | |
| 101 | Название | Кислород |
| 102 | Прежнее название | |
| 103 | Латинское название | Oxygenium |
| 104 | Английское название | Oxygen |
| 105 | Символ | О |
| 106 | Атомный номер (номер в таблице) | 8 |
| 107 | Тип | Неметалл |
| 108 | Группа | |
| 109 | Открыт | Карл Вильгельм Шееле, Швеция, 1771 г., Джозеф Пристли, Великобритания, 1 августа 1774 г. |
| 110 | Год открытия | 1771 г. |
| 111 | Внешний вид и пр. | Газ без цвета, запаха и вкуса |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | 4 аллотропные модификации, обусловленные различным составом молекул: – ε-кислород (O4 или O8) с простой моноклинной кристаллической решёткой, – ζ-кислород, металлическая фаза кислорода (On). 4 аллотропные модификации кислорода (O2), отличающихся строением кристаллической решётки: – α-кислород (α-O2) с простой моноклинной кристаллической решёткой, – β-кислород (β-O2) с ромбоэдрической (тригональной) кристаллической решёткой, – γ-кислород (γ-O2) с простой кубической кристаллической решёткой, – δ-кислород (δ-O2) |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 23,15 % |
| 119 | Содержание в земной коре (по массе) | 46 % |
| 120 | Содержание в морях и океанах (по массе) | 86 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 1 % |
| 122 | Содержание в Солнце (по массе) | 0,9 % |
| 123 | Содержание в метеоритах (по массе) | 40 % |
| 124 | Содержание в организме человека (по массе) | 61 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса)* | 15,99903-15,99977 а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s 2 2s 2 2p 4 |
| 203 | Электронная оболочка | K2 L6 M0 N0 O0 P0 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 48 пм |
| 205 | Эмпирический радиус атома | 60 пм |
| 206 | Ковалентный радиус* | 73 пм |
| 207 | Радиус иона (кристаллический) | O 2- 140,9755(3) кДж/моль (1,461108(4) эВ) –кислород 17 O, 140,9752(3) кДж/моль (1,461105(3) эВ) –кислород 18 O |
| 400 | Физические свойства | |
| 401 | Плотность* | 0,001429 г/см 3 (при 20 °C и иных стандартных условиях , состояние вещества – газ), 0,00142897 г/см 3 (при 0 °C и иных стандартных условиях , состояние вещества – газ), 0,027 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | α-кислород (α-O2) |
| 512 | Структура решётки | Простая моноклинная |
| 513 | Параметры решётки | a = 5,403 Å, b = 3,429 Å, c = 5,086 Å, β = 135,53° |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 155 К |
| 516 | Название пространственной группы симметрии | C12/m1 |
| 517 | Номер пространственной группы симметрии | 12 |
| 521 | Кристаллическая решётка #2 | β-кислород (β-O2) |
| 522 | Структура решётки | Ромбоэдрическая (тригональная) |
| 523 | Параметры решётки | a = 4,21 Å, α = 46,25° |
| 524 | Отношение c/a | |
| 525 | Температура Дебая | |
| 526 | Название пространственной группы симметрии | |
| 527 | Номер пространственной группы симметрии | |
| 531 | Кристаллическая решётка #3 | γ-кислород (γ-O2) |
| 532 | Структура решётки | Простая кубическая |
| 533 | Параметры решётки | a = 6,83 Å |
| 534 | Отношение c/a | |
| 535 | Температура Дебая | |
| 536 | Название пространственной группы симметрии | |
| 537 | Номер пространственной группы симметрии | |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7782-44-7 |
100* Данные в таблице приводятся применительно к кислороду (O2).
201* Указан диапазон значений атомной массы в связи с различной распространённостью изотопов данного элемента в природе.
206* Ковалентный радиус кислорода согласно [1] составляет 66±2 пм.
401* Плотность кислорода согласно [1] составляет 0,001429 г/см 3 (при 0 °C и иных стандартных условиях , состояние вещества – газ).
407* Удельная теплота плавления (энтальпия плавления ΔHпл) кислорода согласно [4] составляет 0,446 кДж/моль.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) кислорода согласно [3] и [4] составляет 3,4099 кДж/моль и 6,828 кДж/моль соответственно.
410* Молярная теплоемкость кислорода согласно [3] составляет 29,4 Дж/(K·моль).
Общие сведения
Кислород — это газообразный химический элемент. Он обозначается символом O, имеет атомный номер 8 и атомный вес 15,9994, а его молярная масса 32 г/моль. Формула кислорода О2. Схема электронной конфигурации атома кислорода — 1s 2 2s 2 2p 4. Строение атома кислорода имеет две оболочки, как и все элементы, расположенные во втором периоде.
В нормальных условиях О2 — бесцветный газ без запаха и вкуса. Он конденсируется в светло-голубой жидкости. Это реакционноспособный элемент, который образует оксиды со всеми другими элементами, кроме гелия, неона, аргона и криптона. Он умеренно растворим в воде (30 см3 на 1 л растворяющейся воды) при температуре 20 градусов Цельсия.
История открытия
Что такое воздух? Древние народы глубоко задумывались над этим вопросом. И это не удивительно, когда понимаешь, насколько важен воздух для многих процессов. Объекты не могут гореть без воздуха. Человек не может выжить без воздуха. На самом деле, древние народы думали, что воздух должен быть «элементом». Но они использовали слово «элемент» в несколько ином значении, нежели современные учёные. Для древних людей элемент был чем-то очень важным и основным. Воздух соответствует этому описанию, наряду с огнём, водой и землёй. Впоследствии многие учёные повлияли на открытие такого элемента, как кислород:
Некоторые люди думают, что Шееле следует отдать должное за открытие кислорода. Он завершил свои эксперименты раньше, чем Пристли. Но его издатель очень медленно печатал отчёты учёного. Они действительно вышли после отчётов Пристли. Таким образом, большинство историков сходится во мнении, что Шееле и Пристли должны разделить между собой право на открытие кислорода.
Ни Шееле, ни Пристли до конца не понимали важность их открытия. Этот шаг был предпринят французским химиком Антуаном-Лораном Лавуазье (1743−94). Лавуазье был первым человеком, который объявил, что новый газ является элементом. Он был также первым человеком, который объяснил, как кислород участвует в горении. Кроме того, он предложил название для газа.
Слово oxygenium («кислород») происходит от греческих слов, обозначающих «рождающий кислоту». Лавуазье выбрал такое название, потому что думал, что все кислоты содержат О2. Поэтому новый элемент отвечал за «образование кислот». Однако в этом отношении Лавуазье ошибся. Не все кислоты содержат кислород.
Элемент в окружающей среде
Земная кора состоит в основном из кремниево-кислородных минералов, и многие другие элементы присутствуют в виде их оксидов. Газообразный кислород составляет пятую часть атмосферы. О2 в атмосфере Земли образуется в результате фотосинтеза растений, он накапливался в течение длительного времени, поскольку они использовали обильные запасы углекислого газа в ранней атмосфере и выделяли кислород.
Элемент хорошо растворяется в воде, что делает возможной жизнь в реках, озёрах и океанах. Вода в этих водоёмах должна регулярно снабжаться кислородом, поскольку, когда запасы О2 в ней истощаются, она больше не может поддерживать рыбу и другие водные организмы.
Почти все химические вещества, кроме инертных газов, связываются с кислородом с образованием соединений. Вода, H2O и кремнезём, SiO2, основной компонент песка, являются одними из наиболее распространённых двойных кислородных соединений. Среди соединений, которые содержат более двух элементов, наиболее распространёнными являются силикаты, которые образуют большинство пород и почв. Другими соединениями, которые в изобилии встречаются в природе, являются карбонат кальция (известняк и мрамор), сульфат кальция (гипс), оксид алюминия (боксит) и различные оксиды железа, которые используются в качестве источника металла.
Элемент встречается во всех видах минералов. Некоторые общие примеры включают оксиды, карбонаты, нитраты, сульфаты и фосфаты. Оксиды — это химические соединения, которые содержат кислород и ещё один элемент. Карбонаты — это соединения, которые содержат кислород, углерод и ещё один элемент. В качестве примера можно привести карбонат натрия или соду, кальцинированную соду или солевую соду (Na2CO3), которая часто встречается в моющих и чистящих средствах.
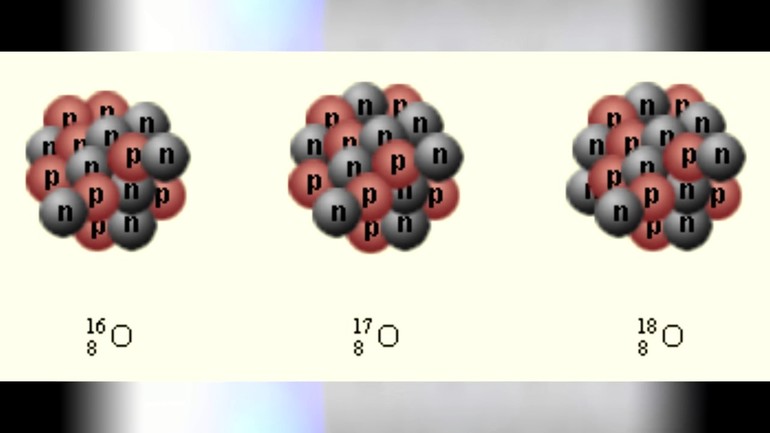
Изотопы кислорода
Есть три естественных изотопа О2: кислород-16, кислород-17 и кислород-18. Изотопы — это две или более формы элемента. Они отличаются друг от друга по их массовому числу. Число, написанное справа от названия элемента, является массовым числом. Оно представляет количество протонов плюс нейтронов в ядре атома элемента. Количество протонов определяет элемент, но количество нейтронов в атоме любого одного элемента может варьироваться. Каждая вариация является изотопом.
Известно также пять радиоактивных изотопов элемента. Радиоактивный изотоп — это тот, который распадается на части и испускает некоторую форму радиации. Радиоактивные изотопы образуются, когда очень маленькие частицы обжигают атомы. Эти частицы прилипают к атомам и делают их радиоактивными.
Воздействие на здоровье
Кислород необходим для всех форм жизни, так как он является составной частью ДНК и почти всех других биологически важных соединений. В лёгких этот элемент поглощается атомом железа в центре гемоглобина в крови и, таким образом, транспортируется туда, где он необходим.
Каждый человек нуждается в этом элементе, чтобы дышать, но, как и во многих случаях, слишком большое его количество вредно. Если человек подвергается воздействию большого количества О2 в течение длительного времени, может произойти повреждение лёгких. Вдыхание 50−100% кислорода при нормальном давлении в течение длительного периода приводит к повреждению лёгких. Люди, которые работают с частым или потенциально высоким воздействием чистого элемента, должны пройти тесты на функционирование лёгких до начала работы и по завершении.
Химические свойства
При стандартной температуре и давлении два атома элемента связываются, образуя диоксид кислорода, двухатомный газ без цвета, запаха и вкуса, с формулой O2. Этот элемент является членом группы халькогенов в периодической таблице Менделеева и является высокореактивным неметаллическим элементом. Он легко образует соединения (в частности, оксиды) почти со всеми другими элементами.
Кислород является сильным окислителем и обладает второй по величине электроотрицательностью среди всех реактивных элементов, уступая только фтору. По массе кислород является третьим по распространённости элементом во вселенной после водорода и гелия и наиболее распространённым по массе элементом в земной коре, составляя почти половину массы земной коры. Свободный кислород химически реактивен, чтобы появляться на Земле без фотосинтетического действия живых организмов, которые используют энергию солнечного света для производства элементарного кислорода из воды.
Элементарный O2 начал накапливаться в атмосфере только после эволюционного появления фотосинтезирующих организмов, примерно 2,5 миллиарда лет назад. Двухатомный газообразный кислород в настоящее время составляет 20,8% от объёма воздуха.
Наиболее важными химическими свойствами кислорода являются:
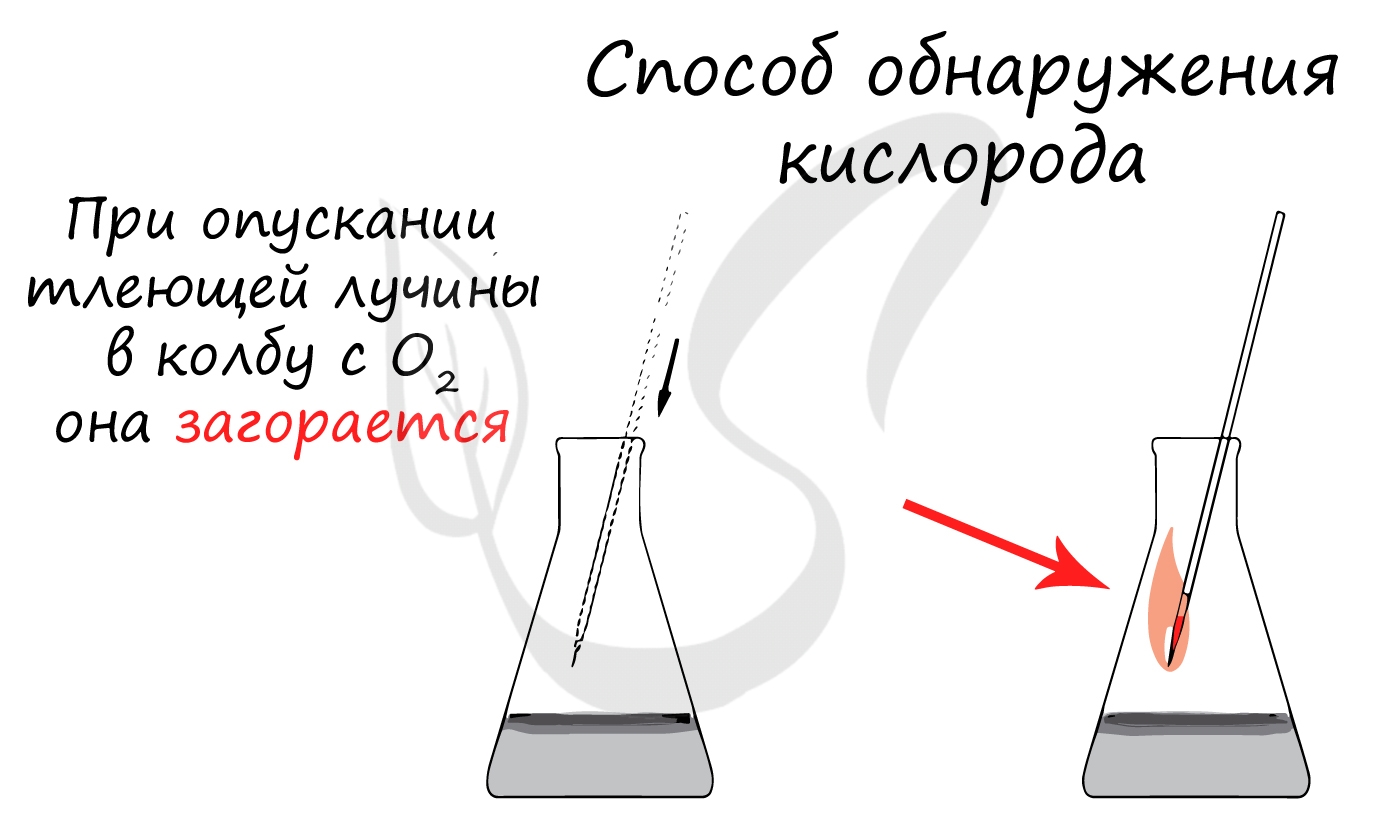
Сам О2 не горит. Зажжённая спичка в баллоне с чистым элементом горит гораздо ярче, но кислород не загорается.
Физические свойства
Кислород более растворим в воде, чем азот. Вода содержит приблизительно одну молекулу O2 на каждые две молекулы N2 по сравнению с атмосферным отношением приблизительно от одного до четырёх. Плотность кислорода в газообразном состоянии 1,42897 кг/м3. Другими физическими свойствами элемента являются:
Применение кислорода
Молекулярный диоксид O2 необходим для клеточного дыхания у всех аэробных организмов. Его реакционноспособные виды, такие как супероксид-ион (O2-) и пероксид водорода (H2O2), являются опасными побочными продуктами использования кислорода в организмах. Однако части иммунной системы высших организмов используют реактивный пероксид, супероксид и синглетный кислород для уничтожения вторгающихся микробов. Реактивные виды также играют важную роль в гиперчувствительной реакции растений на воздействие патогенных микроорганизмов.
В состоянии покоя взрослый человек вдыхает от 1,8 до 2,4 г кислорода в минуту. Это составляет более 6 миллиардов тонн элемента, вдыхаемого человечеством в год. Сферы использования включают в себя следующие:
Кислород и его соединения играют ключевую роль во многих важных процессах жизни и промышленности