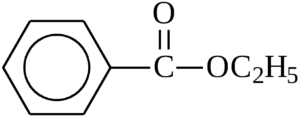
Молекулярная формула
Что такое молекулярная формула
Современные символы химических элементов были введены в науку в 1813 году Я. Берцелиусом. По его предложению элементы обозначаются начальными буквами их латинских названий. Например, кислород (Oxygenium) обозначается буквой О, сера (Sulfur) – буквой S, водород (Hydrogenium) – буквой Н. В тех случаях, когда названия элементов начинаются с одной и той же буквы, к первой букве добавляется еще одна из последующих. Так, углерод (Carboneum) имеет символ С, кальций (Calcium) – Ca, медь (Cuprum) – Cu.
Химические символы – не только сокращенные названия элементов: они выражают и определенные их количества (или массы), т.е. каждый символ обозначает или один атом элемента, или один моль его атомов, или массу элемента, равную (или пропорциональную) молярной массе этого элемента. Например, С означает или один атом углерода, или один моль атомов углерода, или 12 единиц массы (обычно 12 г) углерода.
Молекулярная формула веществ
Формулы веществ также указывают не только состав вещества, но и его количество и массу. Каждая формула изображает или одну молекулу вещества, или один моль вещества, или массу вещества, равную (или пропорциональную) его молярной массе. Например, H2O обозначает или одну молекулу воды, или один моль воды, или 18 единиц массы (обычно (18 г) воды.
Простые вещества также обозначаются формулами, показывающими, из скольких атомов состоит молекула простого вещества: например, формула водорода H2. Если атомный состав молекулы простого вещества точно не известен или вещество состоит из молекул, содержащих различное число атомов, а также, если оно имеет не молекулярное, а атомное или металлическое строение, простое вещество обозначают символом элемента. Например, простое вещество фосфор обозначают формулой P, поскольку в зависимости от условий фосфор может состоять из молекул с различным числом атомов или иметь полимерное строение.
Формулу вещества устанавливают на основании результатов анализа. Например, согласно данным анализа глюкоза содержит 40% (масс.) углерода, 6,72% (масс.) водорода и 53,28% (масс.) кислорода. Следовательно, массы углерода, водорода и кислорода относятся друг к другу как 40:6,72:53,28. Обозначим искомую формулу глюкозы CxHyOz, где x, y и z – числа атомов углерода, водорода и кислорода в молекуле. Массы атомов этих элементов соответственно равны 12,01; 1,01 и 16,00 а.е.м. Поэтому в составе молекулы глюкозы находится 12,01х а.е.м. углерода, 1,01у а.е.м. водорода и 16,00zа.е.м. кислорода. Отношение этих масс равно 12,01х: 1,01у: 16,00z. Но это отношение мы уже нашли, исходя из данных анализа глюкозы. Следовательно:
12,01х: 1,01у: 16,00z = 40:6,72:53,28.
Согласно свойствам пропорции:
x: у: z = 40/12,01:6,72/1,01:53,28/16,00
или х: у: z = 3,33 : 6,65 : 3,33 = 1 : 2 : 1.
Следовательно, в молекуле глюкозы на один атом углерода приходится два атома водорода и один атом кислорода. Этому условию удовлетворяют формулы CH2O, C2H4O2, C3H6O3 и т.д. Первая из этих формул — CH2O — называется простейшей или эмпирической формулой; ей отвечает молекулярная масса 30,02. Для того, чтобы узнать истинную или молекулярную формулу, необходимо знать молекулярную массу данного вещества. Глюкоза при нагревании разрушается, не переходя в газ. Но ее молекулярную массу можно определить и другими методами: она равна 180. Из сопоставления этой молекулярной массы с молекулярной массой, отвечающей простейшей формуле, ясно, что глюкозе отвечает формула C6H12O6.
Таким образом, химическая формула – это изображение состава вещества с помощью символов химических элементов, числовых индексов и некоторых других знаков, а молекулярную формулу вещества можно получить, зная простейшую формулу вещества и его молекулярную массу.
Примеры решения задач
| Задание | При сжигании 8,4 г углеводорода получили 26,4 г углекислого газа и 10,8 г воды. Относительная плотность паров углеводорода по воздуху равна 42. Найдите молекулярную формулу углеводорода. |
| Решение | Значение молярной массы углеводорода можно определить при помощи его плотности по водороду: |
По массам углекислого газа и воды находим массы углерода и водорода. Однако, для начала рассчитаем их молярные массы. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль;
M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль.
m (C) = 26,4×12/44 = 7,2 г.
m (H) = 10,8 × 2×1 / 18 = 1,2 г.
Обозначим количество моль элементов, входящих в состав соединения за «х» (углерод) и «у» (водород). Тогда, мольное отношение будет выглядеть следующим образом:
Следовательно, простейшая формула углеводорода имеет вид CH2и молярную массу 14 г/моль [M(CH2) = Ar(C) + 2×Ar(H) = 12+ 2×1 = 12 + 2 = 14 г/моль].
Чтобы найти истинную формулу оксида хлора найдем отношение полученных молярных масс:
Значит индексы атомов углерода и водорода должны быть в 6 раз выше, т.е. формула углеводорода будет иметь вид C6H12. Это гексен.
| Задание | При сгорании 2,3 г органического вещества, состоящего из углерода, водорода и кислорода, образовалось 4,4 г углекислого газа и 2,7 г воды. Плотность паров вещества по кислороду равна 1,44 г. Определите молекулярную формулу вещества. |
| Решение | Значение молярной массы углеводорода можно определить при помощи его плотности по кислороду: |
Msubstance = 32 × 1,44 = 46 г/моль.
По массам углекислого газа и воды находим массы углерода и водорода, а также кислорода (по разнице между массой вещества и атомов углерода и водорода в нем). Однако, для начала рассчитаем их молярные массы. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль;
M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль.
m (C) = 4,4×12/ 44 = 1,2 г.
m (H) = 2,7 × 2×1 / 18 = 0,3 г.
m(O) = msubstance — m (C) — m (H) = 2,3 – 1,2 – 0,3 = 0,8 г.
Обозначим количество моль элементов, входящих в состав соединения за «х» (углерод), «у» (водород) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом:
x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O);
x:y:z= 1,2/12 : 0,3/1: 0,8/16;
x:y:z= 0,1 : 0,3: 0,05 = 2 : 6 : 1.
Следовательно, простейшая формула органического соединения имеет вид C2H6O и молярную массу 46 г/моль [M(C2H6O) = 2×Ar(C) + 6×Ar(H) + Ar(O) = 2×12+ 6×1 + 16= 24 + 6 + 16 = 46 г/моль].
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула органического соединения будет иметь вид C2H6O.
Нахождение молекулярной формулы вещества (часть С)
Нахождение молекулярной формулы вещества
Нахождение химической формулы вещества по массовым долям элементов
Массовая доля элемента — это отношение его массы к общей массе вещества, в состав которого он входит:
Массовая доля элемента ($W$) выражается в долях единицы или в процентах.
2. Количества вещества железа и кислорода равны соответственно:
3. Находим соотношение количества веществ железа и кислорода:
4. Так как в формуле должно быть целое число атомов, то это отношение приводим к целым числам:
$Fe : O=1 : 1.33=2 : 2.66=3·3.99=3 : 4$.
5. Подставляем найденные числа и получаем формулу оксида:
Нахождение химической формулы вещества по массовым долям элементов, если указана плотность или относительная плотность данного вещества в газообразном состоянии
3. Отношение между атомами:
4. Определяем молекулярную массу углеводорода по относительной плотности ее паров.
5. Вычисляем относительную молекулярную массу углеводорода по простейшей формуле:
3. Отношение между атомами:
5. Молярная масса может быть представлена в виде:
6. Решаем систему двух уравнений с двумя неизвестными:
Нахождение химической формулы вещества по данным об исходном веществе и о продуктах его сгорания (по уравнению химической реакции)
1. Напишем схему уравнения горения углеводорода
$M=1.97$ г/л$·22.4$ л/моль$=44$ г/моль.
3. Определяем количество вещества:
4. Используя величину молярного объема, находим:
Окончательный вид уравнения:
Как найти молекулярную формулу
Молекулярная формула представляет собой способ выражения атомов и их количества, присутствующих в соединении. Молекулярная формула соединения представлена элементарными символами и их соотношениями.
Содержание:
Молекулярная формула представляет собой способ выражения атомов и их количества, присутствующих в соединении. Молекулярная формула соединения представлена элементарными символами и их соотношениями. Таким образом, очень важно знать, как найти молекулярную формулу соединения, чтобы узнать элементы, присутствующие в соединении, и их количества.
Ключевые слова: атомная масса, углерод, эмпирическая формула, водород, молярная масса, молекулярная формула, кислород
Ключевые области покрыты
1. Что такое молекулярная формула
— Определение и объяснение
2. Как найти молекулярную формулу
— Использование эмпирической формулы
3. Почему важно знать молекулярную формулу
— Применение Молекулярной формулы
Что такое молекулярная формула
Как найти молекулярную формулу
Прежде чем найти молекулярную формулу, следует выяснить эмпирическую формулу по массовым процентам каждого атома, присутствующего в соединении. Давайте рассмотрим следующий пример.
O подарок составляет 58 г
O = 1,208 (округлить до 1)
Эмпирическая формула CH2О.
Молярная масса СН2O = (1 x 12) + (2 x 1) + (1 x 16)
Поэтому число СН2Единицами O, присутствующими в соединении, являются
Следовательно, соединение должно быть (СН2О) х 2
Рисунок 01: предложение для C2ЧАС4О2 молекула
Почему важно знать молекулярную формулу?
Заключение
Способ нахождения молекулярной формулы соединения объясняется в этой статье. Чтобы найти молекулярную формулу, массовые проценты каждого атома в этом соединении должны быть известны.
Изображение предоставлено:
Как написать общую формулу для гомологического ряда, основываясь на формуле одного из его представителей?
В данной статье я вам покажу, как написать общую молекулярную формулу органических веществ любого класса, отталкиваясь от структурной формулы любого из его представителей.
Что вам нужно помнить железно, так это общую формулу алканов, она имеет вид CnH2n+2.
Далее, если вас просят, написать общую формулу, например предельных альдегидов:
1) вам следует записать формулу любого из них. Например:
2) Написать молекулярную формулу выбранного выше соединения, посчитав все атомы, входящие в состав его молекулы. В формуле выбранного в п.1. соединения мы обнаруживаем 3 атома углерода, 6 атомов водорода и 1 атом кислорода. Таким образом, оно имеет молекулярную формулу С3Н6O
3) Записать формулу алкана с таким же числом атомов углерода в молекуле. В нашем случае, с тремя атомами. Подставляя значение n=3 в формулу CnH2n+2 получаем С3Н8
4) Посмотреть, чем отличаются друг от друга молекулярные формулы полученного алкана и исходного вещества. В исходном веществе на два атома водорода меньше, и на один атом кислорода больше.
5) Внести изменения в общую формулу алканов, т.е. CnH2n+2 в соответствии с установленной разницей, т.е. уменьшить число атомов водорода на два и добавить один атом О в формулу. Т.е.
Для того чтобы были очевидны преимущества данного метода, давайте попробуем записать общую формулу гомологического ряда ароматических сложных эфиров. Ароматический значит в его структурной формуле есть бензольное кольцо, а сложные эфиры это вещества со сложноэфирной группой –С(O)-O-. Запишем формулу любого такого вещества, например:
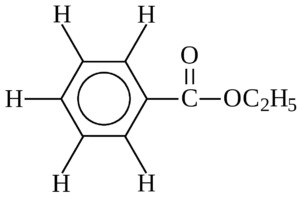
Для удобства ведения подсчетов атомов дорисуем не отображенные на структурной формуле выше атомы водорода, получим:
1) молекула выше состоит из 9 атомов С, 10 атомов Н, двух атомов O. Т.е. молекулярная формула данного вещества С9Н10O2
2) алкан с тем же числом атомов углерода имеет формулу C9H20. Сравнивая эту формулу с формулой изначального вещества С9Н10O2 мы видим, что в ней на 10 атомов H меньше и на два атома О больше, чем в соответствующем алкане.
3) Разница составов молекул исходного вещества и алкана с таким же числом атомов углерода будет той же самой и для общих формул гомологических рядов. Т.е.
Молекулярная формула: как получить, примеры и упражнения
Содержание:
В молекулярная формула Это представление молекулы соединения, в котором атомы всех элементов, присутствующих в соединении, и их количество обозначены их химическими символами. Каждый атом сопровождается нижним индексом.
Молекулярная формула имеет ограничение, которое не указывает ни на связи различных атомов молекулы, ни на их пространственное соотношение; как это делает структурная формула. В некоторых случаях он не конкретен, например: C6ЧАС12ИЛИ6 это молекулярная формула глюкозы, галактозы и фруктозы.
Молекулярная формула органических соединений записывается путем размещения сначала символа углерода (C), затем символа водорода (H), а затем оставшихся атомов. Например, молекулярная формула уксусной кислоты C2ЧАС4ИЛИ2.
Как получить молекулярную формулу
Получение молекулярной формулы соединения основано на предварительном установлении его минимальной или эмпирической формулы. По этой причине начальные этапы получения обеих формул являются общими.
Первый шаг
Обычно массу элементов химического соединения выражают в процентах. Затем необходимо выполнить простой расчет, чтобы преобразовать массовые проценты различных элементов в их массы, выраженные в граммах.
Второй шаг
Зная массу в граммах каждого из элементов и их атомную массу, относительное число каждого атома или число молей каждого атома можно получить, разделив массу каждого из различных элементов на их атомную массу.
Третий шаг
Разделите относительное количество все атомов, введите относительное количество меньшего значения. Значения минимальной доли должны быть целыми числами. В случае, если значение пропорции содержит десятичную дробь, необходимо внести поправку, чтобы эта десятичная дробь исчезла.
Коррекция заключается в умножении всех значений пропорции на число, которое возвращает все значения в целые числа. Например, если значение минимальной пропорции составляет 1,25, все значения необходимо умножить на четыре (4). Поскольку 1,25, умноженное на 4, равняется 5, целому числу.
Четвертый шаг
Все химические символы элементов соединения будут помещены с соответствующими индексами; то есть значение минимальной доли элемента.
Пятый шаг
Минимальная формула соединения может быть преобразована в его молекулярную формулу, получая соотношение между молекулярной массой соединения и массой его минимальной формулы (n). Это соотношение такое же, как между молекулярной формулой и формулой минимума.
n = молекулярная масса соединения / масса минимальной формулы
Чтобы получить молекулярную формулу, умножьте формулу минимума на n. Это означает, что каждый из нижних индексов формулы минимума необходимо умножить на n.
n = Молекулярный вес / Минимальный вес формулы
= Молекулярная формула / Минимальная формула
Молекулярная формула = nминимальная формула
Примеры молекулярных формул
Некоторые общие молекулярные формулы перечислены ниже:
-Гидроксид натрия (NaOH)
-Оксид хлорной кислоты (Cl2ИЛИ7)