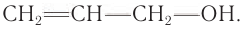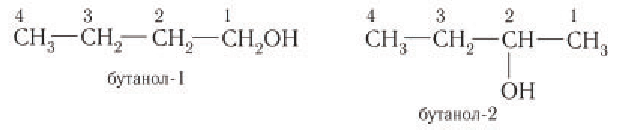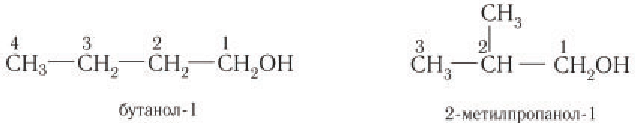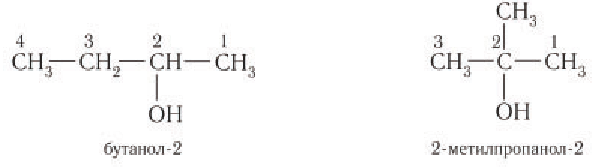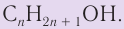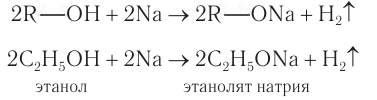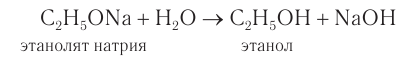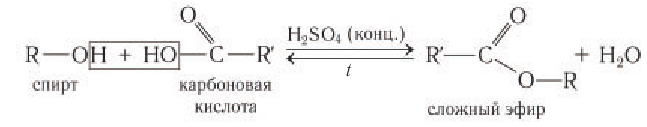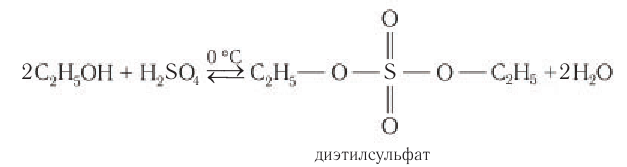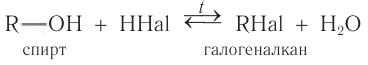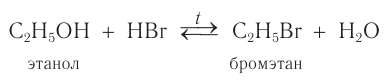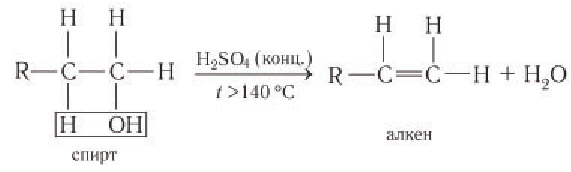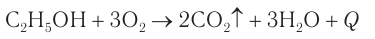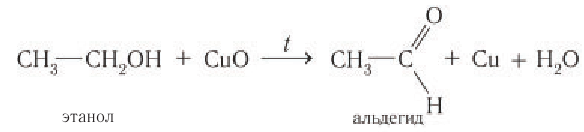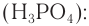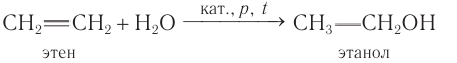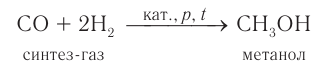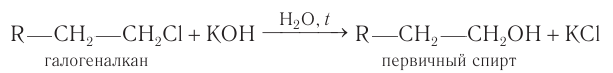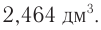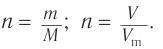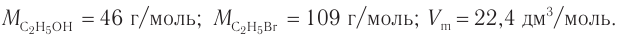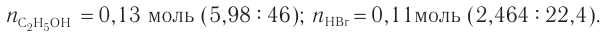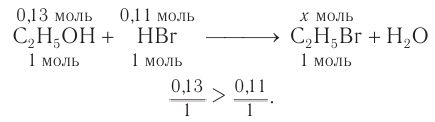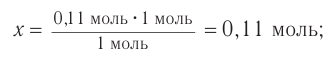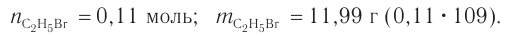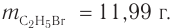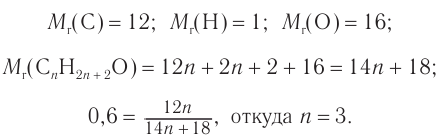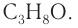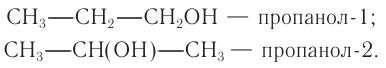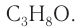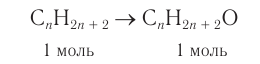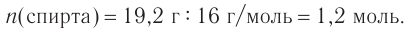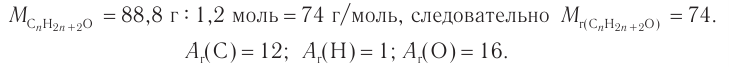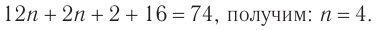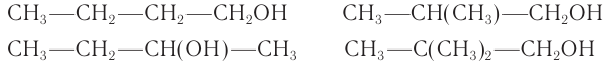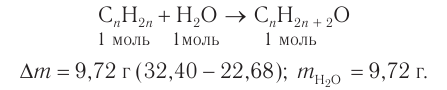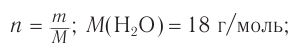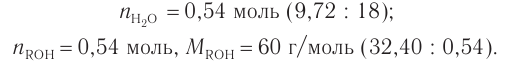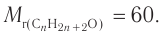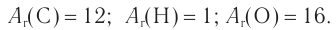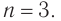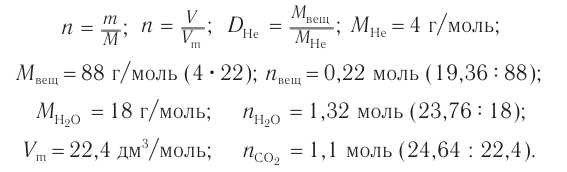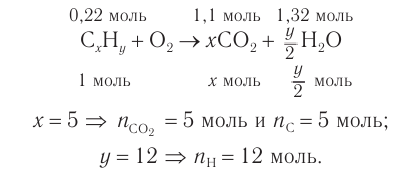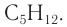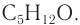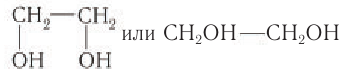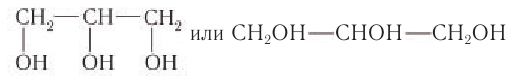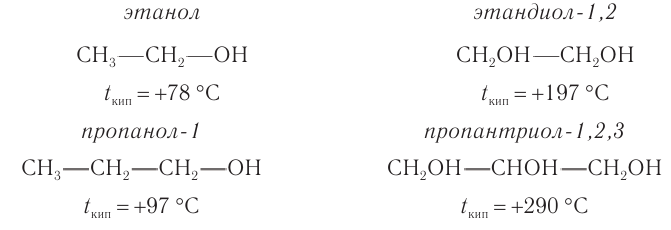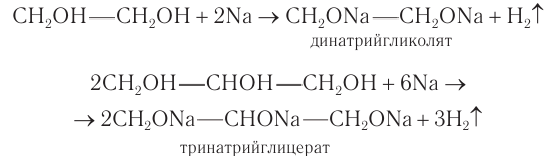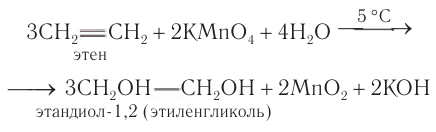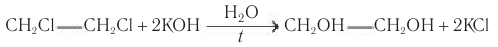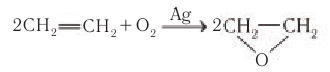Формула питьевого спирта
Определение и формула питьевого спирта
В обычных условиях представляет собой горючую бесцветную жидкость с характерным запахом и жгучим вкусом. Легче воды (плотность 0,7893 г/см 3 ). Хорошо растворяет многие органические вещества.
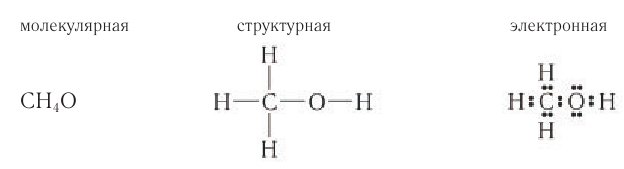
Химическая формула питьевого спирта
Химическая формула питьевого спирта C2H5OH. Она показывает, что в составе молекулы этого вещества находится два атома углерода (Ar = 12 а.е.м.), шесть атомов водорода (Ar = 1 а.е.м.) и один атом кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу питьевого спирта:
Mr(C2H5OH) = 2×12 + 6×1 + 16 = 24 + 6 + 16 = 46.
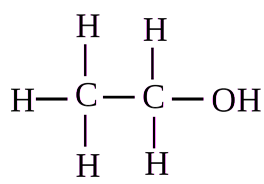
Структурная (графическая) формула питьевого спирта
Структурная (графическая) формула питьевого спирта является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
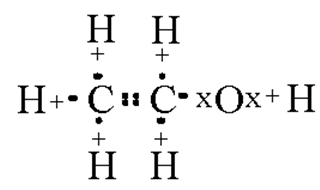
Электронная формула
Для питьевого спирта можно указать и электронную формулу:
Примеры решения задач
| Задание | Определите простейшую формулу соединения калия с марганцем и кислородом, если массовая доля калия равна 24,7%, марганца 34,8%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Вычислим массовую долю кислорода в соединении:
ω (P) = 100% — ω(K) — ω(Mn)= 100% — 24,7% — 34,8% = 40,5%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (марганец) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(K)/Ar(K) : ω(Mn)/Ar(Mn) : ω(O)/Ar(O);
x:y:z= 24,7/39 : 34,8/55 : 40,5/16;
x:y:z= 0,63 : 0,63:2,53 = 1 : 1: 4.
Значит формула соединения калия, марганца и кислорода будет иметь вид KMnO4. Это перманганат калия.
| Задание | Выведите простейшую формулу соединения, в котором массовая доля фосфора составляет 43,66%, а массовая доля кислорода – 56,34%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим число атомов фосфора в молекуле через «х», а число атомов кислорода через «у»
Найдем соответствующие относительные атомные массы элементов фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения:
x:y = 43,66/31 : 56,34/16;
x:y: = 1,4 : 3,5 = 1 : 2,5 = 2 : 5.
Значит простейшая формула соединения фосфора и кислорода имеет вид P2O5. Это оксид фосфора (V).
Спирты
Формула винного, или этилового, спирта (этанола) С2Н5ОН, несомненно, знакома многим даже совершенно далёким от химии людям. Это соединение, которое образуется при ферментативном брожении крахмала, глюкозы и фруктозы, в быту называют просто спиртом.
Получение вина путём сбраживания виноградного сока было освоено людьми уже несколько тысячелетий назад. Однако чистый спирт, содержащий лишь незначительное количество воды, выделили при перегонке вина только в XIII в. В Средние века стали известны многие свойства винного спирта, например горючесть (одно из его латинских названий — aqua ardens, что в переводе означает «огненная вода») и способность извлекать из листьев, плодов и кореньев содержащиеся в них биологически активные вещества и красители (полученные растворы в быту называют настойками). Алхимик Арнальдо из Вилановы упоминает спирт в числе медикаментов и противоядий.
Слово «спирт» происходит от древнего латинского названия этого вещества — spiritus vini («дух вина»). Этот термин до сих пор используется в медицине при записи рецептов. В XVI в. в западноевропейских языках, а в XVIII в. и в русском у винного спирта появилось название — алкоголь (араб. «ал-кугул»).
Безводный (абсолютный) этиловый спирт был впервые получен лишь в 1796 г. российским химиком Товием Егоровичем Ловицем и немецким ученым Иеремией Вениамином Рихтером. Для этой цели они применяли вещества, связывающие воду, например оксид кальция (негашёную известь). Абсолютный спирт легко поглощает влагу воздуха, поэтому его хранят в плотно закрытых сосудах.
Спирты (алкоголи) – это производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп – ОН у насыщенных атомов углерода.
Общая формула спиртов: R(OH)m, m≥1, где R – УВ радикал; m – число функциональных гидроксильных групп – ОН, которое определяет атомность спирта.
Классификация спиртов по строению УВ радикала:
Классификация спиртов по атомности:
Предельные одноатомные спирты (алканолы)
Общая формула: CnH2n+1OH, n≥1
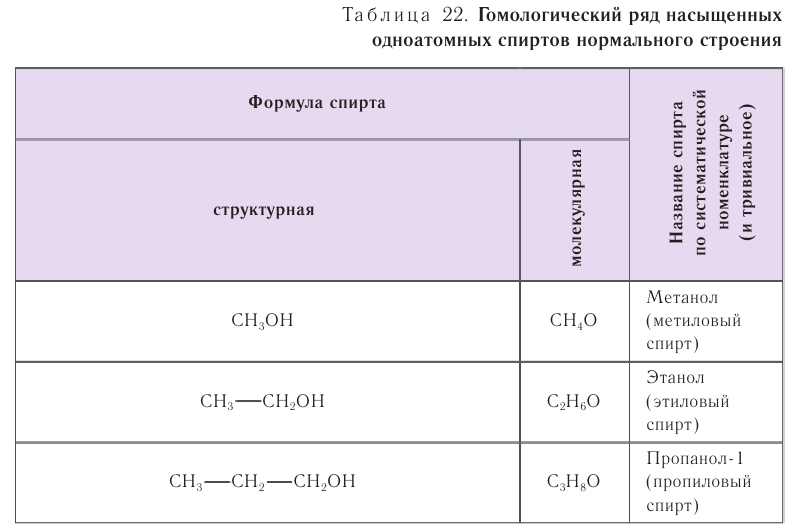
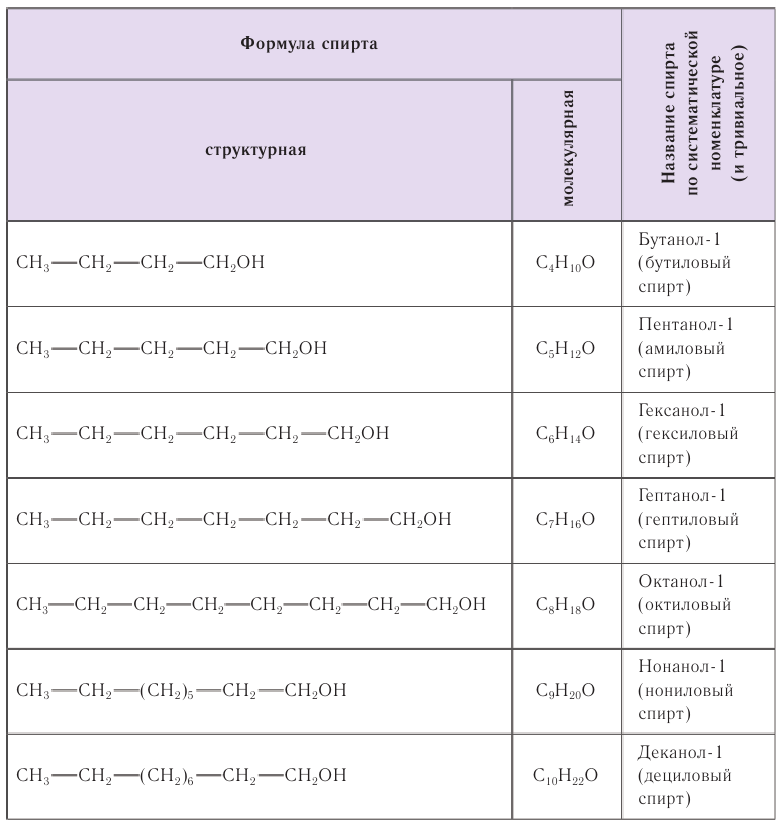
Гомологический ряд
Изомерия и номенклатура
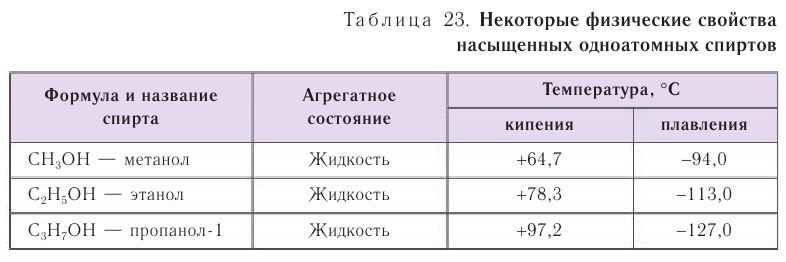
Первые два члена гомологического ряда – СН3ОН и С2Н5ОН – не имеют изомеров, относящихся к классу спиртов. Для остальных алканолов возможны 2 типа изомерии (в пределах своего класса):
— изомерия цепи (углеродного скелета);
— изомерия положения функциональной группы – ОН.
Спирты изомерны другому классу соединений – простым эфирам (R-O-R):
Электронное строение
Физические свойства
Полярность связи О—Н и наличие неподеленных пар электронов на атоме кислорода определяют физические свойства спиртов.
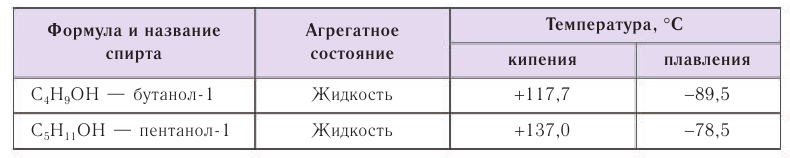
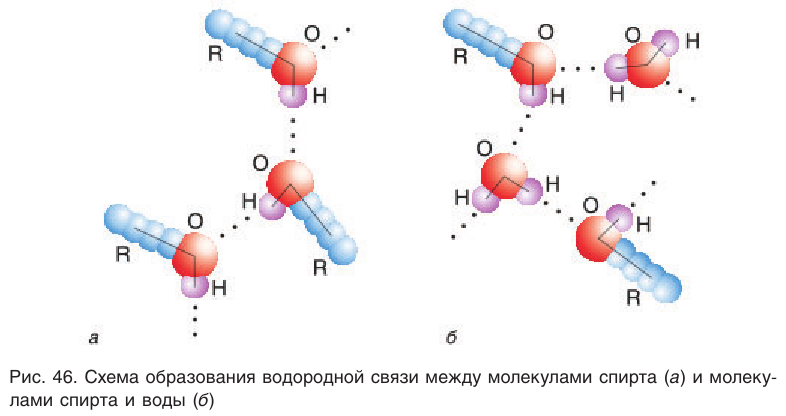
Температуры кипения спиртов больше температуры кипения соответствующих алканов с тем же числом атомов углерода. Это объясняется ассоциацией молекул спиртов вследствие образования межмолекулярных водородных связей.
Водородная связь — это особый вид связи, которая осуществляется при участии атома водорода гидроксильной или аминогруппы одной молекулы и атомами с большой электроотрицательностъю (О, N, F, Сl) другой молекулы. Чем большим положительным зарядом обладает атом водорода и чем больше способность другого атома отдавать свои неподеленные электронные пары, тем легче образуется водородная связь (ВС) и тем она прочнее.
Все алканолы легче воды, бесцветны, жидкие имеют резкий запах, твердые запаха не имеют. Метанол, этанол и пропанол неограниченно растворяются в воде, с увеличением числа углеродных атомов растворимость алканолов в воде уменьшается, высшие спирты не растворяются в воде.
Химические свойства
Химические свойства алканолов определяются особенностями их электронного строения: наличием в их молекулах полярных связей О-Н, С-О, С-Н. Для алканолов характерны реакции, которые идут с расщеплением этих связей: реакции замещения, отщепления, окисления.
I.Реакции замещения
1. Замещение атома водорода гидроксильной группы вследствие разрыва связи О-Н.
а) Взаимодействие с активными металлами с образованием алкоголятов металлов:
Эти реакции протекают только в безводной среде; в присутствии воды алкоголяты полностью гидролизуются:
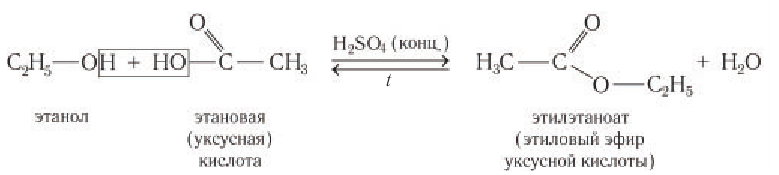
б) Взаимодействие с органическими и неорганическими кислотами с образованием сложных эфиров (реакции этерификации):
2. Замещение гидроксильной группы вследствие разрыва связи С-О.
а) Взаимодействие с галогеноводородами с образованием галогеналканов:
Следует отметить, что спирты можно превратить в галогенпроизводные действием и других реагентов, например хлоридов фосфора:
R – OH + PCl5 → R – Cl + POCl3 + HCl
б) Взаимодействие с аммиаком с образованием аминов.
Реакции идут при пропускании смеси паров спирта с аммиаком при 300 o С над оксидом алюминия:
При избытке спирта алкильными радикалами могут замещаться 2 или 3 атома водорода в молекуле NН3:
II. Реакции отщепления
1.Дегидратация, т.е. отщепление воды
Дегидратация спиртов может быть двух типов: межмолектлярная и внутримолекулярная.
а) Межмолекулярная дегидратация спиртов с образованием простых эфиров R—O—R’. Эти реакции могут протекать с участием одного спирта или смеси двух и более спиртов:
б) Внутримолекулярная дегидратация спиртов с образованием алкенов. Протекает при более высокой температуре. В отличие от межмолекулярной дегидратации в процессе этих реакций происходит отщепление молекулы воды от одной молекулы спирта:
Первый член гомологического ряда алканолов – метанол СН3ОН – не вступает в реакции внутримолекулярной дегидратации.
Дегидратация вторичных и третичных спиртов происходит по правилу Зайцева:
2.Дегидрирование (разрыв связей О – Н и С – Н)
а) При дегидрировании первичных спиртов образуются альдегиды:
В организме человека этот процесс происходит под действием фермента (алкогольдегидрогеназы).
б) При дегидрировании вторичных спиртов образуются кетоны:
в) Третичные спирты не дегидрируются.
III. Реакции окисления
1.Горение (полное окисление)
Спирты горят на воздухе с выделением большого количества тепла:
2.Неполное окисление под действием окислителей: кислорода воздуха в присутствии катализаторов (например, Cu), перманганата калия, дихромата калия и др.
Реакции неполного окисления спиртов по своим результатам аналогичны реакциям дегидрирования:
Способы получения алканолов
Кроме прямой гидратации этилена, существует также сернокислотная гидратация, протекающая в две стадии:
— на первой стадии этилен поглощается серной кислотой:
— на второй стадии этилсерная кислота гидролизуется с образованием этилового спирта и серной кислоты:
При гидратации гомологов этилена в соответствии с правилом Марковникова образуются вторичные или третичные спирты:
2.Гидролиз галогеналканов
При действии водного раствора NaOH атом галогена в галогеналкане замещается группой —ОН:
Обратите внимание, что при действии спиртового раствора щелочи на галогеналканы происходит отщепление галогеноводорода и образование алкена (см. способы получения алкенов).
3. Гидрирование альдегидов и кетонов
Как уже было отмечено выше, дегидрирование спиртов по своей химической сущности является окислением. Обратная реакция — гидрирование альдегидов и кетонов — является, таким образом, их восстановлением.
В присутствии катализаторов (Ni, Pt, Pd, Со) альдегиды восстанавливаются до первичных спиртов, а кетоны — до вторичных спиртов:
4.Специфические методы получения метанола и этанола
Этанол образуется при брожении (ферментации) углеводов – глюкозы или крахмала:
Предельные многоатомные спирты
Свойства многоатомных спиртов рассмотрим на примере простейшего трехатомного спирта – глицерина, или пропантриола-1,2,3:
Физические свойства
Глицерин – вязкая, бесцветная, сладковатая на вкус нетоксичная жидкость с t о кип.=230 о С. Смешивается с водой во всех отношениях.
Химические свойства
I. Замещение атомов водорода гидроксильных групп
1.Как и одноатомные спирты, многоатомные спирты взаимодействуют со щелочными металлами; при этом могут образовываться моно-, ди- и тризамещенные продукты:
2.Наличие нескольких ОН-групп в молекулах многоатомных спиртов обусловливает увеличение подвижности и способности к замещению гидроксильных атомов водорода по сравнению с одноатомными спиртами. Поэтому, в отличие от алканолов, многоатомные спирты взаимодействуют с гидроксидами тяжелых металлов (например, с гидроксидом меди (II) Cu(OH)2. Продуктами этих реакций являются внутрикомплексные («хелатные») соединения, в молекулах которых атом тяжелого металла образует как обычные ковалентные связи Ме←О за счет замещения атомов водорода ОН-групп, так и донорно-акцепторные связи Ме ←О за счет неподеленных электронных пар атомов кислорода других ОН-групп:
Нерастворимый в воде Cu(OH)2 голубого цвета растворяется в глицерине с образованием ярко-синего раствора глицерата меди (II). Эта реакция является качественной реакцией на все многоатомные спирты.
3.Многоатомные спирты, как и одноатомные, взаимодействуют с органическими и неорганическими кислотами с образованием сложных эфиров:
II. Замещение гидроксильных групп
Наиболее известными реакциями этого типа является взаимодействие многоатомных спиртов с галогеноводородами. Например, при взаимодействии глицерина с хлороводородом ОН-группы последовательно замещаются атомами хлора:
Способы получения глицерина
1.Гидролиз жиров – основной способ получения глицерина:
2. Синтез из пропилена
В последнее время глицерин получают из пропилена. Существует несколько вариантов этого синтеза. По одному из них пропилен хлорируют при t o = 440—500 о С, полученный аллилхлорид гидролизуют раствором NaOH. На полученный в результате гидролиза аллиловый спирт действуют пероксидом водорода Н2О2, который в присутствии катализатора присоединяется к спирту по двойной связи с образованием глицерина. Весь процесс можно представить схемой:
Применение важнейших спиртов
В медицине С2Н5ОН применяется как дезинфицирующее средство и средство для компрессов, используется для приготовления экстрактов и настоек, как растворитель для многих лекарственных препаратов.
Скачать:
Скачать бесплатно реферат на тему: «Спирты» Спирты.docx (252 Загрузки)
Скачать бесплатно реферат на тему: «Синтез этилового спирта» Синтез-этилового-спирта.docx (218 Загрузок)
Скачать бесплатно реферат на тему: «Синтез метанола из оксида углерода и водорода» Синтез-метанола-из-оксида-углерода-и-водорода.docx (226 Загрузок)
Скачать рефераты по другим темам можно здесь
Похожее
Добавить комментарий Отменить ответ
Репетитор по химии. Занятия проходят онлайн по Скайпу. По всем вопросам пишите в Ватсапп: +7 928 285 70 42
Содержание:
Спирты:
Углеводороды образуют различные функциональные производные при замещении в молекуле одного или нескольких атомов водорода на функциональную группу
Спирты и фенолы относятся к монофункциональным гидроксилпроизвод-ным углеводородов.
Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу —ОН.
Классификация спиртов
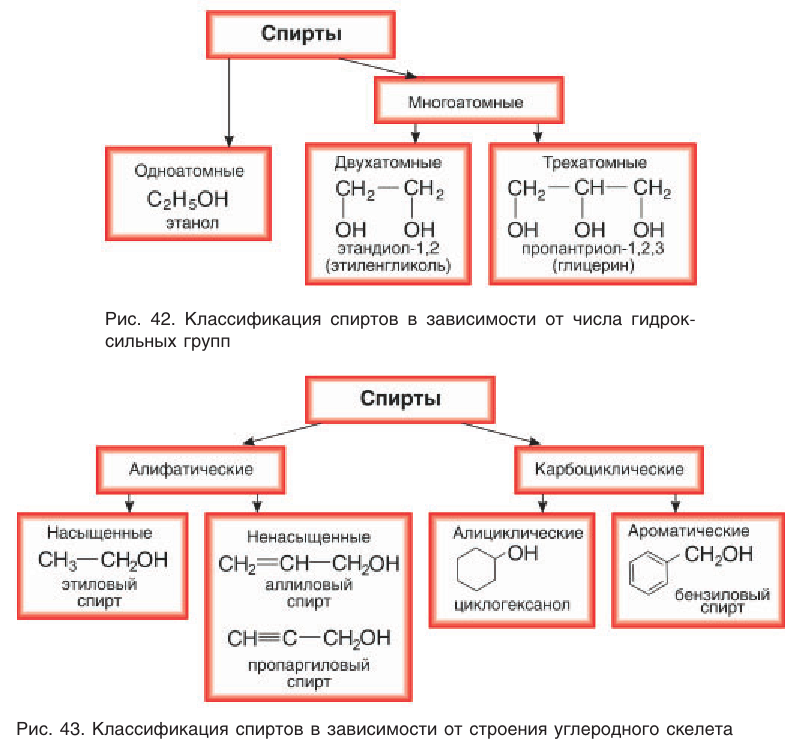
В зависимости от числа гидроксильных групп в молекуле спирты подразделяют на одноатомные, двухатомные, трехатомные, четырехатомные и т. д. (рис. 42). Например:
Спирты, содержащие несколько гидроксильных групп, объединяют общим названием многоатомные спирты.
В зависимости от строения углеродного скелета различают спирты насыщенные, ненасыщенные, ароматические (рис. 43).
Насыщенные спирты — производные алканов, например 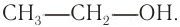
Некоторые одноатомные ненасыщенные спирты, содержащиеся в винограде, из которого производят вина, определяют характерный аромат ряда мускатных вин и рислингов. В процессе старения этих вин одноатомные спирты превращаются в двухатомные. По концентрации образовавшегося двухатомного спирта можно судить о степени старения вина.
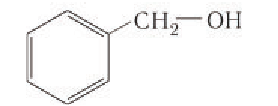
К ароматическим относят спирты, содержащие в молекуле бензольное кольцо и гидроксильную группу, которые связаны друг с другом через атом углерода, например:
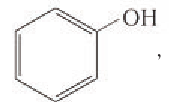
Если в молекулах органических соединений гидроксильные группы связаны непосредственно с атомом углерода бензольного кольца, например:
то такие соединения относят к другому классу органических соединений фенолам.
В лепестках розы (рис. 44) содержится ароматический фенилэтиловый спирт, формула которого 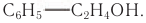
В зависимости от типа атома углерода, с которым связана гидроксильная группа, спирты классифицируют как первичные, вторичные, третичные.
Гидроксильная группа в молекулах первичных спиртов связана с первичным атомом углерода, в молекулах вторичных спиртов — с вторичным атомом углерода и в молекулах третичных спиртов — с третичным атомом углерода. Например:
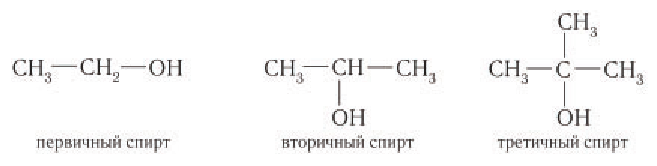
Спирты — производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу —ОН.
Спирты различают по числу гидроксильных групп (атомность спиртов), строению углеродного скелета, типу атома углерода, связанного с гидроксильной группой.
Насыщенные одноатомные спирты
Строение: Насыщенными одноатомными спиртами называют производные алканов, в молекулах которых один атом водорода замещен на гидроксильную группу и содержатся только 
В органической химии известно большое число насыщенных одноатомных спиртов, химический состав и строение которых выражается общей формулой 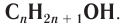
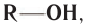
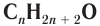
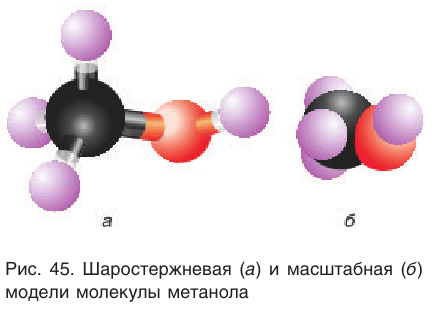
Простейшим представителем данного класса спиртов является метанол 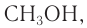
Шаростержневая и масштабная модели молекулы метанола представлены на рисунке 45.
Так как электронное строение алканов и соответствующих им алкильных групп вами уже изучено, то при изучении спиртов — производных алканов — будет рассматриваться только электронное строение функциональной группы спиртов 
В состав функциональной группы спиртов входит атом кислорода, который обладает большой электроотрицательностью и в силу этого оттягивает к себе электронную плотность 
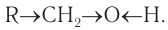
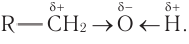
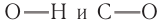
Номенклатура: По правилам номенклатуры ИЮПАК, названия насыщенных одноатомных спиртов образуются от названий соответствующих алканов с добавлением суффикса -ол. Например, 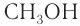
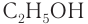
Систематическая номенклатура допускает употребление названий, связанных с названием алкильных групп, для низших членов ряда. Например, 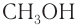
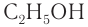
В таблице 22 приведены названия первых десяти представителей гомологического ряда спиртов, у которых функциональная группа —ОН находится у первичного атома углерода, по номенклатуре ИЮПАК и тривиальные.
При названии спиртов с неразветвленной углеродной цепью, начиная с пропанола, цифрой указывается атом углерода, с которым связана гидроксильная группа. Нумерация углеродных атомов начинается с того конца, ближе к которому расположена гидроксильная группа. Названия спиртов образуют, добавляя суффикс -ол к названию соответствующего алкана, цифрой указывается положение гидроксильной группы в цепи. Например:
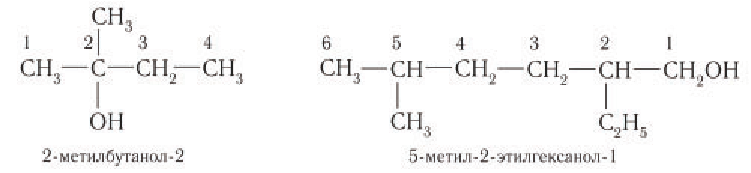
Для названий спиртов с разветвленной углеродной цепью выбирают самую длинную цепь, содержащую функциональную гидроксильную группу, и нумеруют с того конца, ближе к которому расположена гидроксильная группа. Названия спиртов образуют, добавляя суффикс -ол к назанию алкана, соответствующего самой длинной цепи, цифрой указываются атомы углерода, с которыми связана гидроксильная группа и заместители. Названия заместителей перечисляются в алфавитном порядке. Например:
Изомерия: Для насыщенных одноатомных спиртов характерна структурная изомерия. Структурная изомерия спиртов обусловлена изомерией углеродного скелета и изомерией положения гидроксильной группы. Первые два члена гомологического ряда — метанол 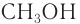
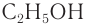
Рассмотрим примеры изомеров спиртов состава 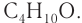
В зависимости от положения гидроксильной группы при том и другом углеродном скелете возможны еще два изомерных спирта:
Общее число структурных изомеров спиртов состава 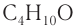
Физические свойства: Первые представители класса насыщенных одноатомных спиртов 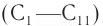
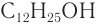
Низшие спирты обладают характерным алкогольным запахом, запах спиртов, стоящих в середине гомологического ряда, сильный и часто неприятный, а высшие спирты (более 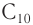
Низшие спирты (
Причиной отсутствия газообразных спиртов при нормальных условиях, а также более высоких температур кипения спиртов по сравнению с алканами с одинаковой относительной молекулярной массой являются межмолекулярные водородные связи, характерные для спиртов. Как отмечалось, связь 
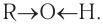
Образованием межмолекулярных водородных связей между молекулами спиртов и полярными молекулами воды (рис. 46, б) объясняется хорошая растворимость низших спиртов, в отличие от углеводородов, которые из-за малой полярности связей С—Н не образуют с водой водородных связей. С увеличением длины цепи алкильных групп растворимость спиртов понижается, и октанол уже не смешивается с водой.
Насыщенными одноатомными спиртами называют производные алканов, в молекулах которых один атом водорода замещен на гидроксильную группу.
Общая формула насыщенных одноатомных спиртов
Структурная изомерия спиртов обусловлена строением углеродного скелета и различным положением гидроксильной группы при одинаковой углеродной цепи.
На физические свойства спиртов большое влияние оказывает водородная связь между молекулами спиртов или молекулами спиртов и воды в их растворах.
Химические свойства спиртов
Характерные реакции спиртов определяются наличием в составе их молекул гидроксильиой группы, атом кислорода которой смещает электронную плотность как от атома водорода, так и от атома углерода. Такая поляризация может способствовать разрыву связей 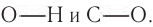
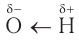
Рассмотрим важнейшие химические свойства спиртов на примере алифатических насыщенных одноатомных спиртов.
Взаимодействие со щелочными металлами: При взаимодействии щелочных металлов 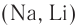

Спирты — очень слабые электролиты, слабее даже, чем вода. Поэтому алкокеиды (алкоголяты) легко разлагаются водой:
При взаимодействии с металлами у спиртов проявляются кислотные свойства, но к классу кислот спирты не относят, так как степень их диссоциации незначительна. Поэтому спирты с водными растворами щелочей взаимодействуют обратимо.
Взаимодействие с карбоновыми и кислородсодержащими минеральными кислотами с образованием сложных эфиров.
В реакции с карбоновыми кислотами от молекулы спирта отщепляется атом водорода, а от молекулы карбоновой кислоты — гидроксильная группа с образованием молекулы воды. Реакция обратима, но равновесие смещается вправо в присутствии концентрированной серной кислоты и при выводе воды из зоны реакции:
В реакциях с кислородсодержащими минеральными кислотами спирты образуют сложные эфиры этих кислот:
Взаимодействие с галогеноводородами с образованием галогеналканов
В реакции с галогеноводородами в молекуле спирта происходит разрыв связи 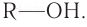
Данная реакция обратима. В этой реакции проявляются слабые основные свойства спирта.
При взаимодействии этанола с бромоводородом образуется бромэтан — тяжелая жидкость:
Внутримолекулярная дегидратация с образованием алкена
Первичные спирты дегидратируются под действием катализатора — концентрированной серной кислоты — при высоких температурах (выше 140 °С) с образованием алкена:
Реакция дегидратации обусловлена отщеплением водорода в виде протона и гидроксильной группы от соседних атомов углерода.
Например, в результате внутримолекулярного отщепления молекулы воды от молекулы этанола (под действием катализатора — концентрированной серной кислоты) образуется этен:
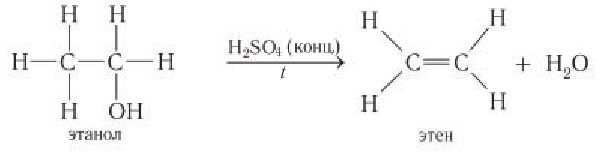
Реакции окисления
Спирты горят на воздухе или в кислороде некоптящим пламенем с выделением большого количества теплоты (рис. 48):
С более слабым, чем кислород, окислителем, например с оксидом меди(II), происходит частичное окисление спиртов, при этом первичные спирты окисляются до альдегидов.
Если в пробирку с этанолом опустить раскаленную скрученную в спираль медную проволоку, покрытую черным налетом оксида меди(II), то черный налет на проволоке исчезает. Спираль приобретает розово-красный цвет, при этом чувствуется неприятный запах образовавшегося альдегида:
Под действием таких окислителей, как подкисленный раствор перманганата калия или дихромата калия, первичные спирты окисляются до карбоновых кислот.
Кислотно-основные свойства насыщенных одноатомных спиртов обусловлены наличием в их молекулах функциональной гидроксильной группы.
Спирты взаимодействуют со щелочными металлами, галогеноводородами, карбоновыми и минеральными кислотами; вступают в реакции дегидратации и окисления.
Получение и применение спиртов
Получение: Для промышленного получения спиртов используют ненасыщенные углеводороды, извлекаемые из нефтепродуктов, или галогеналканы.
Познакомимся с основными общими промышленными и лабораторными способами получения насыщенных одноатомных спиртов и специфическими способами получения этанола и метанола.
1) Одним из наиболее важных общих промышленных способов получения спиртов является гидратация алкенов.
Этанол получают гидратацией этена водяными парами при повышенной температуре (280—300 °С), повышенном давлении (7—8 мПа) и в присутствии катализатора
Спирт, полученный из этена, называют синтетическим.
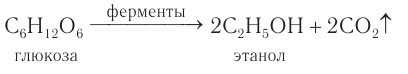
2) В пищевой промышленности этанол получают характерным только для него способом при спиртовом брожении глюкозы под действием ферментов, выделяемых некоторыми видами дрожжевых грибков:
Брожению подвергают виноградный сок, содержащий глюкозу, а также картофельный крахмал, который превращается в глюкозу под действием особого фермента. Этанол, полученный при ферментативном расщеплении различных пищевых продуктов, используют в основном для изготовления спиртных напитков.
В промышленности этанол производят гидролизным способом из древесных опилок, отходов целлюлозно-бумажной промышленности и т. д. Содержащуюся в древесине целлюлозу подвергают гидролизу с образованием глюкозы, которую далее подвергают брожению, и получают этанол, называемый гидролизным спиртом.
3) В промышленности метанол получают характерным только для него способом при взаимодействии водорода с угарным газом (СО) при повышенном давлении и высокой температуре в присутствии катализатора:
Смесь угарного газа и водорода, взятых в количественном соотношении 1 : 2, называют синтез-газом.
Историческое название метанола — древесный спирт. Оно указывает на старый способ получения спирта — сухую перегонку древесины твердых пород дерева (нагревание древесины без доступа воздуха).
Для получения спиртов в лаборатории используют галогеналканы.
При гидролизе моногалогеналканов с галогеном при первичном атоме углерода в водных растворах щелочей при нагревании образуются первичные спирты:
Гидролиз галогеналканов, проводимый в присутствии щелочи, является практически необратимым процессом и используется как общий метод получения первичных насыщенных спиртов в лаборатории.
Применение: Спирты находят широкое применение. В химической промышленности спирты — исходные вещества для разнообразных синтезов. Во многих производствах спирты применяют в качестве растворителей. Рассмотрим несколько примеров промышленного использования важнейших насыщенных одноатомных спиртов.
Метанол (метиловый спирт) 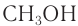
Метанол — прекрасный растворитель для многих органических и неорганических веществ.
Этанол (этиловый спирт) 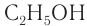
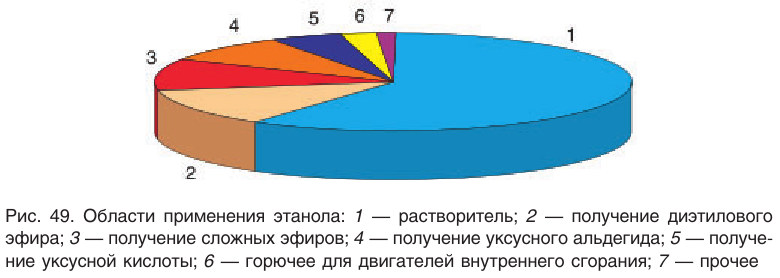
Этанол является исходным веществом в промышленном органическом синтезе (диэтиловый эфир, этилацетат и другие эфиры и т. д.), окислением этанола получают пищевую уксусную кислоту.
Спирт-ректификат, получаемый в промышленности, представляет собой смесь этанола (массовая доля 95,6 %) и воды (массовая доля 4,4 %). Безводный спирт называют абсолютным спиртом.
В этанол, применяемый для технических целей, специально добавляют небольшие количества трудноотделяемых ядовитых, плохо пахнущих и имеющих отвратительный вкус веществ и подкрашивают. Содержащий такие добавки спирт называют денатуратом. Употребление денатурата смертельно опасно.
Другие (низшие) спирты используются в качестве растворителей при изготовлении различных лаков и красок на предприятиях лакокрасочной промышленности, одним из которых является ОАО «Лакокраска» в Лиде.
Высшие спирты ( 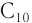
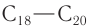


Ненасыщенный аллиловый спирт 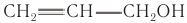
В промышленном масштабе этанол получают гидратацией этена, гидролизным способом, в процессе спиртового брожения глюкозы.
Метанол в промышленных масштабах в основном получают из синтез-газа.
В лаборатории первичные насыщенные одноатомные спирты получают в процессе щелочного гидролиза моногалогеналканов.
Спирты используют для синтеза многих органических веществ.
Решение расчетных задач
В параграфе рассмотрены образцы решения задач таких типов, как расчеты по химическим уравнениям, если одно из реагирующих веществ взято в избытке, и определение молекулярных формул органических веществ на основании качественного и количественного состава.
Пример 1.
Определите массу бромэтана, полученного в реакции, для которой был взят этанол массой 5,98 г и бромоводород объемом (н. у.)
Решение
1. Общие формулы, используемые при расчетах:
2. Значения молярных масс веществ, молярный объем:
3. Определяем химические количества спирта и бромоводорода, взятых для реакции:
4. На основе анализа уравнения реакции определяем, какое из веществ взято в избытке, а затем рассчитываем химическое количество и массу продукта реакции:
Следовательно, спирт взят в избытке. Расчеты продукта реакции проводятся исходя из данных о химическом количестве хлороводорода:
Ответ:
Пример 2.
Массовая доля углерода в насыщенном одноатомном спирте равна 0,6. Определите молекулярную формулу спирта. Составьте структурные формулы возможных изомеров и назовите их по номенклатуре ИЮПАК.
Решение
1. Для решения задачи используем общую формулу 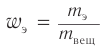
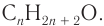
2. Определяем формулу искомого спирта.
Общая формула 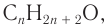
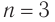
Ответ:
Пример 3.
В результате ряда последовательных реакций из алкана массой 69,6 г получен первичный насыщенный одноатомный спирт массой 88,8 г с тем же числом атомов углерода в молекуле, что и у алкана (алкан 

Решение
1. Из алкана химическим количеством 1 моль получают спирт химическим количеством 1 моль:
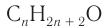
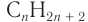
3. Используя общую формулу 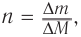
4. Зная химическое количество и массу спирта, определяем его молярную массу и молекулярную формулу:
Решая уравнение
Следовательно, молекулярная формула спирта — 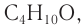
Ответ: 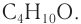
Пример 4.
При гидратации алкена массой 22,68 г получили вторичный насыщенный одноатомный спирт массой 32,40 г. Определите молекулярную формулу спирта, составьте структурную формулу и назовите спирт по номенклатуре ИЮПАК.
Решение
1. Анализ уравнения реакции гидратации, записанного в общем виде, показывает, что для гидратации алкена химическим количеством 1 моль требуется вода химическим количеством 1 моль. Следовательно, разница масс алкена и спирта и есть масса присоединенной воды:
2. Определяем химическое количество воды и спирта, далее молярную массу и молекулярную формулу спирта:
Следовательно,
Решая уравнение 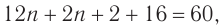
Молекулярная формула спирта — 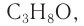
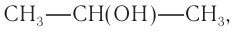
Ответ: 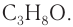
Пример 5.
Определите молекулярную формулу органического вещества, относительная плотность паров которого по гелию равна 22, если при сгорании его массой 19,36 г образовались углекислый газ объемом (н. у.) 2 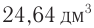
Решение
1. Определяем молярную массу неизвестного вещества, его химическое количество, а также химические количества образовавшихся оксида углерода (IV) и воды:
2. Проанализируем схему реакции горения вещества, предположив, что сожгли углеводород химическим количеством 1 моль. На основе данных о продуктах реакции рассчитаем количественный состав вещества:
Формула вещества —
3. Молярная масса вещества 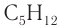
Ответ: 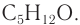
Многоатомные спирты
Строение: Производные углеводородов, в молекулах которых два и более атомов водорода у соседних атомов углерода замещены на гидроксильные группы, называют многоатомными спиртами.
Гидроксильные группы во всех устойчивых многоатомных спиртах связаны с соседними атомами углерода.
Простейшим представителем двухатомных спиртов (гликолей) является этиленгликоль, структурная формула которого:
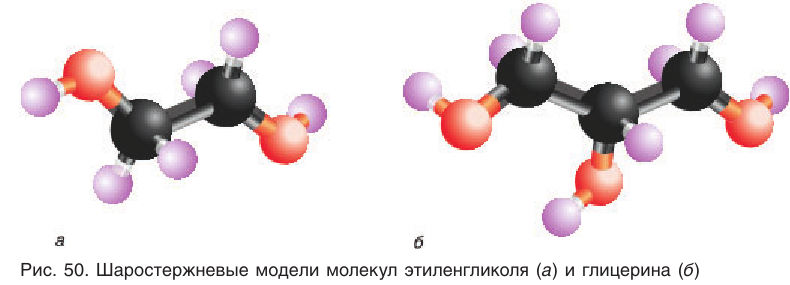
Шаростержневая модель молекулы этиленгликоля приведена на рисунке 50, а.
Простейшим представителем трехатомных спиртов (глицеринов) является глицерин (от греч. glykeros — сладкий), структурная формула которого:
Шаростержневая модель молекулы глицерина приведена на рисунке 50, б.
На примере этих двух спиртов вы познакомитесь с основными характеристиками многоатомных спиртов.
Номенклатура: По номенклатуре ИЮНАК двухатомный спирт 
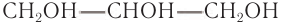
Физические свойства: Этиленгликоль и глицерин — бесцветные вязкие жидкости, тяжелее воды, неограниченно растворимы в воде, хорошо растворяются в этаноле. Эти свойства присущи и другим многоатомным спиртам.
Этиленгликоль ядовит, его водные растворы не кристаллизуются при низких температурах, что позволяет применять его как компонент незамерзающих жидкостей — антифризов. Глицерин имеет сладковатый вкус, гигроскопичен, нелетуч.
Впервые глицерин был получен из оливкового масла шведским химиком и фармацевтом К. Шееле в 1783 г.
Хорошая растворимость этиленгликоля и глицерина в воде объясняется наличием межмолекулярных водородных связей между молекулами спиртов и воды. Число таких связей больше, чем у одноатомных спиртов, из-за большего числа гидроксильных групп в молекулах.
Температуры кипения этих спиртов по сравнению с одноатомными спиртами с таким же числом атомов угелерода в молекуле намного выше:
Причиной более высоких температур кипения многоатомных спиртов является большее число межмолекулярных водородных связей между молекулами спиртов за счет большего числа гидроксильных групп в составе молекул.
Химические свойства: Для этиленгликоля и глицерина характерны все реакции одноатомных спиртов, обусловленные наличием функциональной группы —ОН, и особые свойства, обусловленные одновременным присутствием в молекуле нескольких гидроксильных групп.
1) Взаимодействие со щелочными металлами. Многоатомные спирты реагируют с активными металлами с образованием соединений, которые по аналогии с алкоголятами называют гликолятами и глицератами. Названия «гликоляты» и «глицераты» допускаются в номенклатуре ИЮНАК.
В реакциях могут участвовать одна или более гидроксильных групп. Многоатомные спирты, как и одноатомные, проявляют кислотные свойства в реакциях со щелочными металлами.
2) Взаимодействие с основаниями. В отличие от одноатомных спиртов, этиленгликоль и глицерин реагируют не только со щелочными металлами, но и с нерастворимыми гидроксидами тяжелых металлов. Такие реакции возможны для многоатомных спиртов, потому что из-за взаимного влияния гидроксильных групп в молекуле их кислотность выше, чем у одноатомных спиртов.
Если в стакан с раствором щелочи добавить несколько капель раствора сульфата меди(II) и к образовавшемуся гидроксиду меди(II) прилить многоатомный спирт, например глицерин, то образуется прозрачный раствор ярко-синего цвета (рис. 51). Цвет раствора обусловлен образованием комплексного соединения меди.
Реакция со свежеприготовленным гидроксидом меди(II) является качественной реакцией на многоатомные спирты с гидроксильными группами, находящимися у соседних атомов углерода. Из-за сложности строения образовавшегося глицерата меди уравнение реакции не приводится.
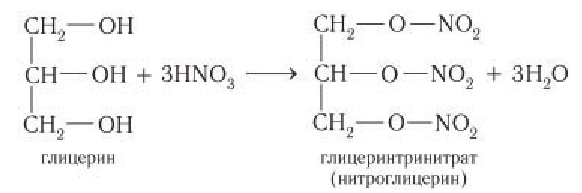
3) Образование сложных эфиров. Для многоатомных спиртов, как и для одноатомных, характерно образование сложных эфиров при взаимодействии с кислородсодержащими минеральными кислотами и карбоновыми кислотами. В частности, в реакции глицерина с избытком азотной кислоты в присутствии каталитических количеств серной кислоты образуется глицеринтринитрат, известный под названием нитроглицерин:
Название «нитроглицерин» относится к тривиальным названиям, оно не отражает строение вещества. Известно, что в химии к нитросоединениям относят вещества, в которых группа — 
Реакцию глицерина с карбоновыми кислотами е образованием сложных эфиров вы будете рассматривать при изучении темы «Жиры».
Получение: Двухатомные и трехатомные спирты можно получать теми же способами, что и одноатомные спирты. В качестве исходных веществ используются алкены и галогеналканы.
Лабораторные способы: Общим способом получения гликолей является окисление алкенов раствором перманганата калия в слабощелочной или нейтральной среде:
Этиленмиколь также получают гидролизом соответствующего дигалогеналкана:
Промышленные способы. Глицерин получают в процессе гидролиза жиров и синтетическим способом из пропена, образующегося при крекинге нефтепродуктов.
Этиленгликоль в промышленных масштабах получают гидратацией эпоксида 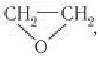
Применение глицерина основано на его гигроскопичности. Его используют для приготовления мазей, в кожевенном производстве — для предохранения кож от высыхания, в текстильной промышленности — для отделки тканей с целью придания им мягкости и эластичности и др. Глицерин применяют при изготовлении косметики, где он играет роль смягчающего и успокаивающего средства; как добавку к зубной пасте, клеям, чтобы предохранить их от быстрого высыхания; для приготовления антифризов.
Незамерзание клеточной жидкости иногда объясняют усиленной выработкой глицерина в растительных клетках.
Большое количество глицерина идет на получение нитроглицерина, который служит сырьем при производстве бездымных порохов и динамита.
Нитроглицерин токсичен, но в малых дозах используется как лечебное средство, так как расширяет кровеносные сосуды сердечной мышцы и тем самым улучшает кровоснабжение сердца.
Многоатомными спиртами называют производные углеводородов, в молекулах которых содержится несколько гидроксильных групп, связанных с соседними атомами углерода.
Многоатомные спирты взаимодействуют с активными металлами, щелочами, гидроксидами тяжелых металлов, кислородсодержащими неорганическими кислотами и карбоновыми кислотами.
Реакция с гидроксидом меди(II) используется для качественного обнаружения многоатомных спиртов.
Этиленгликоль применяют для получения синтетического волокна лавсан, в качестве антифриза; глицерин используется во многих отраслях промышленности.
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.