Вопрос № 2 Как получают кислород в лаборатории ив промышленности? Напишите уравнения соответствующих реакций. Чем отличаются эти способы друг от друга?
Вопрос № 2 Как получают кислород в лаборатории ив промышленности? Напишите уравнения соответствующих реакций. Чем отличаются эти способы друг от друга?
В лаборатории кислород можно получить следующими способами:
1) Разложение перекиси водорода в присутствии катализатора (оксида марганца
2) Разложение бертолетовой соли (хлората калия):
3) Разложение перманганата калия:
В промышленности кислород получают из воздуха, в котором его содержится около 20% по объему. Воздух сжижают под давлением и при сильном охлаждении. Кислород и азот (второй основной компонент воздуха) имеют разные температуры кипения. Поэтому их можно разделить перегонкой: азот имеет более низкую температуру кипения, чем кислород, поэтому азот испаряется раньше кислорода.
Отличия промышленных и лабораторных способов получения кислорода:
1) Все лабораторные способы получения кислорода химические, то есть при этом происходит превращение одних веществ в другие. Процесс получения кислорода из воздуха — физический процесс, поскольку превращение одних веществ в другие не происходит.
2) Из воздуха кислорода можно получать в гораздо больших количествах.
Получение кислорода
История открытия кислорода
Открытие кислорода ознаменовало новый период в развитии химии. С глубокой древности было известно, что для горения необходим воздух. Процесс горения веществ долгое время оставался непонятным. В эпоху алхимии широкое распространение получила теория флогистона, согласно которой вещества горят благодаря их взаимодействию с огненной материей, то есть с флогистоном, который содержится в пламени. Кислород был получен английским химиком Джозефом Пристли в 70-х годах XVIII века. Химик нагревал красный порошок оксида ртути (II), в итоге вещество разлагалось, с образованием металлической ртути и бесцветного газа:
Оксиды – бинарные соединения, в состав которых входит кислород При внесении тлеющей лучины в сосуд с газом она ярко вспыхивала. Ученый считал, что тлеющая лучина вносит в газ флогистон, и он загорается. Д. Пристли пробовал дышать полученным газом, и был восхищен тем, как легко и свободно им дышится. Тогда ученый и не предполагал, что удовольствие дышать этим газом предоставлено каждому. Результатами своих опытов Д. Пристли поделился с французским химиком Антуаном Лораном Лавуазье.
Имея хорошо оснащенную на то время лабораторию, А. Лавуазье повторил и усовершенствовал опыты Д. Пристли. А. Лавуазье измерил количество газа, выделяющееся при разложении определенной массы оксида ртути. Затем химик нагрел в герметичном сосуде металлическую ртуть до тех пор, пока она не превратилась в оксид ртути (II). Он обнаружил, что количество выделившегося газа в первом опыте равно газу, поглотившемуся во втором опыте. Следовательно, ртуть реагирует с каким-то веществом, содержащимся в воздухе. И это же вещество выделяется при разложении оксида. Лавуазье первым сделал вывод, что флогистон здесь совершенно ни при чем, и горение тлеющей лучины вызывает именно неизвестный газ, который в последствии был назван кислородом. Открытие кислорода ознаменовало крах теории флогистона!
Способы получения и собирания кислорода в лаборатории
Лабораторные способы получения кислорода весьма разнообразны. Существует много веществ, из которых можно получить кислород. Рассмотрим наиболее распространенные способы.
1) Разложение оксида ртути (II)
Одним из способов получения кислорода в лаборатории, является его получение по описанной выше реакции разложения оксида ртути (II). Ввиду высокой токсичности соединений ртути и паров самой ртути, данный способ используется крайне редко.
2) Разложение перманганата калия
Перманганат калия (в быту мы называем его марганцовкой) – кристаллическое вещество темно-фиолетового цвета. При нагревании перманганата калия выделяется кислород. В пробирку насыплем немного порошка перманганата калия и закрепим ее горизонтально в лапке штатива. Недалеко от отверстия пробирки поместим кусочек ваты. Закроем пробирку пробкой, в которую вставлена газоотводная трубка, конец которой опустим в сосуд- приемник. Газоотводная трубка должна доходить до дна сосуда-приемника. Ватка, находящаяся около отверстия пробирки нужна, чтобы предотвратить попадание частиц перманганата калия в сосуд-приемник (при разложении выделяющийся кислород увлекает за собой частички перманганата). Когда прибор собран, начинаем нагревание пробирки. Начинается выделение кислорода.
Уравнение реакции разложения перманганата калия:
2KMnO4 t° → K2MnO4 + MnO2 + O2↑
Как обнаружить присутствие кислорода? Воспользуемся способом Пристли. Подожжем деревянную лучину, дадим ей немного погореть, затем погасим, так, чтобы она едва тлела. Опустим тлеющую лучину в сосуд с кислородом. Лучина ярко вспыхивает! Газоотводная трубка была не случайно опущена до дна сосуда-приемника. Кислород тяжелее воздуха, следовательно, он будет собираться в нижней части приемника, вытесняя из него воздух. Кислород можно собрать и методом вытеснения воды. Для этого газоотводную трубку необходимо опустить в пробирку, заполненную водой, и опущенную в кристаллизатор с водой вниз отверстием. При поступлении кислорода газ вытесняет воду из пробирки.
Разложение пероксида водорода
Пероксид водорода – вещество всем известное. В аптеке оно продается под названием «перекись водорода». Данное название является устаревшим, более правильно использовать термин «пероксид». Химическая формула пероксида водорода Н2О2 Пероксид водорода при хранении медленно разлагается на воду и кислород. Чтобы ускорить процесс разложения можно произвести нагрев или применить катализатор.
Катализатор – вещество, ускоряющее скорость протекания химической реакции
Нальем в колбу пероксид водорода, внесем в жидкость катализатор. Катализатором может служить порошок черного цвета – оксид марганца MnO2. Тотчас смесь начнет вспениваться вследствие выделения большого количества кислорода. Внесем в колбу тлеющую лучину – она ярко вспыхивает. Уравнение реакции разложения пероксида водорода:
2H2O2 MnO2 → 2H2O + O2↑
Обратите внимание: катализатор, ускоряющий протекание реакции, записывается над стрелкой, или знаком «=», потому что он не расходуется в ходе реакции, а только ускоряет ее.
Разложение хлората калия
Хлорат калия – кристаллическое вещество белого цвета. Используется в производстве фейерверков и других различных пиротехнических изделий. Встречается тривиальное название этого вещества – «бертолетова соль». Такое название вещество получило в честь французского химика, впервые синтезировавшего его, – Клода Луи Бертолле. Химическая формула хлората калия KСlO3. При нагревании хлората калия в присутствии катализатора – оксида марганца MnO2, бертолетова соль разлагается по следующей схеме:
2KClO3 t°, MnO2 → 2KCl + 3O2↑.
Разложение нитратов
Нитраты – вещества, содержащие в своем составе ионы NO3⎺. Соединения данного класса используются в качестве минеральных удобрений, входят в состав пиротехнических изделий.
Нитраты – соединения термически нестойкие, и при нагревании разлагаются с выделением кислорода:
Обратите внимание, что все рассмотренные способы получения кислорода схожи. Во всех случаях кислород выделяется при разложении более сложных веществ.
Реакция разложения – реакция, в результате которой сложные вещества разлагаются на более простые В общем виде реакцию разложения можно описать буквенной схемой:
Реакции разложения могут протекать при действии различных факторов. Это может быть нагревание, действие электрического тока, применение катализатора. Существуют реакции, в которых вещества разлагаются самопроизвольно.
Получение кислорода в промышленности
В промышленности кислород получают путем выделения его из воздуха.
Воздух – смесь газов, основные компоненты которой представлены в таблице.
Сущность этого способа заключается в глубоком охлаждении воздуха с превращением его в жидкость, что при нормальном атмосферном давлении может быть достигнуто при температуре около -192°С. Разделение жидкости на кислород и азот осуществляется путем использования разности температур их кипения, а именно: Ткип.
При постепенном испарении жидкости в газообразную фазу в первую очередь будет переходить азот, имеющий более низкую температуру кипения, и, по мере его выделения, жидкость будет обогащаться кислородом. Многократное повторение этого процесса позволяет получить кислород и азот требуемой чистоты. Такой способ разделения жидкостей на составные части называется ректификацией жидкого воздуха.
Получение кислорода

Всего получено оценок: 177.
Всего получено оценок: 177.
Кислород появился в земной атмосфере с возникновением зелёных растений и фотосинтезирующих бактерий. Благодаря кислороду аэробными организмами осуществляется дыхание или окисление. Важно получение кислорода в промышленности – он используется в металлургии, медицине, авиации, народном хозяйстве и других отраслях.
Свойства
Кислород – восьмой элемент периодической таблицы Менделеева. Это газ, поддерживающий горение и осуществляющий окисление веществ.
Официально кислород был открыт в 1774 году. Английский химик Джозеф Пристли выделил элемент из оксида ртути:
Однако Пристли не знал, что кислород является частью воздуха. Свойства и нахождение в атмосфере кислорода позже уставил коллега Пристли – французский химик Антуан Лавуазье.
Общая характеристика кислорода:
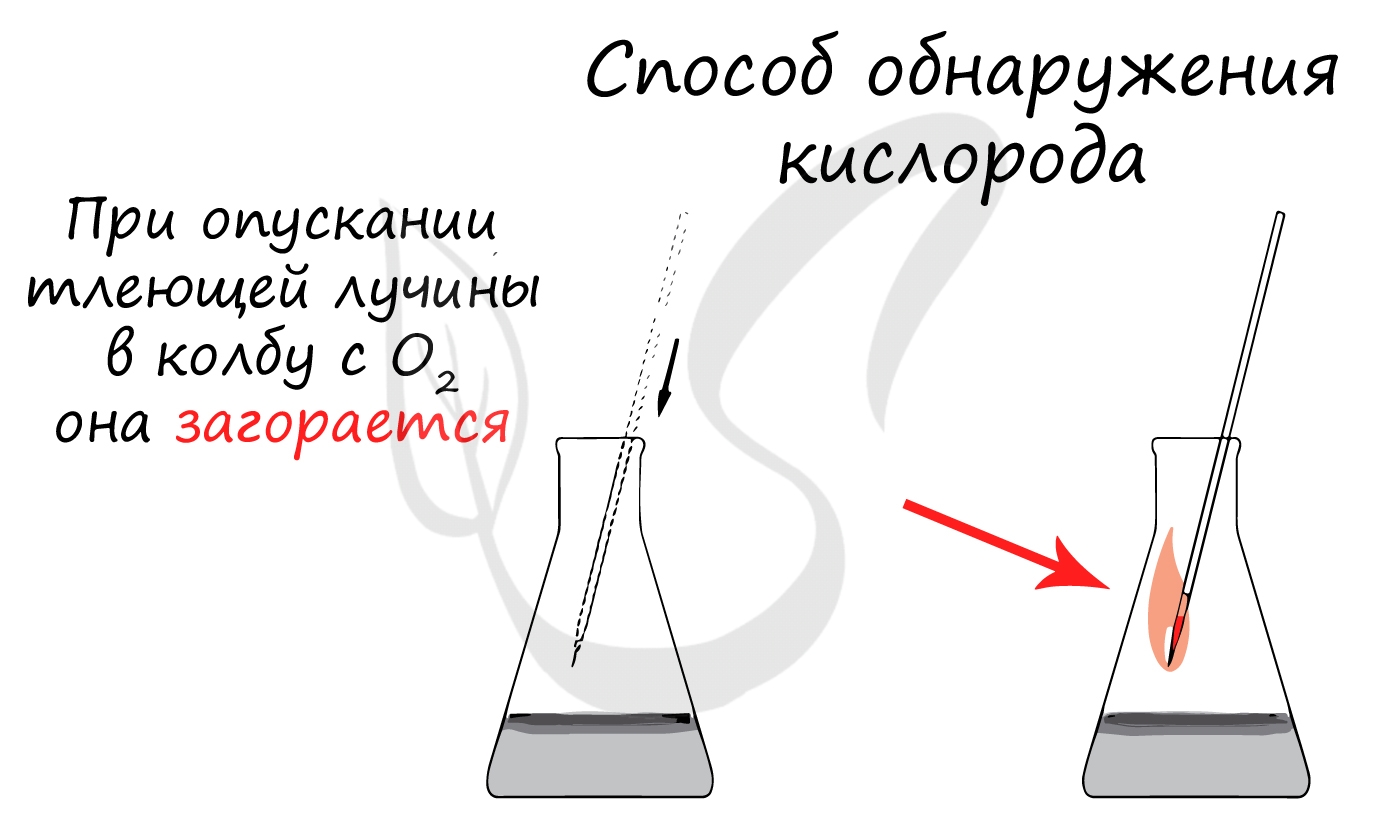
Присутствие кислорода легко проверить, опустив в сосуд с газом тлеющую лучину. При наличии кислорода лучина вспыхивает.
Как получают
В лаборатории кислород образуется из солей, пероксида водорода и в результате электролиза. Разложение солей происходит при нагревании. Например, хлорат калия или бертолетову соль нагревают до 500°С, а перманганат калия или марганцовку – до 240°С:
Также можно получить кислород путём нагревания селитры или нитрата калия:
При разложении пероксида водорода используется оксид марганца (IV) – MnO2, углерод или порошок железа в качестве катализатора. Общее уравнение выглядит следующим образом:
Электролизу подвергается раствор гидроксида натрия. В результате образуется вода и кислород:
Также кислород с помощью электролиза выделяют из воды, разложив её на водород и кислород:
На атомных подводных лодках кислород получали из пироксида натрия – 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑. Способ интересен тем, что вместе с выделением кислорода поглощается углекислый газ.
Как применяют
Собирание и распознавание необходимо для выделения чистого кислорода, использующегося в промышленности для окисления веществ, а также для поддержания дыхания в космосе, под водой, в задымлённых помещениях (кислород необходим пожарным). В медицине баллоны кислорода помогают дышать пациентам с затруднённым дыханием. Также кислород используется для лечения респираторных заболеваний.
Кислород применяют для сжигания топлива – угля, нефти, природного газа. Кислород широко применяется в металлургии и машиностроении, например, для плавки, резки и сварки металла.
Что мы узнали?
Кислород – бесцветный газ, необходимый для дыхания и используемый в промышленности. Кислород получают путём сжижения и испарения воздуха, электролизом воды или гидроксида натрия, выделяют из солей и пероксида водорода. Кислород используется для поддержания дыхания в местах с ограниченным запасом кислорода или его отсутствием, а также в промышленности для сжигания топлива и производства металла.
Кислород
Газ без цвета, без запаха, составляет 21% воздуха.
Общая характеристика элементов VIa группы
От O к Po (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.
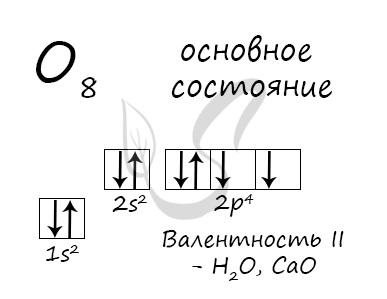
Основное состояние атома кислорода
У атома кислорода (как и атомы азота, фтора, неона) нет возбужденного состояния, так как отсутствует свободная орбиталь с более высоким энергетическим уровнем, куда могли бы перемещаться валентные электроны.
Атом кислорода имеется два неспаренных электрона, максимальная валентность II.
Природные соединения
Получение
В промышленности кислород получают из сжиженного воздуха. Также активно применяются кислородные установки, мембрана которых устроена как фильтр, отсеивающие кислород (мембранная технология).
В лаборатории кислород получают разложением перманганата калия (марганцовки) или бертолетовой соли при нагревании. Применяется реакция каталитического разложения пероксида водорода.
На подводных лодках для получения кислорода применяют следующую реакцию:
Химические свойства
Является самым активным неметаллом после фтора, образует бинарные соединения со всеми элементами кроме гелия, неона, аргона. Чаще всего реакции с кислородом экзотермичны (горение), ускоряются при повышении температуры.
Во всех реакциях, кроме взаимодействия со фтором, кислород проявляет себя в качестве окислителя.
F + O2 → OF2 (фторид кислорода, O +2 )
В реакциях кислорода с металлами образуются оксиды, пероксиды и супероксиды. Реакции с активными металлами идут без нагревания.
Известна реакция горения воды во фторе.
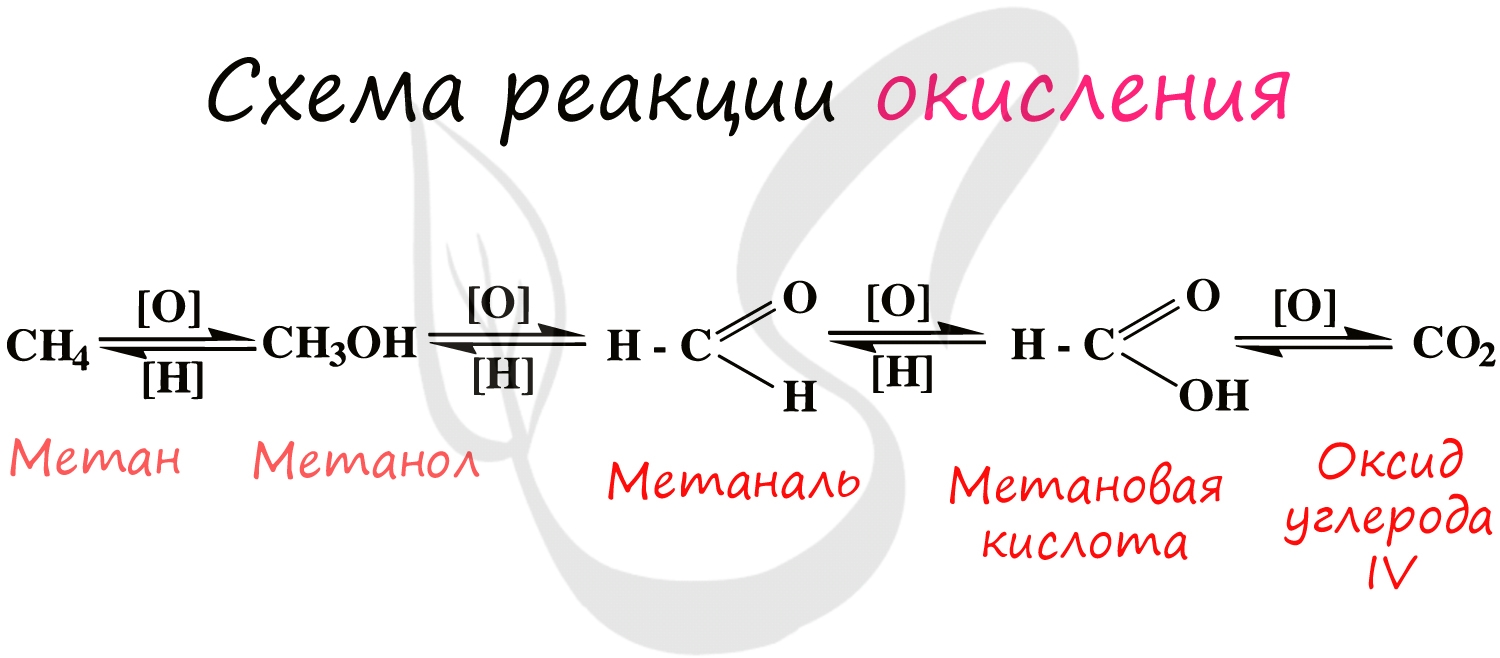
Все органические вещества сгорают с образованием углекислого газа и воды.
Процесс можно остановить на любой стадии в зависимости от желаемого результата.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Урок по химии на тему «Получение кислорода»
Разделы: Химия
– Какую главу изучаем? (Простые вещества.)
– Какие вещества называются простыми? (Вещества, молекулы которых состоят из атомов одного вида.)
– На какие группы делятся простые вещества? (На металлы и неметаллы.)
Изучение нового материала.
Мы продолжаем знакомиться с простыми веществами. Сегодня узнаем больше о веществе, о котором Берцелиус сказал, что вокруг него вращается земная химия. Что это за вещество вы узнаете, выполнив следующее задание. Вместо … вставьте слово, которое соответствует элементу вещества, и запишите слово в тетради. (Приложение 2.)
1. … – самый распространенный элемент земной коры.
2. Молекула простого вещества озона образована элементом …
3. В воздухе содержится 21% …
4. Оксиды – сложные вещества, состоящие из двух элементов, одним из которых является …
5. В состав воды входят два атома водорода и один атом …
– Вы записали одно слово?
– Кто записал несколько слов?
– Какое это слово? (Кислород.)
Итак, начинаем изучать простое вещество кислород!
– Почему изучаем эту тему? Чем важен кислород? (Кислород необходимое вещество для дыхания, самый распространенный элемент земной коры, входит в состав воды.)
– В разделе простые вещества стоит жизненная задача, которая связана с кислородом. Прочитайте ее.
Для путешествия по пещере необходим запас кислорода. Как его можно добыть в походных условиях?
– На основе жизненной задачи скажите, что должны изучать сегодня? (Как получают кислород?)
Тема урока: “Получение кислорода”.
При изучении этой темы:
Для решения той жизненной задачи, которая перед нами стоит, поработайте в группах.
Класс разбит на пять групп по 4 человека. Каждая группа имеет свое задание. (Приложение 1.)
– Внимательно изучите информацию, ответьте на вопросы, запишите уравнения реакций.
Затем представление выполненного задания. Один представитель от группы отвечает устно на вопросы задания, а второй записывает уравнения реакций на доске.
– Будьте внимательны, слушая друг друга. По ходу ваших выступлений будем оформлять схему – получение кислорода.
Используя кислород воздуха для дыхания, уменьшаем его количество. Но содержание в воздухе остается постоянным – 21%. Как же поддерживается необходимое нам постоянное содержание кислорода? Как получается кислород в природе?
Выступление 1 группы о получении кислорода в природе.
Уравнение реакции
Общий вывод: кислород в природе получается благодаря процессу фотосинтеза в растениях на свету.
Оформляется часть схемы
– Подходит ли данный способ для решения жизненной задачи? (Нет, для фотосинтеза необходим свет.)
Кислород необходим не только в природе. В промышленности его используют для получения металлов и других необходимых веществ. Для этого кислород необходим в больших количествах. Способы получения, которые используются при этом, так и называются – промышленные.
Выступление 2 группы о получении кислорода в промышленности.
Уравнение реакции
Общий вывод: кислород в промышленности получают из воздуха и воды.
– Почему для получения больших количеств кислорода используют воздух и воду? (наиболее распространенные вещества в природе, содержащие кислород)
Оформляется часть следующая часть схемы “Получение кислорода”
– Подходит ли данный способ для решения жизненной задачи? (нет, дорогостоящее оборудование, такие процессы занимают много времени)
В Англии на одной из площадей г. Лидса стоит памятник ученому. В правой руке он держит линзу, чтобы собрать пучок солнечных лучей, а в левой – тигель с оксидом ртути. Молодой человек сосредоточен и внимателен, ожидает результаты опыта. Это Джозеф Пристли, англ. ученый, запечатленный в момент получения кислорода в своей лаборатории.
Рассматриваем лабораторные способы получения кислорода.
Выступление 3 группы о некоторых способах получения кислорода в лаборатории.
Все химические реакции разложения.
Вывод: данные способы не подходят для решения жизненной задачи, т.к. соединения ртути ядовито, а калийной селитры может и не оказаться в походных условиях.
– Этими лабораторными способами не ограничивается получение кислорода. Есть еще несколько способов получения кислорода в лаборатории.
Выступление 4 группы о наиболее распространенный способах получения кислорода в лаборатории.
MnO2 – катализатор, ускоряет химическую реакцию, но сам при этом не расходуется.
Все химические реакции разложения.
Общий вывод: в лаборатории кислород получают реакциями разложения кислородсодержащих веществ при нагревании или действии катализатора.
Оформляется оставшаяся часть схемы.
– Оцените данные вещества, условия протекания реакций для использования в походных условиях.
Учащиеся высказывают предположения.
Например, для получения кислорода в походных условиях можно использовать реакцию разложения перманганат калия, который всегда есть в аптечке. Можно использовать также разложение пероксида водорода, для данной реакции применить в качестве катализатора можно кровь, слюну, которые содержат природные катализаторы.
– Получив кислород, необходимо также определенным образом его собрать и доказать наличие.
Выступление 5 группы о способах собирания кислорода и доказательстве его присутствия.
Общий вывод: кислород собирают методом вытеснения воздуха и воды, наличие кислорода доказывают с помощью тлеющей лучинки.
Выполнение лабораторной работы “Получение кислорода разложением перманганата калия и доказательство его наличия” в парах.
Перед работой повторяются правила по технике безопасности при работе со спиртовкой и при нагревании.
– Достигли ли целей урока?
– Как получают кислород?
Вывод по уроку: кислород можно получить в природе, промышленности и лаборатории. Для получения кислорода используют реакции разложения кислородсодержащих веществ. Реакции протекают при нагревании или в присутствии катализатора.
Выберете то задание, которое вам больше нравится.
Расскажите своему другу, который отсутствовал на уроке изучения темы “Получение кислорода”, используя знания о стилях речи, полученные на уроках русского языка.
Подготовить выступление для школьной конференции – Ломоносовские чтения на тему “История открытия кислорода”, используя знания о стилях речи, полученные на уроках русского языка.
Обсуждение выполнения опыта.
Поделитесь своими впечатлениями об уроке. Сформулировать предложение вам поможет рефлексивный экран. Закончите следующие предложения.