Бериллий
(молярная масса)
(первый электрон)
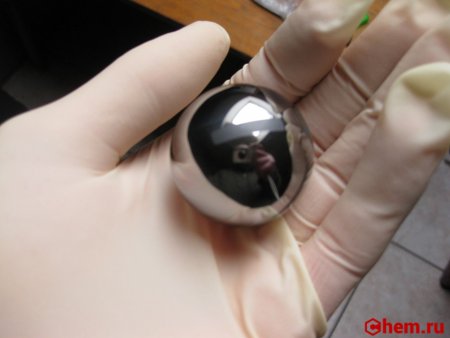
Бериллий (Be, лат. beryllium ) — химический элемент второй группы, второго периода периодической системы с атомным номером 4. Как простое вещество представляет собой относительно твёрдый металл светло-серого цвета, имеет очень высокую стоимость. Высокотоксичен.
Содержание
История
Открыт в 1798 году французским химиком Луи Никола Вокленом, который назвал его глюцинием. Современное название элемент получил по предложению химиков немца Клапрота и шведа Экеберга.
Большую работу по установлению состава соединений бериллия и его минералов провёл русский химик Иван Авдеев. Именно он доказал, что оксид бериллия имеет состав BeO, а не Be2O3, как считалось ранее.
В свободном виде бериллий был выделен в 1828 году французским химиком Антуаном Бюсси и независимо от него немецким химиком Фридрихом Вёлером. Чистый металлический бериллий был получен в 1898 году французским физиком Полем Лебо с помощью электролиза расплавленных солей.
Происхождение названия
Название бериллия произошло от названия минерала берилла (др.-греч. βήρυλλος ) (силикат бериллия и алюминия, Be3Al2Si6O18), которое восходит к названию города Белур (Веллуру) в Южной Индии, недалеко от Мадраса; с древних времён в Индии были известны месторождения изумрудов — разновидности берилла. Из-за сладкого вкуса растворимых в воде соединений бериллия элемент вначале называли «глиций» (др.-греч. γλυκύς — сладкий).
Нахождение в природе
Среднее содержание бериллия в земной коре 3,8 г/т и увеличивается от ультраосновных (0,2 г/т) к кислым (5 г/т) и щелочным (70 г/т) породам. Основная масса бериллия в магматических породах связана с плагиоклазами, где бериллий замещает кремний. Однако наибольшие его концентрации характерны для некоторых тёмноцветных минералов и мусковита (десятки, реже сотни г/т). Если в щелочных породах бериллий почти полностью рассеивается, то при формировании кислых горных пород он может накапливаться в постмагматических продуктах постколлизионных и анорогенных гранитоидов — пегматитах и пневматолито-гидротермальных телах. В кислых пегматитах образование значительных скоплений бериллия связано с процессами альбитизации и мусковитизации. В пегматитах бериллий образует собственные минералы, но часть его (ок. 10 %) находится в изоморфной форме в породообразующих и второстепенных минералах (микроклине, альбите, кварце, слюдах, и др.). В щелочных пегматитах бериллий устанавливается в небольших количествах в составе редких минералов: эвдидимита, чкаловита, анальцима и лейкофана, где он входит в анионную группу. Постмагматические растворы выносят бериллий из магмы в виде фторсодержащих эманаций и комплексных соединений в ассоциации с вольфрамом, оловом, молибденом и литием.
Содержание бериллия в морской воде чрезвычайно низкое — 6⋅10 −7 мг/л.
Известно более 30 собственно бериллиевых минералов, но только 6 из них считаются более-менее распространёнными: берилл, хризоберилл, бертрандит, фенакит, гельвин, даналит. Промышленное значение имеет в основном берилл, в России (Республика Бурятия) разрабатывается фенакит-бертрандитовое Ермаковское месторождение.
Разновидности берилла считаются драгоценными камнями: аквамарин — голубой, зеленовато-голубой, голубовато-зелёный; изумруд — густо-зелёный, ярко-зелёный; гелиодор — жёлтый; известны ряд других разновидностей берилла, различающихся окраской (темно-синие, розовые, красные, бледно-голубые, бесцветные и др.). Цвет бериллу придают примеси различных элементов.
Месторождения
Месторождения минералов бериллия присутствуют на территории Бразилии, Аргентины, Африки, Индии, Казахстана, России (Ермаковское месторождение в Бурятии, Малышевское месторождение в Свердловской области, пегматиты восточной и юго-восточной части Мурманской области) и др.
Физические свойства
Химические свойства
Для бериллия характерны две степени окисления +1 и +2. Гидроксид бериллия (II) амфотерен, причём как основные (с образованием Be 2+ ), так и кислотные (с образованием [Be(OH)4] 2− ) свойства выражены слабо. Степень окисления +1 у бериллия была получена при исследовании процессов испарения бериллия в вакууме в тиглях из оксида бериллия BeO с образованием летучего оксида Be2O в результате сопропорционирования BeO + Be = Be2O.
По многим химическим свойствам бериллий больше похож на алюминий, чем на находящийся непосредственно под ним в таблице Менделеева магний (проявление «диагонального сходства»).
Металлический бериллий относительно мало реакционноспособен при комнатной температуре. В компактном виде он не реагирует с водой и водяным паром даже при температуре красного каления и не окисляется воздухом до 600 °C. Порошок бериллия при поджигании горит ярким пламенем, при этом образуются оксид и нитрид. Галогены реагируют с бериллием при температуре выше 600 °C, а халькогены требуют ещё более высокой температуры. Аммиак взаимодействует с бериллием при температуре выше 1200 °C с образованием нитрида Be3N2, а углерод даёт карбид Ве2С при 1700 °C. С водородом бериллий непосредственно не реагирует.
Бериллий легко растворяется в разбавленных водных растворах кислот (соляной, серной, азотной), однако холодная концентрированная азотная кислота пассивирует металл. Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов:
При проведении реакции с расплавом щелочи при 400—500 °C образуются бериллаты:
Изотопы бериллия
Происхождение бериллия
В процессах как первичного, так и звёздного нуклеосинтеза рождаются лишь лёгкие нестабильные изотопы бериллия. Стабильный изотоп 9 Be может появиться как в звёздах, так и в межзвёздной среде в результате распада более тяжелых ядер, бомбардируемых космическими лучами.
Получение
В виде простого вещества в XIX веке бериллий получали действием калия на безводный хлорид бериллия:
BeCl2 + 2K ⟶ Be + 2KCl
В настоящее время бериллий получают, восстанавливая фторид бериллия магнием:
Производство и применение
По состоянию на 2000 год основными производителями бериллия являлись: США (с большим отрывом), а также Китай, Казахстан. В 2014 году произвела первый образец бериллия и Россия. В России планируется строительство нового комбината по производству бериллия к 2019 году На долю остальных стран приходилось менее 1 % мировой добычи. Всего в мире производится 300 тонн бериллия в год (2016 год).
Легирование сплавов
Бериллий в основном используют как легирующую добавку к различным сплавам. Добавка бериллия значительно повышает твёрдость и прочность сплавов, коррозионную устойчивость поверхностей, изготовленных из этих сплавов изделий. В технике довольно широко распространены бериллиевые бронзы типа BeB (пружинные контакты). Добавка 0,5 % бериллия в сталь позволяет изготовить пружины, которые остаются упругими до температуры красного каления. Эти пружины способны выдерживать миллиарды циклов значительной по величине нагрузки. Кроме того, бериллиевая бронза не искрится при ударе о камень или металл. Один из сплавов носит собственное название рандоль. Благодаря его сходству с золотом рандоль называют «цыганским золотом».
Рентгенотехника
Бериллий слабо поглощает рентгеновское излучение, поэтому из него изготавливают окошки рентгеновских трубок (через которые излучение выходит наружу) и окошки рентгеновских и широкодиапазонных гамма-детекторов, через которые излучение проникает в детектор.
Ядерная энергетика
Оксид бериллия наряду с металлическим бериллием служит в атомной технике как более эффективный замедлитель и отражатель нейтронов, чем чистый бериллий. Кроме того, оксид бериллия в смеси с окисью урана применяется в качестве очень эффективного ядерного топлива. Фторид бериллия в сплаве с фторидом лития применяется в качестве теплоносителя и растворителя солей урана, плутония, тория в высокотемпературных жидкосолевых атомных реакторах.
Фторид бериллия используется в атомной технике для варки стекла, применяемого для регулирования небольших потоков нейтронов. Самый технологичный и качественный состав такого стекла − (BeF2 — 60 %, PuF4 — 4 %,AlF3 — 10 %, MgF2 — 10 %, CaF2 — 16 %). Этот состав наглядно показывает один из примеров применения соединений плутония в качестве конструкционного материала (частичное).
Лазерные материалы
В лазерной технике находит применение алюминат бериллия для изготовления твердотельных излучателей (стержней, пластин).
Аэрокосмическая техника
В производстве тепловых экранов и систем наведения с бериллием не может конкурировать практически ни один конструкционный материал. Конструкционные материалы на основе бериллия обладают одновременно и лёгкостью, и прочностью, и стойкостью к высоким температурам. Будучи в 1,5 раза легче алюминия, эти сплавы в то же время прочнее многих специальных сталей. Налажено производство бериллидов, применяемых как конструкционные материалы для двигателей и обшивки ракет и самолётов, а также в атомной технике.
Ракетное топливо
Стоит отметить высокую токсичность и высокую стоимость металлического бериллия, и в связи с этим приложены значительные усилия для выявления бериллийсодержащих топлив, имеющих значительно меньшую общую токсичность и стоимость. Одним из таких соединений бериллия является гидрид бериллия.
Огнеупорные материалы
Оксид бериллия является наиболее теплопроводным из всех оксидов, его теплопроводность при комнатной температуре выше, чем у большинства металлов и почти всех неметаллов (кроме алмаза и карбида кремния). Он служит высокотеплопроводным высокотемпературным изолятором и огнеупорным материалом для лабораторных тиглей и в других специальных случаях.
Акустика
Ввиду своей легкости и высокой твёрдости бериллий успешно применяется в качестве материала для электродинамических громкоговорителей. Однако, его высокая стоимость, трудность обработки (из-за хрупкости) и токсичность (при несоблюдении технологии обработки) делают возможным применение динамиков с бериллием только в дорогих профессиональных аудиосистемах. Из-за высокой эффективности бериллия в акустике некоторые производители в целях улучшения продаж заявляют о применении бериллия в своих продуктах, в то время как это не так.
Большой Адронный Коллайдер
В точках столкновения пучков на Большом Адронном Коллайдере (БАК) вакуумная труба сделана из бериллия. Он одновременно практически не взаимодействует с частицами, произведенными в столкновениях (которые регистрируют детекторы), но при этом достаточно прочен.
Биологическая роль и физиологическое действие
В живых организмах бериллий не несёт какой-либо значимой биологической функции. Однако бериллий может замещать магний в некоторых ферментах, что приводит к нарушению их работы. Ежедневное поступление бериллия в организм человека с пищей составляет около 0,01 мг.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs |
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu,
Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2,
W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, Au
Бериллий: способы получения и химические свойства
Бериллий Be — это cветло-серый, легкий, хрупкий металл. На воздухе покрывается оксидной пленкой. Восстановитель.
Относительная молекулярная масса Mr = 9,012; относительная плотность для твердого и жидкого состояния d = 1,85; tпл = 1287º C; tкип = 2507º C.
Способ получения
1. В результате электролиза расплава хлорида бериллия образуются бериллий и хлор :
3. Оксид бериллия легко восстанавливается магнием при 700 — 800º С, образуя бериллий и оксид магния:
BeO + Mg = MgO + Be
4. Фторид бериллия также легко восстанавливается магнием при 700 — 750º С с образованием бериллия и фторида магния:
BeF2 + Mg = Be + MgF2
Качественная реакция
Качественная реакция на бериллий — окрашивание пламени горелки в коричнево — красный цвет.
Химические свойства
1.1. Бериллий взаимодействует с азотом при 700 — 900º С образуя нитрид бериллия:
1.2. Бериллий сгорает в кислороде (воздухе) при 900º С с образованием оксида бериллия:
2Be + O2 = 2BeO
Be + Br2 = BeBr2
1.4. С серой бериллий реагирует при температуре 1150º C с образованием сульфида бериллия:
Be + S = BeS
1.5. С углеродом бериллий реагирует при 1700 — 1900º С и вакууме, образуя карбид бериллия:
2Be + C = Be2C
2. Бериллий активно взаимодействует со сложными веществами:
2.2. Бериллий взаимодействует с кислотами:
2.2.1. Бериллий реагирует с разбавленной соляной кислотой, при этом образуются хлорид бериллия и водород :
Be + 2HCl = BeCl2 + H2 ↑
2.2.2. Реагируя с разбавленной и горячей азотной кислотой бериллий образует нитрат бериллия, газ оксид азота (II) и воду:
2.2.3. В результате реакции концентрированной фтороводородной кислоты и бериллия образуется осадок тетрафторобериллат водорода и газ водород:
2.3. Бериллий может взаимодействовать с основаниями:
2.3.1. Бериллий взаимодействует с гидроксидом натрия в расплаве при температуре 400 — 500º С, при этом образуется бериллат натрия и водород:
2.4. Бериллий вступает в реакцию с газом аммиаком при 500 — 700º С. В результате данной реакции образуется нитрид бериллия и водород:
2.5. Бериллий может вступать в реакцию с оксидами :
В результате взаимодействия бериллия и оксида магния при температуре 1075º С образуется оксид бериллия и магний:
Be + MgO = BeO + Mg
3. Бериллий взаимодействует с органическими веществами :
Бериллий может вступать в реакцию с ацетиленом при 400 — 450º С, образуя карбид бериллия и водород:
Бериллий
Бериллий / Beryllium (Be), 4
Содержание
История
Открыт в 1798 г. французским химиком Луи Никола Вокленом. Большую работу по установлению состава соединений бериллия и его минералов провёл русский химик И. В. Авдеев (1818—1865). Именно он доказал, что оксид бериллия имеет состав BeO, а не Be2O3, как считалось ранее.
Происхождение названия
Название бериллия произошло от названия минерала берилла (др.-греч. βήρυλλος beryllos) (силикат бериллия и алюминия, Be3Al2Si6O18), которое восходит к названию города Белур (Веллуру) в Южной Индии, недалеко от Мадраса; с древних времён в Индии были известны месторождения изумрудов — разновидности берилла. Из-за сладкого вкуса растворимых в воде соединений бериллия элемент вначале называли «глюциний» (др.-греч. γλυκύς glykys — сладкий).
Нахождение в природе
Изотоп 8 Be отсутствует в природе, поскольку является крайне нестабильным и имеет период полураспада 10 −18 с. [3] Стабильным является 9 Be. Кроме 9 Be в природе встречаются радиоактивные изотопы 7 Be и 10 Be.
Содержание бериллия в морской воде чрезвычайно низкое — 6·10 −7 мг/л. [4]
Известно более 30 собственно бериллиевых минералов, но только 6 из них считаются более-менее распространёнными: берилл, хризоберилл, бертрандит, фенакит, гельвин, даналит. Промышленное значение имеет в основном берилл, в России (Республика Бурятия) разрабатывается фенакит-бертрандитовое Ермаковское месторождение.
Разновидности берилла считаются драгоценными камнями: аквамарин — голубой, зеленовато-голубой, голубовато-зеленый; изумруд — густо-зеленый, ярко-зеленый; гелиодор — желтый; известны ряд других разновидностей берилла, различающихся окраской (темно-синие, розовые, красные, бледно-голубые, бесцветные и др.). Цвет бериллу придают примеси различных элементов.
Месторождения
Месторождения минералов бериллия присутствуют на территории Бразилии, Аргентины, Африки, Индии, России (Бурятия, Сибирь) и др. [5]
Физические свойства
Бериллий — относительно твердый, но хрупкий металл серебристо-белого цвета. Имеет высокий модуль упругости — 300 ГПа (у сталей — 200—210 ГПа). На воздухе активно покрывается стойкой оксидной плёнкой BeO.
Химические свойства
Для бериллия характерна только одна степень окисления +2. Соответствующий гидроксид амфотерен, причем как основные (с образованием Be 2+ ), так и кислотные (с образованием [Be(OH)4] 2- ] свойства выражены слабо.
По многим химическим свойствам бериллий больше похож на алюминий, чем на находящийся непосредственно под ним магний (проявление «диагонального сходства»).
Металлический бериллий относительно мало реакционноспособен при комнатной температуре. В компактном виде он не реагирует с водой и водяным паром даже при температуре красного каления и не окисляется воздухом до 600 °C. Порошок бериллия при поджигании горит ярким пламенем, при этом образуются оксид и нитрид. Галогены реагируют с бериллием при температуре выше 600 °C, а халькогены требуют еще более высокой температуры. Аммиак взаимодействует с бериллием при температуре выше 1200 °C с образованием нитрида Be3N2, а углерод дает карбид Ве2С при 1700 °C. С водородом бериллий непосредственно не реагирует.
Бериллий легко растворяется в разбавленных водных растворах кислот (соляной, серной, азотной), однако холодная концентрированная азотная кислота пассивирует металл. Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов:
При проведении реакции с расплавом щелочи при 400—500 °C образуются диоксобериллаты:
Получение
В виде простого вещества в XIX веке бериллий получали действием калия на безводный хлорид бериллия:
В настоящее время бериллий получают, восстанавливая его фторид магнием:

либо электролизом расплава смеси хлоридов бериллия и натрия. Исходные соли бериллия выделяют при переработке бериллиевой руды.
Применение
Легирование сплавов
Бериллий в основном используют как легирующую добавку к различным сплавам. Добавка бериллия значительно повышает твёрдость и прочность сплавов, коррозионную устойчивость поверхностей изготовленных из этих сплавов изделий. В технике довольно широко распространены бериллиевые бронзы типа BeB (пружинные контакты). Добавка 0,5 % бериллия в сталь позволяет изготовить пружины, которые пружинят при красном калении.
Рентгенотехника
Бериллий слабо поглощает рентгеновское излучение, поэтому из него изготавливают окошки рентгеновских трубок (через которые излучение выходит наружу).
Ядерная энергетика
Лазерные материалы
В лазерной технике находит применение алюминат бериллия для изготовления твердотельных излучателей (стержней, пластин).
Аэрокосмическая техника
В производстве тормозов для аэрокосмической техники, тепловых экранов и систем наведения с бериллием не может конкурировать практически ни один конструкционный материал. Конструкционные материалы на основе бериллия обладают одновременно и лёгкостью, и прочностью, и стойкостью к высоким температурам. Будучи в 1,5 раза легче алюминия, эти сплавы в то же время прочнее многих специальных сталей. Налажено производство бериллидов применяемых как конструкционные материалы для двигателей и обшивки ракет и самолетов, а также в атомной технике.
Ракетное топливо
Стоит отметить высокую токсичность и высокую стоимость металлического бериллия, и в этой связи приложены значительные усилия для выявления бериллийсодержащих топлив имеющих значительно меньшую общую токсичность и стоимость. Одним из таких соединений бериллия является гидрид бериллия.
Огнеупорные материалы
Оксид бериллия применяется в качестве очень важного огнеупорного материала в специальных случаях. Считается одним из лучших огнеупорных материалов.
Биологическая роль и физиологическое действие
В живых организмах бериллий не несёт какой-либо значимой биологической функции. Однако бериллий может замещать магний в некоторых ферментах, что приводит к нарушению их работы. Ежедневное поступление бериллия в организм человека с пищей составляет около 0,01 мг.
Бериллий ядовит: Летучие (и растворимые) соединения бериллия, в том числе и пыль, содержащая соединения бериллия, высокотоксичны. Для воздуха ПДК в пересчёте на бериллий составляет 0,001 мг/м³. Бериллий обладает ярко выраженным аллергическим и канцерогенным действием. Вдыхание атмосферного воздуха, содержащего бериллий, приводит к тяжёлому заболеванию органов дыхания — бериллиозу.