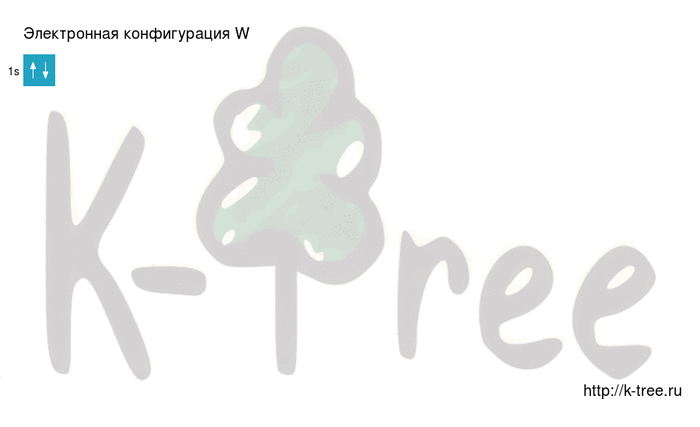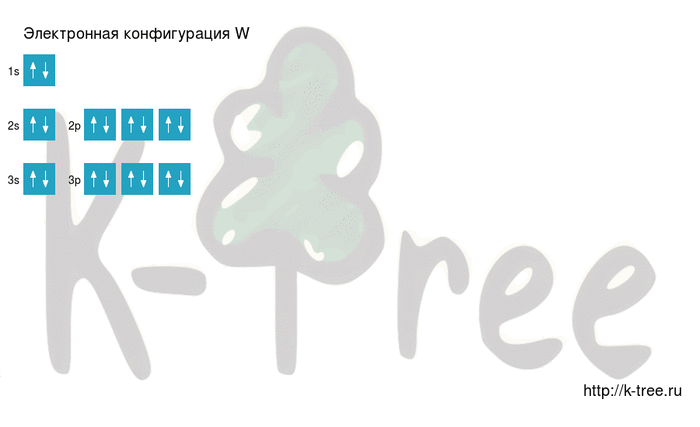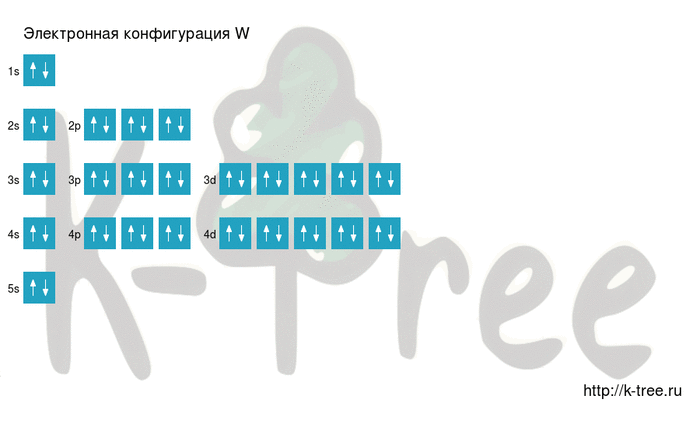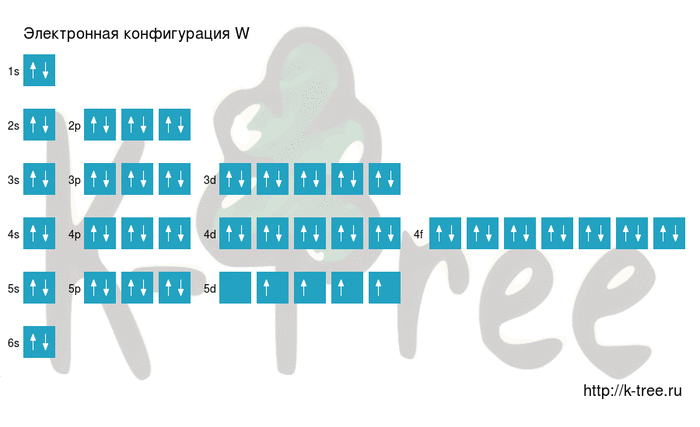Вольфрам W
Вольфрам в таблице менделеева занимает 74 место, в 6 периоде.
| Символ | W |
| Номер | 74 |
| Атомный вес | 183.8400000 |
| Латинское название | Wolframium |
| Русское название | Вольфрам |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема вольфрама
W: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 4
Короткая запись:
W: [Xe]6s 2 4f 14 5d 4
Порядок заполнения оболочек атома вольфрама (W) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Вольфрам имеет 74 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
4 электрона на 5d-подуровне
Степень окисления вольфрама
Ионы вольфрама
Валентность W
Атомы вольфрама в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность вольфрама характеризует способность атома W к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа W
Квантовые числа определяются последним электроном в конфигурации, для атома W эти числа имеют значение N = 5, L = 2, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Вольфрам W
Вольфрам в таблице менделеева занимает 74 место, в 6 периоде.
| Символ | W |
| Номер | 74 |
| Атомный вес | 183.8400000 |
| Латинское название | Wolframium |
| Русское название | Вольфрам |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема вольфрама
W: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 4
Короткая запись:
W: [Xe]6s 2 4f 14 5d 4
Порядок заполнения оболочек атома вольфрама (W) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Вольфрам имеет 74 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
4 электрона на 5d-подуровне
Степень окисления вольфрама
Ионы вольфрама
Валентность W
Атомы вольфрама в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность вольфрама характеризует способность атома W к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа W
Квантовые числа определяются последним электроном в конфигурации, для атома W эти числа имеют значение N = 5, L = 2, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Вольфрам W
Вольфрам в таблице менделеева занимает 74 место, в 6 периоде.
| Символ | W |
| Номер | 74 |
| Атомный вес | 183.8400000 |
| Латинское название | Wolframium |
| Русское название | Вольфрам |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема вольфрама
W: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 4
Короткая запись:
W: [Xe]6s 2 4f 14 5d 4
Порядок заполнения оболочек атома вольфрама (W) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Вольфрам имеет 74 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
4 электрона на 5d-подуровне
Степень окисления вольфрама
Ионы вольфрама
Валентность W
Атомы вольфрама в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность вольфрама характеризует способность атома W к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа W
Квантовые числа определяются последним электроном в конфигурации, для атома W эти числа имеют значение N = 5, L = 2, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Вольфрам, свойства атома, химические и физические свойства
Вольфрам, свойства атома, химические и физические свойства.
183,84(1) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 4 6s 2
Вольфрам — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 74. Расположен в 6-й группе (по старой классификации — побочной подгруппе шестой группы), шестом периоде периодической системы.
Физические свойства вольфрама
Атом и молекула вольфрама. Формула вольфрама. Строение вольфрама:
Вольфрам – металл. Относится к группе переходных металлов. Вольфрам — самый тугоплавкий из металлов.
Вольфрам обозначается символом W.
Как простое вещество вольфрам при нормальных условиях представляет собой твёрдый, блестящий, серебристо-серый металл.
Молекула вольфрама одноатомна.
Химическая формула вольфрама W.
Строение атома вольфрама. Атом вольфрама состоит из положительно заряженного ядра (+74), вокруг которого по шести оболочкам движутся 74 электрона. При этом 72 электрона находятся на внутреннем уровне, а 2 электрона – на внешнем. Поскольку вольфрам расположен в шестом периоде, оболочек всего шесть. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья и пятая – внутренние оболочки представлены s-, р- и d-орбиталями. Четвертая – внутренняя оболочка представлена s-, р-, d- и f-орбиталями. Шестая – внешняя оболочка представлена s-орбиталью. На внутреннем энергетическом уровне атома вольфрама на 5d-орбитали находятся четыре неспаренных электрона. На внешнем энергетическом уровне атома вольфрама – на s-орбитали находятся два спаренных электрона. В свою очередь ядро атома вольфрама состоит из 74 протонов и 110 нейтронов. Вольфрам относится к элементам d-семейства.
Радиус атома вольфрама (вычисленный) составляет 193 пм.
Атомная масса атома вольфрама составляет 183,84(1) а. е. м.
При стандартных условиях вольфрам химически стоек.
Изотопы и модификации вольфрама:
Свойства вольфрама (таблица): температура, плотность, давление и пр.:
| 100 | Общие сведения | |
| 101 | Название | Вольфрам |
| 102 | Прежнее название | |
| 103 | Латинское название | Wolframium |
| 104 | Английское название | Tungsten |
| 105 | Символ | W |
| 106 | Атомный номер (номер в таблице) | 74 |
| 107 | Тип | Металл |
| 108 | Группа | Переходный металл |
| 109 | Открыт | Карл Вильгельм Шееле, Швеция, 1781 г. (назван), Хуан Хосе Эльхуяр Любизе и Фаусто де Эльхуяр, Испания, 1783 г. |
| 110 | Год открытия | 1783 г. |
| 111 | Внешний вид и пр. | Твёрдый, тугоплавкий, блестящий серебристо-серый металл |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | 2 аллотропные модификации: – α-вольфрам с кубической объёмно-центрированной кристаллической решёткой, |
| 204 | Радиус атома (вычисленный) | 193 пм |
| 205 | Эмпирический радиус атома* | 135 пм |
| 206 | Ковалентный радиус* | 162 пм |
| 207 | Радиус иона (кристаллический) | W 4+ W 6+ + 6e – → W, E o = +0,68 В |
| 306 | Энергия сродства атома к электрону | 78,76(1) кДж/моль (0,81626(8) эВ) |
| 400 | Физические свойства | |
| 401 | Плотность* | 19,3 г/см 3 (при 20 °C и иных стандартных условиях , состояние вещества – твердое тело), 17,6 г/см 3 (при температуре плавления 3422 °C и иных стандартных условиях , состояние вещества – жидкость) |
| 402 | Температура плавления* | 3422 °C (3695 K, 6192 °F) |
| 403 | Температура кипения* | 5930 °C (6203 K, 10706 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 52,31 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 774 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | 0,114 Дж/г·K (при 0-1000 °C) |
| 410 | Молярная теплоёмкость | 24,27 Дж/(K·моль) |
| 411 | Молярный объём | 9,55 см³/моль |
| 412 | Теплопроводность | 173 Вт/(м·К) (при стандартных условиях ), 162,8 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | α-вольфрам |
| 512 | Структура решётки | Кубическая объёмно-центрированная |
| 513 | Параметры решётки | 3,160 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 310 K |
| 516 | Название пространственной группы симметрии | Im_ 3m |
| 517 | Номер пространственной группы симметрии | 229 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-33-7 |
205* Эмпирический радиус вольфрама согласно [1] и [3] составляет 139 пм и 137 пм соответственно.
206* Ковалентный радиус вольфрама согласно [1] и [3] составляет 162±7 пм и 170 пм соответственно.
401* Плотность вольфрама согласно [3] и [4] составляет 19,25 г/см 3 (при 0 °C и иных стандартных условиях , состояние вещества – твердое тело) и 19,32 г/см 3 (при 20 °C и иных стандартных условиях , состояние вещества – твердое тело) соответственно.
402* Температура плавления вольфрама согласно [4] составляет 3420 °C (3693,15 K, 6188 °F).
403* Температура кипения вольфрама согласно [3] и [4] составляет 5555 °C (5828 K, 10031 °F) и 5680 °C (5953,15 K, 10256 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) вольфрама согласно [4] составляет 61,5 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) вольфрама согласно [3] и [4] составляет 824 кДж/моль и 769 кДж/моль соответственно.
Вольфрам W
Вольфрам в таблице менделеева занимает 74 место, в 6 периоде.
| Символ | W |
| Номер | 74 |
| Атомный вес | 183.8400000 |
| Латинское название | Wolframium |
| Русское название | Вольфрам |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема вольфрама
W: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 4
Короткая запись:
W: [Xe]6s 2 4f 14 5d 4
Порядок заполнения оболочек атома вольфрама (W) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Вольфрам имеет 74 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
4 электрона на 5d-подуровне
Степень окисления вольфрама
Ионы вольфрама
Валентность W
Атомы вольфрама в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность вольфрама характеризует способность атома W к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа W
Квантовые числа определяются последним электроном в конфигурации, для атома W эти числа имеют значение N = 5, L = 2, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева