Ртуть
Ртуть (лат. hydrargyrum ) — химический элемент II группы дополнительной подгруппы периодической системы элементов Менделева с атомным номером 80 и атомной массой 200,59, обозначается символом Hg. Простое вещество при комнатной температуре представляет собой тяжёлую серебристо-белую заметно летучую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии. В природе находится как в самородном виде, так и образует ряд минералов. Чаще всего ртуть получают путём восстановления из её наиболее распространённого минерала — киновари. Применятся для изготовления измерительных приборов, вакуумных насосов, источников света и в других областях науки и техники.
| Ртуть / Hydrargyrum (Hg) | |
|---|---|
| Атомный номер | 80 |
| Внешний вид | тяжёлая жидкость серебристо-белого цвета |
| Свойства атома | |
| Атомная масса (молярная масса) | 200,59 а. е. м. (г/моль) |
| Радиус атома | 157 пм |
| Энергия ионизации (первый электрон) | 1 006,0 (10,43) кДж/моль (эВ) |
| Электронная конфигурация | [Xe] 4f 14 5d 10 6s 2 |
| Химические свойства | |
| Ковалентный радиус | 149 пм |
| Радиус иона | (+2e) 110 (+1e) 127 пм |
| Электроотрицательность (по Полингу) | 2,00 |
| Электродный потенциал | Hg←Hg 2+ 0,854 В |
| Степени окисления | 2, 1 |
| Термодинамические свойства | |
| Плотность | 13,546 (@ +20 °C) г/см³ |
| Удельная теплоёмкость | 0,138 Дж/(K·моль) |
| Теплопроводность | 8,3 Вт/(м·K) |
| Температура плавления | 234,28 K |
| Теплота плавления | 2,295 кДж/моль |
| Температура кипения | 629,73 K |
| Теплота испарения | 58,5 кДж/моль |
| Молярный объём | 14,8 см³/моль |
| Кристаллическая решётка | |
| Структура решётки | ромбоэдрическая |
| Период решётки | 2,990 Å |
| Отношение c/a | n/a |
| Температура Дебая | 100,00 K |
Содержание
История
Происхождение названия
Русское название ртути, по одной из версий, — это заимствование из арабского (через тюркские языки); по другой версии, «ртуть» связана с литовским ritu — качу, катаю, происшедшим от индоевропейского рет (х) — бежать, катиться. Литва и Русь были тесно связаны, а во 2-й половине XIV века русский язык был языком делопроизводства Великого Княжества Литовского, а также языком первых письменных памятников Литвы.
Латинское hydrargirum произошло от греческих слов hýdor — вода и árgyros — серебро. «Жидким» (или живым, быстрым) серебром ртуть называется также в немецком (Quecksilber) и в староанглийском (quicksilver) языках, а по-болгарски ртуть — живак: действительно, шарики ртути блестят, как серебро, и очень быстро «бегают» — как живые.
Соединения ртути
Ртуть и её соединения применяются в технике, химической промышленности, медицине. Жёлтый оксид ртути(II) входит в состав глазной мази и мазей для лечения кожных заболеваний. Красный оксид ртути(II) применяется для получения красок. Хлорид ртути(I), который называется каломель, используется в пиротехнике, а также в качестве фунгицида. В ряде стран каломель используется в качестве слабительного. Токсическое действие каломели проявляется особенно тогда, когда после приема её внутрь не наступает слабительное действие и организм долгое время не освобождается от этого препарата.
Хлорид ртути(II), который называется сулема, является очень токсичным. Сулема применялась в медицине как дезинфицирующее средство, в технике она используется для обработки дерева, получения некоторых видов чернил, травления и чернения стали. В сельском хозяйстве сулема применяется как фунгицид.
Амидохлорид ртути (белый преципитат ртути) входит в состав некоторых мазей. В ветеринарии амидохлорид ртути применяется как средство против паразитарных заболеваний кожи.
Нитрат ртути(II) применяется для отделки меха и получения других соединений этого металла. Токсичность нитрата ртути(II) примерно такая же, как и токсичность сулемы. Многие органические соединения ртути используются в качестве пестицидов и средств для обработки семян. Отдельные органические соединения ртути применяются как диуретические средства.
Получение
В России известны 23 месторождения ртути, промышленные запасы составляют 15,6 тыс.тонн (на 2002 год).
Физические свойства
Ртуть — единственный металл, жидкий при комнатной температуре. Ртуть не обладает магнитными свойствами.
Химические свойства
Ртуть — малоактивный металл (см. ряд напряжений ).
Применение
Сплав ртути с таллием используется для низкотемпературных термометров.
Ртуть используется для переработки вторичного алюминия и добычи золота (см. Амальгамная металлургия ).
Ртуть входит в состав некоторых биоцидных красок для предотвращения обрастания корпуса судов в морской воде.
Также используются и соли ртути:
Биологическая роль
Ртуть
Ртуть / Hydrargyrum (Hg), 80
[Xe] 4f 14 5d 10 6s 2
Ртуть — элемент побочной подгруппы второй группы шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80. Обозначается символом Hg (лат. Hydrargyrum ). Простое вещество ртуть (CAS-номер: 7439-97-6) — переходный металл, при комнатной температуре представляет собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй элемент — бром).
Содержание
История
Ртуть известна с древних времен. Нередко ее находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и ее соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твердость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 г. Для представления элемента как у алхимиков, так и в нынешнее время используется символ планеты Меркурий.
Происхождение названия
Нахождение в природе
Ртуть — относительно редкий элемент в Земной коре со средней концентрацией 83 мг/т. Однако в виду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7. В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся прежде всего самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg4Cl.
Месторождения
Ртуть считается редким металлом.
Известны месторождения ртути в Закавказье (Дагестан, Армения), Таджикистане, Словении, Киргизии, Украине (Горловка, Никитовский ртутный комбинат).
В окружающей среде
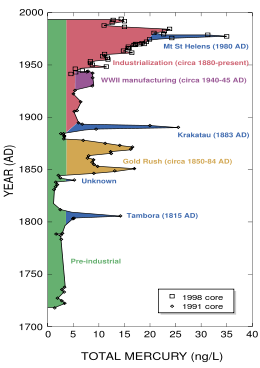
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограмма на литр льда. Природные источники, такие как вулканы, составляют примерно половину всех выбросов атмосферной ртути. За оставшуюся половину ответственна деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля главным образом в тепловых электростанциях — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Изотопы ртути
| Изотоп | 196 | 198 | 199 | 200 | 201 | 202 | 204 |
|---|---|---|---|---|---|---|---|
| Концентрация, (%) | 0,146 | 10,02 | 16,84 | 23,13 | 13,22 | 29,80 | 6,85 |
Получение
Ртуть получают обжигом киновари (cульфида ртути(II)): Уравнение реакции:
Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
В России известны 23 месторождения ртути, промышленные запасы составляют 15,6 тыс. тонн (на 2002 год).
Физические свойства
| Температура в °С | ρ, 10 3 кг/м 3 | Температура в °С | ρ, 10 3 кг/м 3 |
| 0 | 13,5951 | 50 | 13,4723 |
| 5 | 13,5827 | 55 | 13,4601 |
| 10 | 13,5704 | 60 | 13,4480 |
| 15 | 13,5580 | 65 | 13,4358 |
| 20 | 13,5457 | 70 | 13,4237 |
| 25 | 13,5335 | 75 | 13,4116 |
| 30 | 13,5212 | 80 | 13,3995 |
| 35 | 13,5090 | 90 | 13,3753 |
| 40 | 13,4967 | 100 | 13,3514 |
| 45 | 13,4845 | 300 | 12,875 |
Химические свойства
Характерные степени окисления
| Степень окисления | Оксид | Гидроксид | Характер | Примечания |
|---|---|---|---|---|
| +1 | Не получен | * | Слабоосновный | Склонность к диспропорционированию |
| +2 | HgO | ** | Очень слабое основание, иногда — амфотерный |
‘*Гидроксид не получен, существуют только соответствующие соли
‘**Гидроксид существует только в очень разбавленных ( −4 моль/л) растворах.
Для ртути характерны две степени окисления: +1 и +2. В степени окисления +1 ртуть представляет собой двухъядерный катион Hg2 2+ со связью металл-металл. Ртуть — один из немногих металлов, способных формировать такие катионы, и у ртути они — самые устойчивые.
В степени окисления +1 ртуть склонна к диспропорционированию. Оно протекает при нагревании:
добавлении лигандов, стабилизирующих степень окисления ртути +2.
Из-за диспропорционирования ни оксид, ни гидроксид ртути (I) получить не удаётся.
На холоду ртуть +2 и металлическая ртуть, наоборот, конпропорционируют. Поэтому, в частности, при реакции нитрата ртути (II) со ртутью получается нитрат ртути (I):
В очень концентрированной щелочи оксид ртути частично растворяется с образованием гидроксокомплекса:
Ртуть в степени окисления +2 образует уникально прочные комплексы со многими лигандами, причём как жесткими, так и мягкими по теории ЖМКО. С иодом (-1), серой (-2) и углеродом она образует очень прочные ковалентные связи. По устойчивости связей металл-углерод ртути нет равных среди других металлов, поэтому получено огромное количество ртутьорганических соединений.
Свойства простого вещества [8]
Ртуть — малоактивный металл (см. ряд напряжений). Она не растворяется в растворах кислот, не обладающих окислительными свойствами, но растворяется в царской водке:
Также с трудом растворяется в серной кислоте при нагревании, с образованием сульфата ртути:
При растворении избытка ртути в азотной кислоте на холоде образуется нитрат Hg2(NO3)2.
При нагревании до 300 °C ртуть вступает в реакцию с кислородом:
При этом образуется оксид ртути(II) красного цвета. Эта реакция обратима: при нагревании выше 340 °C оксид разлагается до простых веществ.

Реакция разложения оксида ртути исторически является одним из первых способов получения кислорода.
При нагревании ртути с серой образуется сульфид ртути(II):
Ртуть также реагирует с галогенами (причём на холоду — медленно).
Ртуть можно окислить также щелочным раствором перманганата калия:
и различными хлорсодержащими отбеливателями. Эти реакции используют для удаления металлической ртути.
Применение
Применение ртути и её соединений
Медицина
Амальгаму серебра применяют в стоматологии в качестве материала зубных пломб.
Ртуть-203 (T1/2 = 53 сек) используется в радиофармакологии.
Техника
Металлургия
Химическая промышленность
Сельское хозяйство
Высокотоксичные соединения ртути, такие как хлорид ртути(I) (каломель), хлорид ртути (II) (сулема), мертиолят и другие используют для протравливания семенного зерна и в качестве пестицидов.
Токсикология ртути
Ядовиты только пары́ и растворимые соединения ртути. Металлическая ртуть не оказывает существенного воздействия на организм. Пары могут вызвать тяжёлое отравление. Ртуть и её соединения (сулема, каломель, цианид ртути) поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании — дыхательные пути (а проникновение ртути в организм чаще происходит именно при вдыхании её паров, не имеющих запаха). По классу опасности ртуть относится к первому классу (чрезвычайно опасное химическое вещество). Опасный загрязнитель окружающей среды, особенно опасны выбросы в воду, поскольку в результате деятельности населяющих дно микроорганизмов происходит образование растворимой в воде и токсичной метилртути. Ртуть — типичный представитель кумулятивных ядов.
Гигиеническое нормирование концентраций ртути
Демеркуризация
Очистка помещений и предметов от загрязнений металлической ртутью и источников ртутных паров называется демеркуризацией. В быту широко применяется демеркуризация с помощью серы. Так, например, если разбился градусник, раньше предлагали тщательно собрать все шарики ртути медицинской клизмой в стеклянную банку с герметичной крышкой, а щели и неровности засыпать порошком серы (S). Сера вступает в химическую реакцию со ртутью при комнатной температуре, образуя нерастворимое и потому не ядовитое твердое вещество — сульфид ртути. Однако этот метод исключительно малоэффективен. Сера со ртутью легко реагирует только при тщательном растирании в ступке. Если насыпать на тяжелую ртуть легкий порошок серы, реакция практически не будет идти. Или пойдет чрезвычайно медленно. На самом деле следует тщательнейшим образом собрать все видимые (при ярком свете лампы!) капельки ртути в герметично закрывающуюся емкость. Для сбора крупных капель можно использовать пипетку с тонким носиком, а более мелкие капли нужно собрать амальгамированной (покрытой тончайшим слоем ртути) медной проволокой, которую нужно перед этим тщательно зачистить, чтобы ртуть смочила медь (лучше всего для этой цели подходит азотная кислота, в которую нужно на одну — две секунды опустить конец проволоки). Подойдет и оловянный припой. Налипшую ртуть следует стряхивать в ту же емкость, которую потом нужно сдать на утилизацию — туда же, куда сдают перегоревшие люминесцентные и энергосберегающие лампы, которые тоже содержат ртуть. Невидимые глазом, а также попавшие в щели капельки следует залить раствором хлорного железа FeCl3, который превратит ртуть в неиспаряющуюся и малоядовитую каломель Hg2Cl2. В крайнем случае следует залить это место раствором «марганцовки» или йодной настойкой. Пол на следующий день нужно тщательно вымыть. Ни в коем случае нельзя убирать частицы ртути при помощи пылесоса, так как это вызывает рассеивание на более мелкие частицы через выход воздуха из пылесоса, а это повлечет за собой увеличение концентрации паров ртути и усложнит процесс очистки помещений.
В природе существует множество полезных ископаемых, которые обладают определёнными характеристиками и используются для различных нужд человека.
Одним из древних металлов является ртуть. Химический элемент имеет особенности, которые делают его незаменимым в современной промышленности.
История открытия
О ртути люди узнали ещё в древние времена. Вещество часто находили в виде самородка, который представлял жидкие капли на горных породах. Но чаще металл получали из его соединения с серой — сульфида ртути (HgS), или киновари. Люди из Древнего Рима и Греции применяли вещество для очистки золота от разных примесей. В то время народы уже раскрыли, что металл и его соединения вредны для здоровья.
О веществе стало известно так рано, потому что добываемая киноварь быстро разлагалась под воздействием высоких температур воздуха и образовывала металлическую ртуть. В период древних цивилизаций люди обжигали киноварь в глиняных сосудах, на крышках которых конденсировался необходимый металл. Сегодня для этого применяют трубчатые печи.
Когда алхимики открыли новый элемент, они назвали его «живым серебром» (argentum vivum). Учёные считали его женским началом веществ и матерью всех металлов. Они полагали, что при помощи мышьяка и серы жидкой ртути можно вернуть твёрдость и получить таким образом золото.
В течение многих столетий алхимики утверждали, что это вещество содержится в любом металле. Кроме того, они верили, что оно могло стать основой для философского камня. Позже веществу дали другое название — hydrargyrum, что с латинского переводится как «жидкое серебро».
В Средневековье известные химические элементы ассоциировали с открытыми в то время семью планетами. Ртуть совпадала с обозначением Меркурия. Так люди подчёркивали близость металла к золоту (Солнцу), поскольку небесное тело расположено близко к светилу. Также название «Mercury» соответствовало уникальному свойству элемента. Капли вещества стремительно перекатывались по гладким поверхностям, что напоминало быстрое передвижение античного бога-посланника Меркурия.
В 1735 году шведский учёный Георг Брандт подробно описал образование вещества в чистом виде. Для обозначения уже использовался символ планеты Меркурий.
В 1759 году Браун и Ломоносов доказали, что вещество относится к металлам. Они смогли определить его металлические свойства в твёрдом агрегатном состоянии после замерзания.
Нахождение в природе
В России есть 23 места, где добывают ртуть. Самое крупное из них находится на Чукотке.
Металл также добывают и в других странах:
Концентрация вещества в земной коре составляет всего 83 мг/т. Редкий металл слабо соединяется химически с иными элементами. Но ртутные руды часто бывают очень концентрированными, если их сравнивать с обычными горными породами, и могут содержать до 2,5% серебристого металла.
В основном ртуть рассеяна в природе. Лишь 0,02% от всего её объёма заключено в месторождениях. Наибольшие концентрации наблюдаются в глинистых сланцах. В Мировом океане объём вещества достигает 0,1 мкг/л.
Металл можно обнаружить во многих сульфидных минералах.
Основными природными материалами для добычи вещества выступают антимониты, блёклые руды, сфалериты и реальгары. Ртуть добывают из киновари, метациннабарита, а также из селенидов металла (тиманита и онофрита).
Описание элемента
Элемент расположен между золотом и таллием в таблице Менделеева. Ртуть имеет порядковый номер 80 и обозначается Hg. Она относится к элементам шестого периода и входит в подгруппу цинка. Это единственный металл, простые вещества которого находятся в жидком состоянии при нормальных условиях.
Непрозрачный металл представлен тяжёлой серебристой жидкостью.
Основные физические свойства ртути:
В жидком виде ртуть обладает металлическим блеском. Когда вещество затвердевает, оно приобретает кристаллическое состояние. Ртуть может взаимодействовать со многими металлами, образуя при реакции с ними соединения, которые называются амальгамы. Химический элемент относится к группе диамагнетиков: он не магнитится, а отталкивается в присутствии магнитов. При горении вещество образует ядовитые испарения.
Ртуть характеризуется высоким потенциалом ионизации. Она способна восстанавливаться до атомарной формы (самородка). Кроме того, элемент обладает высокой химической стойкостью к кислороду и кислотам.
Химические особенности
Металл характеризуется степенью окисления +1 и +2. В первом случае он представлен двухъядерным катионом Hg22+ с металлической связью и склонен к диспропорционированию, которое проходит при нагревании и разбавлении водой.
Элемент со степенью окисления +2 образует с различными лигандами устойчивые комплексы. Прочные ковалентные связи наблюдаются с йодом, серой и углеродом. С последним веществом ртуть образует самые устойчивые соединения.
Сферы использования
Применение ртути в современной промышленности соблюдается с большой осторожностью. Перед работой с этим элементом нужно познакомиться с мерами безопасности.
Сферы использования металла:
В области медицины вещество практически не используют, поскольку оно считается опасным для жизни человека. В виде консерванта он содержится в малых количествах в вакцинах. В прошлом ртуть использовали в качестве слабительного, мочегонного и антисептического средства.
С 2020 года будет запрещено производство некоторых предметов для бытовых нужд, содержащих токсичный металл, поскольку испарения часто вызывают отравления у людей. Также введут регулирование применения вещества и ограничат многие промышленные процессы и отрасли, связанные с этим химическим элементом.
Ртуть — довольно интересный металл, который проявляет необычные свойства. О нём имеется немало занимательных фактов, однако учёные продолжают изучать особенности «жидкого серебра». Возможно, в будущем этому элементу найдут дополнительное применение и смогут снизить степень его токсичности.