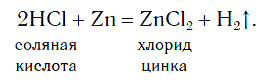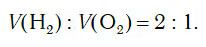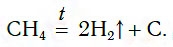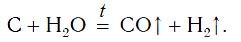Получение водорода в промышленности и в лаборатории
Задача 786.
Как получают водород в промышленности и в лаборатории? Привести уравнения реакций.
Решение:
а) Получение водорода в промышленности:
1. Получение синтез-газа:
3. Электролиз водного раствора едкого натра или едкого калия. Используют 25% NaOH или 34% КОН. Электроды изготавливают из листового никеля. При этом на катоде выделяется водород, а на аноде – кислород:
5. Получение водорода из природного газа. В промышленности по этому методу природный газ смешивают с кислородом и водяным паром при нагревании данной смеси до 800-900 0 С в присутствии катализатора (пароводяная и кислородная конверсия):
6. Метод выделения водорода из коксового газа или из газов переработки нефти. Метод основан на глубоко охлаждении газовой смеси, при котором все газы кроме водорода сжижаются – водород остаётся в газовой фазе, которую под давлением собирают в баллоны.
7. Метод получения водорода при получении сажи из природного газа:
8. Метод получения водорода при пропускании паров воды над раскалённым углем при температуре 10000 о C (водяной газ, содержащий до 86% угарного газа и водорода):
б) Получение водорода в лабораторных условиях:
1. Метод растворения цинка в холодной соляной кислоте или в разбавленной серной кислоте:
2. Растворение алюминия с сильными щелочами:
3. Электролиз раствора КОН (электроды из листового никеля):
4. Действие порошком алюминия на кипящую воду в присутствии нескольких капель разбавленного перманганата калия:
5. В полевых условиях водород получают из смеси (порошок ферросилиция с сухим Са(ОН)2 и NaOH). При поджигании данной смеси сначала она начинает тлеть, а затем наблюдается выделение водорода:
Смесь называется гидрогенит.
Следовательно, при электролизе H2SO4 будет разряжаться ионы водорода и выделяться газообразный водород.
При электролизе раствора CuSO4 будет происходить разряд ионов меди и, при этом на катоде выделится металлическая медь, потому что электродный потенциал меди значительно положительнее, чем потенциал водородного электрода.
Таким образом, для электрохимического получения водорода можно использовать растворы H2SO4, K2SO4 KCl и NaOH.
Из уравнения реакции следует, что из четырёх молекул парообразной воды образуется четыре молекулы газообразного водорода, т.е. реакция протекает без изменения числа молей газообразных веществ, поэтому равновесие системы не нарушается при изменении давления. В данном случае при удалении продукта реакции водорода из реакционной зоны равновесие системы согласно принципу Ле Шателье сместится вправо, в сторону увеличения образования водорода. Но лучше всего выводить из реакционной системы твёрдый продукт Fe3O4, что будет способствовать смещению равновесия вправо, если железную окалину направлять на регенерацию, допустим посредством накаливания окалины в струе паровоздушной смеси и, затем, возвратить образуемое металлическое железо в реакционную зону. Избыток металлического железа будет способствовать ускорению реакции и, следовательно, увеличению продукта реакции. Таким образом, отведение водорода и регенерация железа способствуют протеканию реакции до практически полного окисления металлического железа.
Способы получения водорода в промышленности и лаборатории
Получение водорода в промышленности
В промышленности водород получают главным образом из природных и попутных газов, коксового газа и продуктов газификации топлива (водяного и паровоздушного газов), путем неполного окисления углеводородов.
Основным источником водорода в промышленности является конверсия (от лат. “превращение”) углеводородов, главным образом природного газа, парами воды (пароводяная конверсия):
CH4 + H2O → CO + 3H2, 800-900 °C, ΔH298 0 = 206,2 кДж/моль
С последующим каталитическим взаимодействием оксида углерода (II) с парами воды:
Катализатором этой реакции служит Fe2O3 с активирующими добавками (Cr2O3, Al2O3, K2O и др.).
Эндотермичность процесса конверсии метана можно частично восполнить энергией, выделяющейся при неполном его окислении.
Этот процесс называется кислородной конверсией метана. Поэтому в промышленности часто комбинируют все эти три процесса в один. Для этого природный газ смешивается с водяным паром и кислородом:
Диоксид углерода удаляют промывкой газовой смеси водой под давлением и окончательно – поглощением растворами щелочей.
Все описанные выше процессы используются как по отдельности, так и в сочетании друг с другом.
Помимо природного газа для получения водорода путем конверсии используют генераторный (CO + N2), водяной (CO + H2) – пароводяная конверсия, попутные газы – пароводяная и (или) кислородная конверсия.
В связи с уменьшением запасов углеводородного сырья большой интерес приобретает метод получения водорода восстановлением водяного пара раскаленным углем:
C + H2O → CO + H2, 1000 °C, ΔH298 0 = 131 кДж/моль
При этом образуется генераторный газ. Затраты энергии на его получение можно компенсировать за счет реакции неполного окисления угля:
При комбинировании этих процессов получается водяной газ, состоящий в основном из смеси водорода и угарного газа:
Важным следствием является то, что получаемые генераторный и водяной газы можно использовать для дальнейшего получения водорода методом пароводяной конверсии.
Из газовых смесей с большим содержанием водорода (коксовый газ, газы нефтепереработки) его получают путем глубокого охлаждения смеси, при котором практически все газы кроме водорода сжижаются.
Водород высокой чистоты получают электролизом водных растворов щелочей (NaOH или KOH). Раньше для этого использовалась серная кислота. Однако это нерационально из-за быстрого коррозионного разрушения стальной аппаратуры. Хотя образующаяся в процессе электролиза пероксодисерная кислота H2S2O8 может использоваться для получения пергидроля:
В случае щелочей концентрация этих растворов выбирается такой, которая отвечает их максимальной электрической проводимости (25% для NaOH и 34% для KOH). Электроды обычно изготавливают из листового никеля. Этот металл не подвергается коррозии в растворах щелочей, даже будучи анодом. В случае надобности получающийся водород очищают от паров воды и следов кислорода. Этим способом целесообразно получать водород в районах с дешевой электроэнергией.
Водород образуется также как побочный продукт в процессе получения хлора и щелочей электролизом водных растворов хлоридов щелочных металлов.
Потенциальные способы получения водорода в промышленности
2H2O → 2H2 + O2, 2000 °C, электрическая дуга.
Недостаток – большие расходы энергии.
3. Биохимическое разложение воды под действием бактерий.
4. Химическое разложение воды, восстановление водорода:
Получение водорода в лаборатории
Восстановление металлами и неметаллами различных водородсодержащих соединений: воды, кислот, щелочей. Чаще используется взаимодействие разбавленных кислот (соляной, серной) с цинком, реже с железом. Если реакция выделения водорода проходит очень медленно, к кислоте добавляют несколько капель любого раствора CuCl2 (к соляной кислоте) или CuSO4 (к серной кислоте). Медь выделяется на цинке (или железе) и образует с ним гальваническую пару, что ускоряет выделение водорода. Реакции обычно проводят в аппарате Кипа.
Цинк обычно содержит примеси мышьяка, сурьмы и др. элементов, поэтому выходящий из аппарата водород немного загрязнен AsH3 и др. газами. Такой газ взрывоопасен, поэтому перед его использованием водород проверяют на чистоту. Для этого из аппарата Киппа через некоторое время после начала его работы отбирают в пробирку (держа ее вверх дном) пробу газа и подносят отверстие пробирки к пламени горелки. Если при этом водород горит спокойно (без хлопка), то он не содержит примеси воздуха. В противном случае следует еще раз удалить из аппарата часть газа и повторить испытание. Этот процесс повторяют до получения спокойного, слабо светящегося пламени водорода. В противном случае нужно менять цинк (железо) на более чистые.
Для демонстрационных опытов можно использовать такую установку:
Очень чистый водород в лаборатории можно получить электролизом водных растворов щелочей.
Для получения водорода в лаборатории также можно использовать гидрид кальция:
Пропускание паров воды через раскаленную железную трубку:
Урок 26. Получение водорода и его применение
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.
Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
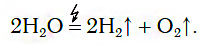
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
Существуют и другие промышленные способы получения водорода.
Применение водорода
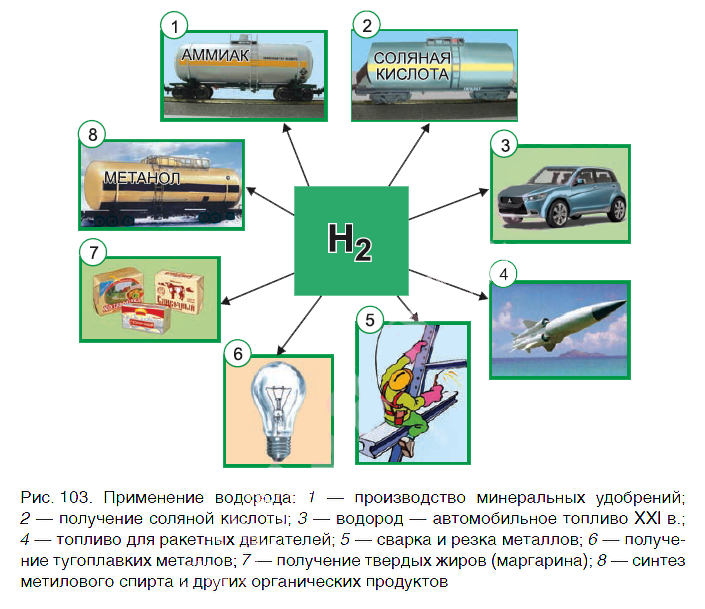
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 о С. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.
В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Получение водорода
История открытия водорода История водорода начинается с XVI века, когда было замечено, что при действии кислот на железо и другие металлы выделяется некий неизвестный газ. Первоначально его назвали «горючим воздухом». Такое название газ получил из-за способности гореть. Во второй половине XVIII века английский ученый Генри Кавендиш получил водород при действии соляной кислоты HCl на цинк:
Zn + 2HCl = ZnCl2 + H2
Что же такое кислота с точки зрения химии? Кислота – это сложное вещество, в состав которого всегда входят атомы водорода. В формулах кислот атомы водорода принято писать на первом месте. Атомы, следующие в формуле за водородом, называют кислотным остатком. Так, в соляной кислоте HCl кислотный остаток – Cl.
Например, в серной кислоте H2SO4, кислотный остаток – SO4. Кислота – сложное вещество, в состав которого входят атомы водорода и кислотный остаток Генри Кавендиш изучил свойства «горючего воздуха». Он установил, что этот газ намного легче воздуха, а при сгорании на воздухе образует прозрачные капли жидкости. Этой жидкостью оказалась вода.
Генри Кавендиша считают первооткрывателем водорода. Вывод о том, что «горючий воздух» представляет собой простое вещество, был сделан в 1784 году французским химиком Антуаном Лораном Лавуазье. Антуан Лоран Лавуазье дал этому веществу латинское название (Hydrogenium), которое происходило от греческих слов «хюдор» – вода и «геннао» – рождаю. В те годы под элементами подразумевали простые вещества, которые нельзя далее разложить на составные части. Поэтому у химического элемента водорода такое же название, как и у просто вещества H2. Русское слово водород – это точный перевод латинского названия Hydrogenium.
Получение водорода в лаборатории
Современный лабораторный способ получения водорода не отличается от того, которым его получал Генри Кавендиш. Это реакции металлов с кислотами. В лаборатории водород получают в аппарате Киппа (рисунок 152).
Аппарат Киппа изготовляется из стекла и состоит из нескольких частей:
Реакционная колба имеет верхнюю шарообразную часть с отверстием, в которое вставляется газоотводная трубка, снабженная краном или зажимом, и нижний резервуар в виде полусферы. Нижний резервуар и реакционная колба разделены резиновой или пластиковой прокладкой с отверстием, через которое проходит в нижний резервуар длинная трубка воронки, доходящая почти до дна. На прокладку через боковое отверстие шпателем насыпают твёрдые вещества (мрамор, цинк). Отверстие закрывается пробкой с газоотводной трубкой. Затем при открытом кране или зажиме в верхнюю воронку заливается раствор кислоты. Когда уровень жидкости достигает вещества на прокладке, начинается химическая реакция с выделением газа. При закрытии крана давление выделяющегося газа выдавливает жидкость из реактора в верхнюю часть воронки. Реакция прекращается. Открытие крана приводит к возобновлению реакции. Поместим в реакционную колбу кусочки цинка. В качестве кислоты воспользуемся серной кислотой. При контакте цинка и серной кислоты протекает реакция:
Zn + H2SO4 = ZnSO4 + H2
Водородом можно заполнить мыльный пузырь.
Для этого необходимо опустить газоотводную трубку в мыльный раствор. На конце трубки начнется формирование мыльного пузыря, заполненного водородом; со временем пузырь отрывается и улетает вверх, что доказывает легкость водорода. Соберем выделяющийся водород. С учетом того, что водород намного легче воздуха, для сбора водорода сосуд, в котором собирается газ, необходимо располагать вверх дном, или производить собирание методом вытеснения воды. Как обнаружить водород? Заполним пробирку водородом, держа ее вверх дном, по отношению к газоотводной трубке. Поднесем пробирку отверстием к пламени спиртовки – слышится характерный хлопок.
Хлопок – это признак того, что в пробирке содержится водород. При поднесении пробирки к пламени водород вступает в реакцию с кислородом, содержащимся в воздухе. При малых количествах реакция кислорода и водорода сопровождается хлопком. Более подробно об этой реакции будет рассказано в следующем параграфе.
Получение водорода в промышленности
Одним из промышленных способов получения водорода является реакция разложения воды под действием электрического тока:
2H2O эл.ток → 2H2 + O2.
Данный метод позволяет получить чистый водород и кислород. Процесс превращения химических веществ в другие вещества под действием электричества называется электролизом.
Электролиз – химическая реакция, протекающая под действием электрического тока Проведем электролиз воды. В стакан наполненный водой, опустим металлические электроды. Поверх электродов опустим в стакан пробирки, заполненные водой. Подсоединим электроды к источнику тока – батарейке. В пробирках наблюдается выделение газов – водорода и кислорода, которые вытесняют воду. Наблюдая за процессом электролиза, можно заметить, что в одной из пробирок газа собирается в два раза больше, чем в другой. Проанализировав уравнение реакции электролиза воды, можно сделать вывод, в какой пробирке выделяется водород, а в какой – кислород. Попробуйте это сделать самостоятельно.
Существуют и другие способы получения водорода. Железо-паровой метод долгое время широко применялся в промышленности. Через электрическую трубчатую печь проходит трубка из нержавеющей стали, заполненная железными стружками. Через трубку с железными стружками пропускают водяной пар. При температуре около 800°С пары воды взаимодействуют с железом, образуя оксид Fe3O4 (железную окалину) и газообразный водород:
3Fe + 4Н2О = 4Н2 + Fe3O4.
Можно получить Н2, пропуская Н2О через слой раскаленного угля. При этом образуется смесь двух газов – СО и Н2 (водяной газ):
Н2О + С = CO + Н2
В настоящее время водород получают взаимодействием углеводородов (в основном метана, СН4) с водяным паром или неполным окислением метана кислородом:
2СН4 + О2 = 2СО + 4Н2
Итог статьи:
Водород. Физические и химические свойства, получение

Водород занимает первое место в периодической системе (Z = 1). Он имеет простейшее строение атома: ядро атома – 1 протон, окружено электронным облаком, состоящим из 1 электрона.
В одних условиях водород проявляет металлические свойства (отдает электрон), в других — неметаллические (принимает электрон).
В природе встречаются изотопы водорода: 1Н — протий (ядро состоит из одного протона), 2Н — дейтерий (D — ядро состоит из одного протона и одного нейтрона), 3Н — тритий (Т — ядро состоит из одного протона и двух нейтронов).
Простое вещество водород
Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью.
Физические свойства. Водород — бесцветный нетоксичный газ без запаха и вкуса. Молекула водорода не полярна. Поэтому силы межмолекулярного взаимодействия в газообразном водороде малы. Это проявляется в низких температурах кипения (-252,6 0С) и плавления (-259,2 0С).
Водород легче воздуха, D (по воздуху) = 0,069; незначительно растворяется в воде (в 100 объемах H2O растворяется 2 объема H2). Поэтому водород при его получении в лаборатории можно собирать методами вытеснения воздуха или воды.
Получение водорода
1.Действие разбавленных кислот на металлы:
Zn +2HCl → ZnCl2 +H2↑
2.Взаимодействие щелочных и щ-з металлов с водой:
Ca +2H2O → Ca(OH)2 +H2↑
3.Гидролиз гидридов: гидриды металлов легко разлагаются водой с образованием соответствующей щелочи и водорода:
NaH +H2O → NaOH +H2↑
СаH2 + 2Н2О = Са(ОН)2 + 2Н2↑
5. Электролиз воды. Для увеличения электрической проводимости воды к ней добавляют электролит, например NаОН, Н2SO4 или Na2SO4. На катоде образуется 2 объема водорода, на аноде — 1 объем кислорода.
2H2O → 2H2+О2
Промышленное получение водорода
1. Конверсия метана с водяным паром, Ni 800 °С (самый дешевый):
CH4 + H2O → CO + 3 H2
CO + H2O → CO2 + H2
2. Пары воды через раскаленный кокс при 1000 о С:
С + H2O → CO + H2
CO +H2O → CO2 + H2
Образующийся оксид углерода (IV) поглощается водой, этим способом получают 50 % промышленного водорода.
3. Нагреванием метана до 350°С в присутствии железного или никелевого катализатора:
СH4 → С + 2Н2↑
4. Электролизом водных растворов KCl или NaCl, как побочный продукт:
2Н2О + 2NaCl→ Cl2↑ + H2↑ + 2NaOH
Химические свойства водорода
1) С галогенами образует галогеноводороды:
Н2 + Cl2 → 2НСl.
При этом с фтором — взрывается, с хлором и бромом реагирует лишь при освещении или нагревании, а с йодом только при нагревании.
2) С кислородом:
2Н2 + О2 → 2Н2О
с выделением тепла. При обычных температурах реакция протекает медленно, выше 550°С — со взрывом. Смесь 2 объемов Н2 и 1 объема О2 называется гремучим газом.
3) При нагревании энергично реагирует с серойь(значительно труднее с селеном и теллуром):
Н2 + S → H2S (сероводород),
4) С азотом с образованием аммиака лишь на катализаторе и при повышенных температурах и давлениях:
ЗН2 + N2 → 2NН3
5) С углеродом при высоких температурах:
2Н2 + С → СН4 (метан)
Со сложными веществами:
7) С оксидами металлов (используется для восстановления металлов):
CuO + H2 → Cu + H2O
Fe3O4 + 4H2 → 3Fe + 4Н2О
8) с оксидом углерода (II):
CO + 2H2 → CH3OH
Синтез — газ (смесь водорода и угарного газа) имеет важное практическое значение, тк в зависимости от температуры, давления и катализатора образуются различные органические соединения, например НСНО, СН3ОН и другие.
9)Ненасыщенные углеводороды реагируют с водородом, переходя в насыщенные:
СnН2n + Н2 → СnН2n+2.