Сульфат алюминия
| Сульфат алюминия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Сульфат алюминия |
| Химическая формула | Al2(SO4)3 |
| Физические свойства | |
| Молярная масса | 342,15 г/моль |
| Плотность | 1,62—2,672 г/см³ |
| Термические свойства | |
| Температура плавления | 770 °C |
| Классификация | |
| Рег. номер CAS | 10043-01-3 |
| Регистрационный номер EC | 233-135-0 |
Содержание
Описание
Сульфат алюминия — это соль белого цвета с серым, голубым или розовым оттенком, при обычных условиях существует в виде кристаллогидрата Al2(SO4)3·18H2O — бесцветных кристаллов. При нагревании теряет воду не плавясь, при прокаливании распадается на Al2O3 и SO3. Хорошо растворяется в воде. Технический сульфат алюминия можно получить, обрабатывая серной кислотой боксит или глину, а чистый продукт, — растворяя Al(OH)3 в горячей концентрированной H2SO4.
Сульфат алюминия применяется для очистки воды хозяйственно-питьевого и промышленного назначения и для использования в бумажной, текстильной, кожевенной и других отраслях промышленности.
Используется в качестве пищевой добавки E-520. [1]
Химические свойства
Сульфат алюминия разлагается при температурах от 770 до 860 °C:
Получение
Сульфат алюминия получают взаимодействием гидроксида алюминия с серной кислотой:
Также сульфат алюминия получают при соединении алюминия с серной кислотой:
Сульфат алюминия
Сульфат алюминия растворим в воде и, в основном, используется в качестве флокулянта для очистки питьевой и технической воды станциями очистки сточных вод, а также в производстве бумаги.
Сульфат алюминия иногда упоминается как серная кислота, квасцы алюмоаммиачные или пищевая добавка Е 523. Безводная форма встречается в природе как редкий минерал Миллозевичит, содержащийся в вулканических средах, а также получается при сжигании угольных отходов. Сульфат алюминия образует множество различных гидратов, в числе которых кристаллогидрат Al2(SO4)3*16H2O и октадекагидрат Al2(SO4)3*18H2O.
Сульфат алюминия обладает способностью поглощать и удерживать молекулы воды из окружающей атмосферы.
Получение сульфата алюминия технического возможно путем добавления гидроксида алюминия Al(OH)3 в серную кислоту H2SO 4.
Также возможно получение сульфата алюминия из тетрагидроксоалюмината натрия.
Сульфат алюминия – это белое или почти белое кристаллической формы или в виде порошка соединение без запаха. Он растворим в воде, не летуч и легковоспламеняем. Сульфат алюминия обладает чрезвычайно кислым вкусом.
Применение сульфата алюминия
Раствор сульфата алюминия используется для очистки воды и как краситель в обработке текстиля. В процессе очистки воды раствор сульфата алюминия приводит к коагулированию, нежелательные примеси и загрязненные частицы оседают на дно сосуда и легко отфильтровываются.
При растворении в большом количестве нейтральной или слегка щелочной воды, раствор сульфата алюминия образует студенистый осадок гидроксида алюминия Al(OH)3, который используется при печати и окрашивании тканей, так как является нерастворимым пигментом.
Сульфат алюминия иногда используется для снижения pH почвы сада, что в свою очередь приводит при выращивании некоторых видов цветов (Гортензии) к их повторному цветению.
Сульфат алюминия является активным ингредиентом некоторых антиперспирантов.
В строительстве он используется в качестве гидроизолятора и ускорителя в производстве бетона.
Сульфат алюминия может быть использован в борьбе с моллюсками, насекомыми и слизняками.

В медицине сульфат алюминия входит в состав лекарств, облегчающих боль и дискомфорт, вызванные укусами насекомых. Он помогает разрушить токсичные химические вещества, содержащиеся в укусах, и помогает уменьшить их воздействие на кожу. Эти препараты выпускается в виде спреев, которые наносятся непосредственно на пораженные участки кожи и эффективнее помогают, если будут использованы сразу же после укуса.
Вред сульфата алюминия
Сульфат алюминия вреден при проглатывании или вдыхании. Вдыхание паров сульфата алюминия вызывает кашель и, возможно, одышку.
При контакте с кожей или глазами сульфат алюминия вызывает раздражение, покраснение, зуд и боль. Употребление сульфата алюминия внутрь приводит к сильному раздражению кишечника и желудка, сопровождаемое рвотой, тошнотой и диареей.
Это соединение может вызывать сильные ожоги, если контактирует с открытыми участками кожи.
Первая помощь при отравлении сульфатом алюминия
При попадании сульфата алюминия на кожу или в глаза необходимо промыть пораженный участок водой. В случае вдыхания паров необходимо выйти из токсичной области и медленно отдышаться. Если сульфат алюминия был применен внутрь, необходимо выпить стакан молока, а затем спровоцировать рвоту.
При отравлении сульфатом алюминия ни в коем случае нельзя использовать бикарбонаты, так как такое сочетание в буквальном смысле является взрывным.
Хранение сульфата алюминия
Сульфат алюминия необходимо хранить в прохладном, сухом месте в плотно закрытой таре, не смешивая с другими веществами.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Кровь человека «бегает» по сосудам под огромным давлением и при нарушении их целостности способна выстрелить на расстояние до 10 метров.
Наши почки способны очистить за одну минуту три литра крови.
Печень – это самый тяжелый орган в нашем теле. Ее средний вес составляет 1,5 кг.
Для того чтобы сказать даже самые короткие и простые слова, мы задействуем 72 мышцы.
Самое редкое заболевание – болезнь Куру. Болеют ей только представители племени фор в Новой Гвинее. Больной умирает от смеха. Считается, что причиной возникновения болезни является поедание человеческого мозга.
Раньше считалось, что зевота обогащает организм кислородом. Однако это мнение было опровергнуто. Ученые доказали, что зевая, человек охлаждает мозг и улучшает его работоспособность.
Большинство женщин способно получать больше удовольствия от созерцания своего красивого тела в зеркале, чем от секса. Так что, женщины, стремитесь к стройности.
Если улыбаться всего два раза в день – можно понизить кровяное давление и снизить риск возникновения инфарктов и инсультов.
В стремлении вытащить больного, доктора часто перегибают палку. Так, например, некий Чарльз Йенсен в период с 1954 по 1994 гг. пережил более 900 операций по удалению новообразований.
В нашем кишечнике рождаются, живут и умирают миллионы бактерий. Их можно увидеть только при сильном увеличении, но, если бы они собрались вместе, то поместились бы в обычной кофейной чашке.
Общеизвестный препарат «Виагра» изначально разрабатывался для лечения артериальной гипертонии.
74-летний житель Австралии Джеймс Харрисон становился донором крови около 1000 раз. У него редкая группа крови, антитела которой помогают выжить новорожденным с тяжелой формой анемии. Таким образом, австралиец спас около двух миллионов детей.
Стоматологи появились относительно недавно. Еще в 19 веке вырывать больные зубы входило в обязанности обычного парикмахера.
Существуют очень любопытные медицинские синдромы, например, навязчивое заглатывание предметов. В желудке одной пациентки, страдающей от этой мании, было обнаружено 2500 инородных предметов.
Кариес – это самое распространенное инфекционное заболевание в мире, соперничать с которым не может даже грипп.
Полиоксидоний относится к иммуномодулирующим препаратам. Он воздействует на определенные звенья иммунитета, благодаря чему способствует повышению устойчивости о.
Алюминий. Химия алюминия и его соединений
Бинарные соединения алюминия
Алюминий
Положение в периодической системе химических элементов
Алюминий расположен в главной подгруппе III группы (или в 13 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение алюминия и свойства
Электронная конфигурация алюминия в основном состоянии :
+13Al 1s 2 2s 2 2p 6 3s 2 3p 1 1s 



Электронная конфигурация алюминия в возбужденном состоянии :
+13Al * 1s 2 2s 2 2p 6 3s 1 3p 2 1s 



Алюминий проявляет парамагнитные свойства. Алюминий на воздухе быстро образует прочные оксидные плёнки, защищающие поверхность от дальнейшего взаимодействия, поэтому устойчив к коррозии.
Физические свойства
Алюминий – лёгкий металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Обладает высокой тепло- и электропроводностью.
Алюминий — один из наиболее ценных цветных металлов для вторичной переработки. На протяжении последних лет, цена на лом алюминия в пунктах приема непреклонно растет. По ссылке можно узнать о том, как сдать лом алюминия.
Нахождение в природе
Алюминий — самый распространенный металл в природе, и 3-й по распространенности среди всех элементов (после кислорода и кремния). Содержание в земной коре — около 8%.
В природе алюминий встречается в виде соединений:
Корунд Al2O3. Красный корунд называют рубином, синий корунд называют сапфиром.
Способы получения
Алюминий образует прочную химическую связь с кислородом. Поэтому традиционные способы получения алюминия восстановлением из оксида протекают требуют больших затрат энергии. Для промышленного получения алюминия используют процесс Холла-Эру. Для понижения температуры плавления оксид алюминия растворяют в расплавленном криолите (при температуре 960-970 о С) Na3AlF6, а затем подвергают электролизу с углеродными электродами. При растворении в расплаве криолита оксид алюминия распадается на ионы:
На катоде происходит восстановление ионов алюминия:
Катод: Al 3+ +3e → Al 0
На аноде происходит окисление алюминат-ионов:
Суммарное уравнение электролиза расплава оксида алюминия:
Лабораторный способ получения алюминия заключается в восстановлении алюминия из безводного хлорида алюминия металлическим калием:
AlCl3 + 3K → Al + 3KCl
Качественные реакции
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид алюминия растворяется с образованием тетрагидроксоалюмината:
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Соли алюминия можно обнаружить с помощью водного раствора аммиака. При взаимодействии растворимых солей алюминия с водным раствором аммиака также в ыпадает полупрозрачный студенистый осадок гидроксида алюминия.
AlCl3 + 3NH3·H2O = Al(OH)3 ↓ + 3NH4Cl
Al 3+ + 3NH3·H2O = Al(OH)3 ↓ + 3NH4 +
Видеоопыт взаимодействия раствора хлорида алюминия с раствором аммиака можно посмотреть здесь.
Химические свойства
1.1. Алюминий реагируют с галогенами с образованием галогенидов:
1.2. Алюминий реагирует с серой с образованием сульфидов:
Al + P → AlP
1.4. С азотом алюминий реагирует при нагревании до 1000 о С с образованием нитрида:
2Al + N2 → 2AlN
1.5. Алюминий реагирует с углеродом с образованием карбида алюминия:
1.6. Алюминий взаимодействует с кислородом с образованием оксида:
Видеоопыт взаимодействия алюминия с кислородом воздуха (горение алюминия на воздухе) можно посмотреть здесь.
2. Алюминий взаимодействует со сложными веществами:
2.1. Реагирует ли алюминий с водой? Ответ на этот вопрос вы без труда найдете, если покопаетесь немного в своей памяти. Наверняка хотя бы раз в жизни вы встречались с алюминиевыми кастрюлями или алюминиевыми столовыми приборами. Такой вопрос я любил задавать студентам на экзаменах. Что самое удивительное, ответы я получал разные — у кого-то алюминий таки реагировал с водой. И очень, очень многие сдавались после вопроса: «Может быть, алюминий реагирует с водой при нагревании?» При нагревании алюминий реагировал с водой уже у половины респондентов))
2Al 0 + 6 H2 + O → 2 Al +3 ( OH)3 + 3 H2 0
Амальгаму алюминия можно получить, выдержав кусочки алюминия в растворе хлорида ртути ( II ):
3HgCl2 + 2Al → 2AlCl3 + 3Hg
Видеоопыт взаимодействия амальгамы алюминия с водой можно посмотреть здесь.
2.2. Алюминий взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль и водород.
2Al + 6HCl = 2AlCl3 + 3H2↑
2.3. При обычных условиях алюминий не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат алюминия и вода:
2.4. Алюминий не реагирует с концентрированной азотной кислотой также из-за пассивации.
С разбавленной азотной кислотой алюминий реагирует с образованием молекулярного азота:
При взаимодействии алюминия в виде порошка с очень разбавленной азотной кислотой может образоваться нитрат аммония:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2 ↑
Видеоопыт взаимодействия алюминия со щелочью и водой можно посмотреть здесь.
Алюминий реагирует с расплавом щелочи с образованием алюмината и водорода:
2Al + 6NaOH → 2Na3AlO3 + 3H2 ↑
Эту же реакцию можно записать в другом виде (в ЕГЭ рекомендую записывать реакцию именно в таком виде):
2Al + 6NaOH → 2NaAlO2 + 3H2↑ + 2Na2O
2Al + 3CuO → 3Cu + Al2O3
Еще пример : алюминий восстанавливает железо из железной окалины, оксида железа (II, III):
Восстановительные свойства алюминия также проявляются при взаимодействии его с сильными окислителями: пероксидом натрия, нитратами и нитритами в щелочной среде, перманганатами, соединениями хрома (VI):
Структура сульфата алюминия (Al2 (SO4) 3), применение, виды, токсичность
сульфат алюминия неорганическая соль алюминия формулы Al2(SO4)3, это обычно выглядит как белое твердое вещество с блестящими кристаллами. Цвет соединения будет зависеть от его концентрации железа и любых других примесей. Существует два основных типа сульфата алюминия: A и B.
На нижнем изображении показаны белые кристаллы гидратированного сульфата алюминия. Можно отметить отсутствие коричневых окрасок, указывающих на ионы железа в кристаллической решетке..
Кроме того, он может образовывать двойные соли с калием и аммонием, соединения, известные как квасцы. Частично это может быть связано со сродством воды в гидратах удерживать другие ионы, кроме алюминия.
Сульфат алюминия может разлагаться под действием воды в гидроксиде алюминия и серной кислоте. Это свойство позволило использовать его в качестве подкислителя почв.
Это также токсичное соединение, особенно при контакте с его порошком. Тем не менее, он имеет бесконечное число применений и применений, которые идут от очистки воды с помощью метода коагуляции, происходящего через его использование в нескольких отраслях промышленности, до его использования в терапевтических целях..
структура
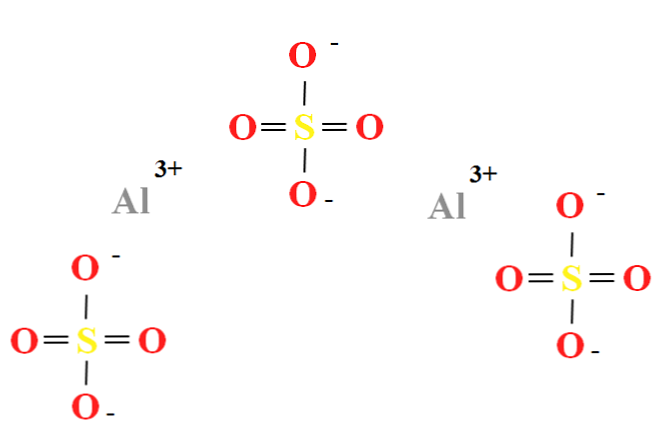
Сульфат алюминия имеет соотношение двух катионов Al 3+ на каждые три аниона ТАК4 2- (верхнее изображение), что можно наблюдать непосредственно в его химической формуле Al2(SO4)3.
Обратите внимание, что Аль 3+ они сероватые, а ТАК4 2- они желтые (для атома серы) и красные (для атомов кислорода).
Сульфат алюминия может иметь много структур, хотя его гидраты имеют тенденцию принимать моноклинную кристаллическую систему.
Физико-химические свойства
внешний вид
Он выглядит как твердое вещество с блестящими белыми кристаллами, гранулами или порошком.
Молекулярный вес
342,31 г / моль (безводный).
запах
аромат
Сладкий вкус умеренно вяжущий.
Точка плавления
770ºС безводная форма (86,5ºС октадекагидратада)
Растворимость в воде
31,2 г / 100 мл при 0 ° С; 36,4 г / 100 мл при 20 ° С и 89 г / 100 мл при 100 ° С.
плотность
растворимость
Слабо растворим в этиловом спирте.
Давление пара
стабильность
Стабильный в воздухе.
разложение
При нагревании примерно до точки плавления он может разлагаться, выделяя, в частности, оксид серы, токсичный газ..
коррозионная активность
Растворы сульфата алюминия вызывают коррозию алюминия. Также соединение может разъедать металлы в присутствии влаги.
рКа
3,3 до 3,6. И его pH составляет 2,9 или более в 5% водном растворе.
Для чего это (использует)
Коагуляция или флокуляция воды
-При смешивании с водой (пригодной для питья, подачи или отходов) сульфат алюминия вызывает образование гидроксида алюминия, который образует комплексы с соединениями и частицами в растворе, ускоряя их осаждение, что в отсутствие обработки сульфатом алюминия может привести к долгое время.
-Сульфат алюминия также используется при очистке воды в бассейне, что делает его более привлекательным для использования.
-Благодаря использованию сульфата алюминия вода получается без мутности и цвета, что повышает ее способность к обработке за счет облегчения очистки воды. К сожалению, этот метод очистки может привести к незначительному увеличению концентрации алюминия в воде..
-Алюминий является очень токсичным металлом, который накапливается в коже, мозге и легких, вызывая серьезные нарушения. Кроме того, неизвестно, какую функцию он выполняет в живых существах..
-Европейский Союз требует, чтобы максимально допустимый предел содержания алюминия в воде не превышал 0,2 мг / л. Между тем, Агентство по охране окружающей среды США требует, чтобы максимальный предел загрязнения воды алюминием не превышал 0,05-0,2 мг / л..
-Очистка сточных вод или использование сульфата алюминия позволяет экономно удалять или уменьшать содержание фосфора в них..
Использование в качестве протравы чернил и при разработке бумаги
-Сульфат алюминия использовался в качестве протравы для красителей или чернил, помогая закрепиться на красящем материале. Его фиксирующее действие обусловлено Al (OH)3, чья желатиновая консистенция способствует адсорбции красителей на текстиле.
-Хотя он использовался примерно с 2000 г. до н.э. для описанной цели, только органические красители требуют морилки. Синтетические красители, с другой стороны, не требуют протравы для выполнения своей функции.
-Это было вытеснено из производства бумаги, но это все еще используется в производстве бумажной массы. Удаляет примеси, а также используется для связывания материалов, нейтрализации зарядов и калибровки канифоли.
Промышленное использование
-Он используется в строительной промышленности для ускорения схватывания бетона. Кроме того, он используется в гидроизоляции зданий.
-В производстве мыла и жиров он используется в производстве глицерина.
-Он используется в нефтяной промышленности при производстве синтетических катализаторов, которые используются во время эксплуатации.
-Он используется в фармацевтической промышленности в качестве вяжущего при приготовлении лекарств и косметики.
-Вмешивается в производство красителей, таких как кармин. Он также используется в качестве красителя при производстве синтетических каучуков бутадиен-стирола..
-В сахарной промышленности его используют в качестве очистителя мелассы для сахарного тростника..
-Используется при изготовлении дезодорантов. Почему? Потому что это вызывает сужение протоков потовых желез, ограничивая тем самым накопление пота, необходимой среды для роста бактерий, вызывающих запах.
-Используется при дублении кожи, необходим процесс его использования. Кроме того, он используется в производстве удобрений.
-Используется в качестве добавки при приготовлении красок, адгезивов и герметиков, а также в средствах для чистки и ухода за мебелью..
Лечебное и терапевтическое использование
-Сульфат алюминия является иммунологическим адъювантом. Следовательно, он выполняет функцию обработки антигенов таким образом, что при высвобождении в месте их действия они производят большую продукцию антител к антигенам, которые были инокулированы..
-Адъювант Фрейнда и БЦЖ, а также другие адъюванты, в том числе эндогенные, такие как интерлейкины, неспецифичны для антигенов, что позволяет увеличить радиус действия иммунитета. Это позволило разработать вакцины против многочисленных заболеваний.
-Коагулирующее действие сульфата алюминия позволило устранить многочисленные вирусы в очищенной воде, среди прочего: Q бета, MS2, T4 и P1. Результаты показывают, что обработка воды сульфатом алюминия приводит к инактивации таких вирусов..
-Сульфат алюминия используется в форме карандаша или в виде порошка при лечении мелких поверхностных ран или ссадин, возникающих при бритье.
-Он используется в производстве ацетата алюминия, соединения, используемого при лечении некоторых заболеваний уха. Он также использовался без особого успеха для смягчения последствий укусов муравьев..
-Растворы сульфата алюминия используются в концентрации от 5 до 10% при местном лечении язв, что позволяет контролировать их секрецию.
-Вяжущее действие сульфата алюминия сокращает поверхностные слои кожи, коагулируя белки и заживляя раны.
Другое использование
-Сульфат алюминия помогает контролировать чрезмерный рост водорослей в прудах, озерах и в потоках воды. Он также используется для удаления моллюсков, в том числе испанского слизняка.
-Садовники применяют это соединение для подкисления щелочных почв. При контакте с его водой сульфат алюминия разлагается на гидроксид алюминия и разбавленную серную кислоту. Затем гидроксид алюминия выпадает в осадок, оставляя серную кислоту в растворе.
-Подкисление почв из-за серной кислоты визуализируется очень творчески, благодаря наличию растения под названием гортензия, чьи цветы становятся синими в присутствии кислой почвы; то есть они чувствительны и реагируют на изменения pH.
-Сульфат алюминия участвует в производстве пены для борьбы с огнем и борьбы с ним. Как? Реагирует с бикарбонатом натрия с выделением СО2. Этот газ блокирует доступ O2 до места сгорания материала; и, следовательно, прекращение огня, которое развивалось.
Производство сульфата алюминия
Сульфат алюминия синтезируется путем взаимодействия обогащенного алюминием соединения, такого как бокситовая руда, с серной кислотой при повышенных температурах. Следующее химическое уравнение представляет реакцию:
Сульфат алюминия также может образовываться в результате реакции нейтрализации между гидроксидом алюминия и серной кислотой в соответствии со следующей реакцией:
Серная кислота вступает в реакцию с алюминием, образуя сульфат аммония и выделяя молекулы водорода в виде газа. Реакция схематизируется следующим образом:
тип
Сульфат алюминия подразделяется на два типа: тип A и тип B. В сульфате алюминия типа A твердые вещества имеют белый цвет и имеют концентрацию железа менее 0,5%..
В сульфате алюминия типа B твердые вещества коричневые и имеют концентрацию железа менее 1,5%..
Есть отрасли, производящие сульфат алюминия, которые имеют различные критерии для их классификации. Так, промышленность сообщает, что для его приготовления сульфата алюминия типа А максимальная концентрация железа составляет 0,1% в виде оксида железа. В то время как для типа B они указывают максимальную концентрацию железа 0,35%.
токсичность
-В глазах это вызывает сильное раздражение, даже вызывает постоянные травмы..
-Вдыхание вызывает раздражение носа и горла, что может вызвать кашель и сыпь.
-Его прием вызывает раздражение желудка, тошноту и рвоту.
-Существуют токсические эффекты, которые, хотя они не связаны непосредственно с сульфатом алюминия, косвенно связаны с их использованием. Это случай определенных токсических эффектов алюминия, вызванных использованием сульфата алюминия при очистке воды..
-Пациенты, которые подвергаются хроническому диализу с использованием солей, приготовленных в очищенной воде, с использованием сульфата алюминия, испытывают очень серьезные нарушения здоровья. Среди этих нарушений у нас есть анемия, деменция при диализе и рост заболеваний костей..