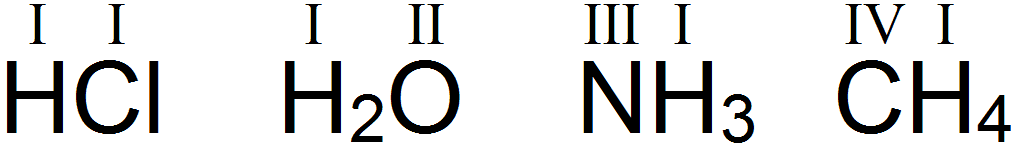§ 1.6. Валентность элементов. Структурные формулы химических соединений
В предыдущей главе, вы уже могли заметить, что атомы, группируясь друг с другом, не обязательно образуют двухатомные молекулы, т.е. соединяются в соотношении один к одному. В молекуле воды, например, к одному атома кислорода прикрепляется два атома водорода. Количество связей, которые атом химического элемента образует с другими атомами, называется его валентностью.
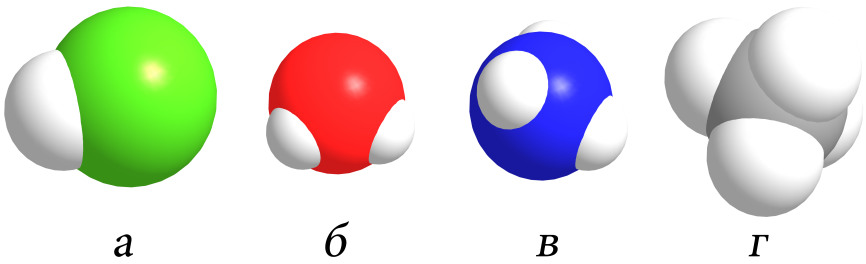
Если схематично изобразить строение этих молекул, обозначая атомы химических элементов соответствующими им символами, а связь между ними отрезком,
получаются формулы следующего вида, называемые структурными:
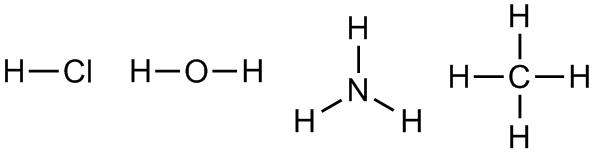
Валентность химических элементов в соединениях принято указывать надстрочным индексом справа от символа химического элемента, либо над ним, как, например, это сделано ниже:
Для некоторых элементов характерна постоянная валентность, то есть в соединениях их валентность равна всегда одному и тому же числу.
Так, например, постоянная валентность, равная единице, наблюдается для ряда металлов, называемых щелочными — лития, натрия, калия, рубидия и цезия, Постоянная валентность, равная двум, наблюдается у кислорода, магния, кальция, стронция, бария, цинка. Постоянная валентность равная трем наблюдается у алюминия Al.
Элементы с переменной валентностью — это элементы, которые в разных соединениях могут иметь различные значения валентности. Следовательно, атомы этих элементов в разных соединениях могут образовывать различное число химических связей (таблица 2).
Таблица 2. Наиболее характерные значения валентности некоторых элементов
Химические формулы для «чайников»
Я думаю, что знакомство с формулами лучше всего начать со структурных формул органических веществ. Считается, что они сложны для понимания, поэтому в школе их изучают в выпускных классах. Но я уверен, что через 10 минут вы разберетесь, как легко составлять структурные формулы.
Но в химии приняты не только структурные формулы. И здесь мы познакомимся с некоторыми из них. Достаточно распространены так называемые истинные формулы. Для метана истинная формула записывается так:
Углеводороды
Двойные и тройные связи
Итак, за короткое время мы уже разобрались, что такое структурные формулы и выяснили, что они бывают развёрнутые и упрощённые. Но пока что мы познакомились только с одинарными химическими связями. Но на самом деле существуют двойные и даже тройные связи. Посмотрим на следующую таблицу.
Циклические углеводороды
Продолжим знакомство с формулами углеводородов. Они ещё не раскрыли нам всех своих секретов. Оказывается, что цепочки могут быть замкнутыми. То есть, атомы углерода соединяются друг с другом циклически.
| Вещество | Развёрнутая формула | Упрощённая формула | Брутто-формула |
|---|---|---|---|
| Циклопропан | $slope(60)H`/C`/C:a`/H; H\#C\C:b\H; H-#a-#b-H | H2C_(x1.4)CH2_q3CH2_q3 | |
| Циклобутан | H|C|C|H; H|C|C|H; H-#2-#6-H; H-#3-#7-H | H2C-CH2`|CH2`-H2C_#1 | |
| Циклопентан | C_(x1.1)C@:H2() @()_qC@H2()_qC@H2()_qC@H2()_q@H2() | H2C_(x1.4)CH2_qCH2_qCH2_qH2C_q | |
| Циклогексан | C\C@:H2() @()|C@H2()`/C@H2()`\C@H2()`|C@H2()/@H2() | $L(1.3)CH2\CH2|CH2`/CH2`\H2C`|H2C/ |
Изомеры
До сих пор мы не особенно обращали внимания на последнюю колонку, где выведены брутто-формулы. Но может возникнуть вполне законный вопрос: зачем вообще нужны структурные формулы? Ведь брутто-формулы гораздо проще записывать. Может быть, достаточно было бы пользоваться только ими?
Но оказывается, что без структурных формул обойтись не получится. Например, если сравнить брутто-формулы из двух предыдущих таблиц, то мы увидим, что циклопропан имеет абсолютно тот же состав, что и пропен ( C3H6 ). А брутто-формула циклобутана совпадает с бутеном ( C4H8 ). Но это разные вещества! И разница заключается в структуре. То есть, имеет большое значение, в каком порядке элементы соединены друг с другом. А значит, именно структурные формулы позволяют точно описать нужное вещество.
В химии существует такое понятие как изомеры. Так называют разные вещества, которые имеют одинаковый состав. Это не редкость. И в этом нет ничего странного. Ведь бывают же совершенно разные слова, состоящие из одинаковых букв.
Классическими изомерами среди углеводородов можно назвать бутан и изобутан. Посмотрим на их формулы:
Изобутан является изомером бутана. Обратите внимание, что брутто-формулы одинаковы. Но хотя они близки по свойствам, это разные вещества.
Как видно, разнообразие углеводородов не перестаёт удивлять. Оказывается, они могут состоять не только из линейных цепочек, но могут образовывать разветвлённые структуры. И чем длиннее исходная цепочка, тем больше вариантов. Если у бутана возможны только два изомера, то у пентана их уже три:
Обратите внимание, что научное название зависит от числа звеньев в прямой цепочке, а традиционное название просто учитывает количество атомов углерода в молекуле. Так получилось из-за того, что химики, которые только начинали исследовать углеводороды, первым делом научились определять состав веществ. То есть, сначала люди смогли получить лишь брутто-формулы. А из них невозможно понять, какова длина самой длинной цепочки. Поэтому названия учитывали общее число атомов углерода.
Затем наука дошла до того, что люди смогли исследовать структуру молекул, придумали структурные формулы и переименовали уже известные вещества в соответствии с новыми знаниями. Но старые названия уже успели прижиться и существуют до сих пор.
Бензол и скелетные формулы
Думаю, что пора познакомиться ещё с одним весьма примечательным представителем углеводородов. Это вещество называется бензол. Вот его формулы:
| Развёрнутая формула | Упрощённая формула | Скелетная формула | Брутто-формула |
|---|---|---|---|
| H|C\C|C `//C `\C `||C /\/H | H_(y.5)C\\CH|CH`//C `\HC`||HC/ | \\|`//`\`||/ |
Давайте посмотрим, как выглядят формулы других веществ, производных от бензола.
| Вещество | Развёрнутая формула | Скелетная формула | Смешанный вариант | Брутто-формула |
|---|---|---|---|---|
| Нафталин | C/C \\C |C `//C `\C`|`\\C `/C ||C \C/`/|H | /\\|`//`\`|`\\`/||\// | C10H8 | |
| Толуол | H|C|C\C|C `//C `\C `||C /\/H; H-#2-H | |\\|`//`\`||/ | CH3|\\|`//`\`||/ | |
| Кумол | H\C\C/C/H; H|#2|H; H|#4|H; H|#3|C\C|C `//C `\C `||C /\/H | \ |\\|`//`\`||/ | H3C\ |\\|`//`\`||/ |
Как видите, появился ещё и смешанный вариант. Опять какой-то новый вид формул? На этот раз уже нет. Просто иногда внутри одной формулы удобно сочетать различные способы.
А вот скелетная формула углеводорода, который называется коронен. Причём, другие варианты здесь уже использовать нет смысла.
| Бутан | Бутен | Изобутан | Гексан |
| /\/ | //\/ | \|`|0/ | /\/\/ |
Трехмерные изображения
Иногда плоского изображения становится недостаточно. Поэтому для изображения трехмерных структурных формул используют особое изображение для химических связей:
Формулы с окружностью
Само собой, все они означают одно и то же. Но первые три отличаются только поворотом вокруг собственного центра. Тут нет ничего необычного, ведь молекулы не стоят на одном месте. А вот дальше мы видим кружок вместо трёх двойных связей. Причём, я намеренно изобразил все атомы водорода в последней формуле. Чтобы было хорошо видно, что каждый угол фактически лишился одной чёрточки. Их заменил кружок. Он как бы означает, что все двойные связи равномерно распределены внутри кольца.
Формулы бензола, где используется чередование одинарных и двойных связей называются формулами Кекуле в честь немецкого учёного, который внёс значительный вклад в исследование структуры бензола.
На самом деле, среди химиков нет единого мнения по поводу того, насколько правильно использование формул с кружком. Некоторые авторы категорически против. Но есть масса публикаций, где такая запись широко употребляется. Моя задача состоит в том, чтобы Вы узнали о существовании подобных формул и не удивлялись, увидев их.
Вот пара примеров записи уже для уже знакомых нам веществ:
| Нафталин: | /\|`/`\`|_o`\`/|\/_o | Толуол: | `/`-`\/-\_o-CH3 |
Знакомство с кислородом. Спирты
Ещё здесь из четырёх спиртов есть два изомера: 1-пропанол и 2-пропанол. У них одинаковые брутто-формулы, хотя вещества это разные. Их молекулы отличаются номером углеродного атома, к которому крепится группа OH. Возможно, Вы спросите, почему у 1-пропанола гидроксильная группа присоединена к третьему, а не к первому атому углерода? Тут следует вспомнить, что молекулы не находятся в одном положении. Они постоянно крутятся. И вполне могут развернуться как угодно:
Карбоновые кислоты
Отличительной особенностью органических кислот является наличие карбоксильной группы (COOH), которая и придаёт таким веществам кислотные свойства.
Карбоновые кислоты могут иметь несколько карбоксильных групп. В этом случае они называются: двухосновная, трёхосновная и т.д.
В пищевых продуктах содержится немало других органических кислот. Вот только некоторые из них:
| Щавелевая кислота | Молочная кислота | Яблочная кислота | Лимонная кислота |
| HOOC-COOH | H3C\ /COOH | HOOC\/ \COOH | HOOC\/ \/COOH |
| двухосновная карбоновая кислота | оксикарбоновая кислота | Двухосновная оксикарбоновая кислота | Трёхосновная оксикарбоновая кислота |
Название этих кислот соответствует тем пищевым продуктам, в которых они содержатся. Кстати, обратите внимание, что здесь встречаются кислоты, имеющие и гидроксильную группу, характерную для спиртов. Такие вещества называются оксикарбоновыми кислотами (или оксикислотами).
Внизу под каждой из кислот подписано, уточняющее название той группы органических веществ, к которой она относится.
Радикалы
Если выражаться более определённо, то одновалентным радикалом называется часть молекулы, лишённая одного атома водорода. Ну а если отнять два атома водорода, то получится двухвалентный радикал.
Радикалы в химии получили собственные названия. Некоторые из них получили даже латинские обозначения, похожие на обозначения элементов. И кроме того, иногда в формулах радикалы могут быть указаны в сокращённом виде, больше напоминающем брутто-формулы.
Всё это демонстрируется в следующей таблице.
| Название | Структурная формула | Обозначение | Краткая формула | Пример спирта | ||
|---|---|---|---|---|---|---|
| Метил | CH3-<> | Me | CH3 | CH3OH | ||
| Этил | CH3-CH2-<> | Et | C2H5 | C2H5OH | ||
| Пропил | CH3-CH2-CH2-<> | Pr | C3H7 | C3H7OH | ||
| Изопропил | H3C\CH(*`/H3C*)-<> | i-Pr | C3H7 | (CH3)2CHOH | ||
| Фенил | `/`=`\//-\\-<> | Ph | C6H5 | C6H5OH | ||
Существует ещё такое явление, как свободные радикалы. Это радикалы, которые по каким-то причинам отделились от функциональных групп. При этом нарушается одно из тех правил, с которых мы начали изучение формул: число химических связей уже не соответствует валентности одного из атомов. Ну или можно сказать, что одна из связей становится незакрытой с одного конца. Обычно свободные радикалы живут короткое время, ведь молекулы стремятся вернуться в стабильное состояние.
Знакомство с азотом. Амины
Предлагаю познакомиться с ещё одним элементом, который входит в состав многих органических соединений. Это азот.
Он обозначается латинской буквой N и имеет валентность, равную трём.
В общем, никаких особых новшеств здесь нет. Если эти формулы Вам понятны, то можете смело заниматься дальнейшим изучением органической химии, используя какой-нибудь учебник или интернет.
Но мне бы хотелось ещё рассказать о формулах в неорганической химии. Вы убедитесь, как их легко будет понять после изучения строения органических молекул.
Рациональные формулы
Не следует делать вывод о том, что неорганическая химия проще, чем органическая. Конечно, неорганические молекулы обычно выглядят гораздо проще, потому что они не склонны к образованию таких сложных структур, как углеводороды. Но зато приходится изучать более сотни элементов, входящих в состав таблицы Менделеева. А элементы эти имеют склонность объединяться по химическим свойствам, но с многочисленными исключениями.
| Вещество | Структурная формула | Рациональная формула | Брутто-формула |
|---|---|---|---|
| Оксид кальция | Ca=O | CaO | |
| Гидроксид кальция | H-O-Ca-O-H | Ca(OH)2 | |
| Карбонат кальция | $slope(45)Ca`/O\C|O`|/O`\#1 | CaCO3 | |
| Гидрокарбонат кальция | HO/`|O|\O/Ca\O/`|O|\OH | Ca(HCO3)2 | |
| Угольная кислота | H|O\C|O`|/O`|H | H2CO3 |
При первом взгляде можно заметить, что рациональная формула является чем то средним между структурной и брутто-формулой. Но пока что не очень понятно, как они получаются. Чтобы понять смысл этих формул, нужно рассмотреть химические реакции, в которых участвуют вещества.
Но и гидроксид кальция не встречается в природе из-за наличия в воздухе углекислого газа. Думаю, что все слыхали про этот газ. Он образуется при дыхании людей и животных, сгорании угля и нефтепродуктов, при пожарах и извержениях вулканов. Поэтому он всегда присутствует в воздухе. Но ещё он довольно хорошо растворяется в воде, образуя угольную кислоту:
Таким образом, гидроксид кальция, растворённый в воде, вступает в реакцию с угольной кислотой и превращается в малорастворимый карбонат кальция:
Из карбоната кальция в значительной степени состоят мел, известняк, мрамор, туф и многие другие минералы. Так же он входит в состав кораллов, раковин моллюсков, костей животных и т.д.
Но если карбонат кальция раскалить на очень сильном огне, то он превратится в оксид кальция и углекислый газ.
Думаю, что пора знакомиться с ионами. Это слово наверняка всем знакомо. А после изучения функциональных групп, нам ничего не стоит разобраться, что же представляют собой эти ионы.
Вы наверное уже догадываетесь, что ионы можно описывать не только рациональными формулами. Вот скелетная формула гидрокарбонат-аниона:
Система Хилла
Немного о системе easyChem
Вместо заключения мне хотелось бы рассказать о системе easyChem. Она разработана для того, чтобы все те формулы, которые мы тут обсуждали, можно было легко вставить в текст. Собственно, все формулы в этой статье нарисованы при помощи easyChem.
Выглядит конечно не очень красиво, но тоже осуществимо.
Система easyChem позволяет хранить все формулы прямо в HTML-документе в текстовом виде. По-моему, это очень удобно.
Кроме того, брутто-формулы в этой статье вычисляются автоматически. Потому что easyChem работает в два этапа: сначала текстовое описание преобразуется в информационную структуру (граф), а затем с этой структурой можно выполнять различные действия. Среди них можно отметить следующие функции: вычисление молекулярной массы, преобразование в брутто-формулу, проверка на возможность вывода в виде текста, графическая и текстовая отрисовка.
Вот несколько примеров, раскрывающих секрет подготовки текста статьи:
| Текстовое описание easyChem | Выводимый результат | Сгенерированная брутто-формула |
|---|---|---|
| (NH4)2CO3 | (NH4)2CO3 | |
| H-C-C-O-H; H|#2|H; H|#3|H | H-C-C-O-H; H|#2|H; H|#3|H | |
| CH3|\\|`//`\`||/ | CH3|\\|`//`\`||/ |
Описания из левого столбца автоматически превращаются в формулы во втором столбце.
В первой строчке описание рациональной формулы очень похоже на отображаемый результат. Разница только в том, что числовые коэффициенты выводятся подстрочником.
Во второй строке развёрнутая формула задана в виде трёх отдельных цепочек, разделённых символом ; Я думаю, нетрудно заметить, что текстовое описание во многом напоминает те действия, которые потребовались бы для изображения формулы карандашом на бумаге.
В третьей строке демонстрируется использование наклонных линий при помощи символов \ и /. Значок ` (обратный апостроф) означает, что линия проводится справа налево (или снизу вверх).
Здесь есть гораздо более подробная документация по использованию системы easyChem.
На этом разрешите закончить статью и пожелать удачи в изучении химии.
Структурные формулы и названия
предельных углеводородов
Три разновидности структурных формул
1. Самая полная форма записи формулы углеводорода – это когда каждый атом молекулы показан отдельно:
Такая запись громоздкая, занимает много места и используется редко.
2. Форма записи, в которой указывают общее число атомов водорода при каждом атоме С, а между соседними углеродами ставят черточки,
означающие х……… с…. :
3. Структурная формула, в которой черточки между атомами, расположенными в записи на одной строке, не указывают, тогда как атомы, выходящие на другие строки, соединяют черточками с прямой цепью:
Иногда углеродные цепи изображают ломаными линиями, геометрическими фигурами (треугольник, квадрат, куб). При этом в каждом изломе цепи, а также в начале и в конце цепи подразумевают атом С. Например, изображениям
соответствуют структурные формулы
Ниже приведены некоторые свойства отдельных предельных углеводородов и формы их записи (табл. 1).
Названия предельных углеводородов (алканов) линейного строения
| Название алкана | Молекулярная формула | Структурная формула | Агрегатное состояние | Температура кипения, °С |
|---|---|---|---|---|
| Метан | СН4 | СН4 | Газ | –161,6 |
| Этан | С2Н6 | СН3СН3 | Газ | –88,6 |
| Пропан | С3Н8 | СН3СН2СН3 | Газ | –42,1 |
| Бутан | С4Н10 | СН3СН2СН2СН3 | Газ | –0,5 |
| Пентан | С5Н12 | СН3(СН2)3СН3 | Жидкость | 36,1 |
| Гексан | С6Н14 | СН3(СН2)4СН3 | Жидкость | 68,7 |
| Гептан | С7Н16 | СН3(СН2)5СН3 | Жидкость | 98,5 |
| Октан | С8Н18 | СН3(СН2)6СН3 | Жидкость | 125,6 |
| Нонан | С9Н20 | СН3(СН2)7СН3 | Жидкость | 150,7 |
| Декан | С10Н22 | СН3(СН2)8СН3 | Жидкость | 174,0 |
Составление названий разветвленных и замещенных алканов
1. Выбирают главную углеродную цепь и нумеруют ее таким образом (слева или справа), чтобы входящие заместители получили наименьшие номера.
2. Название начинают с цифрового локанта – номера углерода, при котором находится заместитель. После цифры через черточку пишут название заместителя. Разные заместители указывают последовательно. Если одинаковые заместители повторяются два раза, то в названии после цифровых локантов, указывающих положение этих заместителей, пишут приставку «ди». Соответственно при трех одинаковых заместителях приставка «три», при четырех – «тетра», при пяти заместителях – «пента» и т. д.
Названия заместителей
| СН3– | С2Н5– | СН3СН2СН2– |  | Сl– | F– | Br– | –NO2 |
| метил | этил | пропил | изопропил | хлор | фтор | бром | нитро |
3. Слитно с приставкой и заместителем пишут название углеводорода, пронумерованного в качестве главной углеродной цепи:
а) 2-метилбутан; б) 2,3-диметилпентан; в) 2-хлор-4-метилпентан.
Названия циклоалканов составляют аналогично, только к названию углеводорода – по числу атомов углерода в цикле – добавляют приставку «цикло»:
Элемент сходства – алканы с линейной цепью:
Cходство трех формул веществ последнего примера – в каждом случае при втором атоме С главной углеродной цепи находится одинаковый заместитель – группа СН3.
Примеры изомерных углеводородов
| Молекулярная формула | Структурные формулы |
|---|---|
| С4Н10 | СН3СН2СН2СН3,  |
| С5Н12 | СН3СН2СН2СН2СН3,  |
| С6Н14 | СН3(СН2)4СН3,  |
 |