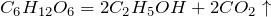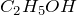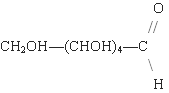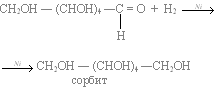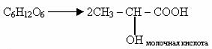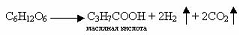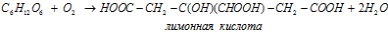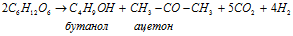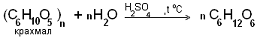Формула глюкозы
Химическая формула глюкозы
Глюкоза – бифункциональное соединение, поскольку содержит пять гидроксильных и одну альдегидную группу, т.е. является многоатомным альдегидоспиртом.
Относится к классу углеводов с общей формулой Сn(Н2О)m.
Структурная и сокращенная формула глюкозы
Структурная формула глюкозы:
Сокращенная формула глюкозы:
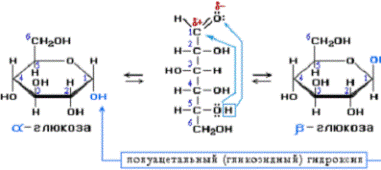
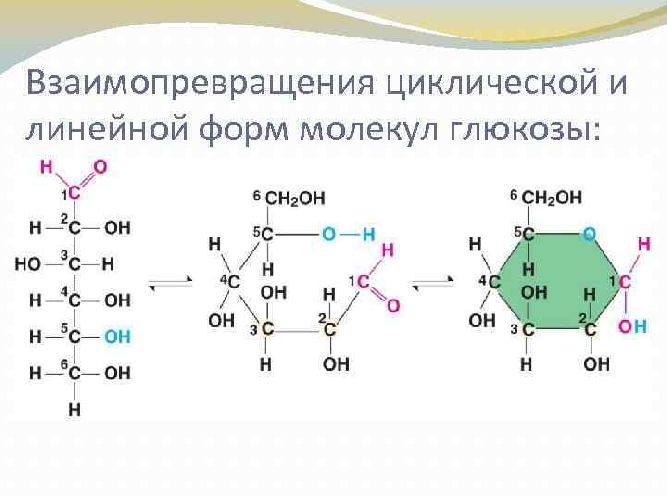
Молекула глюкозы может существовать в нескольких изомерных формах, одна из них линейная, а две – циклические.
В растворе все эти формы находятся в динамическом равновесии:
Циклические 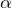
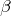
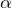
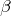
Пространственное строение циклических изомеров:
В кристаллическом состоянии глюкоза находится в состоянии 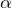
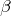
Для глюкозы характерна оптическая изомерия. Формулы оптических изомеров:
В природе встречается только D- изомер глюкозы.
Межклассовый изомер глюкозы, также имеющий формулу C6H12O6 – фруктоза (кетоноспирт):
Примеры решения задач
| Задание | Вычислите, будут ли изотоническими растворы, содержащие при одной и той же температуре 0,25 моль/л сахарозы С 12Н22О11 и 45 г/л глюкозы C6H12O6. |
| Решение | По определению, изотонические растворы — растворы, имеющие одинаковое осмотическое давление. |
Осмотическое давление выражается формулой:
где 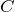
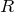
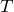
Рассчитаем молярную концентрацию раствора глюкозы:

Таким образом, концентрации растворов сахарозы и глюкозы одинаковы:

температура растворов одна и та же, следовательно, растворы будут изотоническими.
| Задание | В результате реакции спиртового брожения виноградного сахара, содержащего 20% несахаристых примесей, выделилось 138г спирта. Какое количество виноградного сахара вступило в реакцию брожения? Какой объем углекислого газа выделился в результате реакции? |
| Решение | Виноградный сахар – это глюкоза. Формула глюкозы С6H12O6. |
Запишем уравнение реакции спиртового брожения для виноградного сахара:
В результате реакции образуется этиловый спирт и выделяется углекислый газ.
Молярные массы этанола и глюкозы равны:
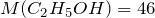
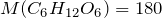
Для нахождения массы виноградного сахара, вступившего в реакцию спиртового брожения, составим пропорцию исходя из уравнения реакции:
180 г 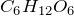
х г 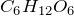
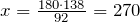
Таким образом, в реакцию спиртового брожениявступило 270 г чистого виноградного сахара.
Так как, виноградный сахар содержит 20% несахаристых примесей, то его содержание будет равно 100% – 20% = 80%.
Рассчитаем массу образца виноградного сахара по формуле:
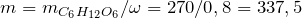
Рассчитаем объем углекислого газа (CO2), составив пропорцию по уравнению реакции:
при образовании 92 г C2H5OH выделяется 44,8 л CO2
при образовании 138 г C2H5OH выделяется у л CO2
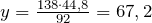
Следовательно, в результате брожения выделилось 67,2 л углекислого газа.
Глюкоза

Всего получено оценок: 470.
Всего получено оценок: 470.
Органическое кислородсодержащее соединение с шестью атомами углерода называется глюкозой, виноградным сахаром, декстрозой или гексозой. Это универсальный источник энергии среди всех живых организмов планеты. Формула вещества – C6H12O6.
Строение
Вещество глюкоза в химии – это моносахарид, то есть простейший углевод, состоящий из одной молекулы или одной структурной единицы. Глюкозная структурная единица входит в состав более сложный углеводов – дисахаридов и полисахаридов.
Вещество включает функциональные группы:
Молекула может существовать в виде двух циклов (α и β), отличающихся пространственным расположением одной гидроксильной группы, и в линейной форме (D-глюкоза).
Структурная формула глюкозы – O=CH-CHOH-CHOH-CHOH-CHOH-CH2OH или CH2OH(CHOH)4-COH.
Получение
Большое количество виноградного сахара находится в растительности, в частности плодах и листьях. Поэтому вещество можно потреблять непосредственно из фруктов и ягод. Глюкоза – конечный продукт фотосинтеза:
В промышленности соединение выделяют путём гидролиза полисахаридов. Начальными продуктами являются картофельный или зерновой крахмал, а также целлюлоза. В разбавленное водой сырьё добавляют горячий раствор серной или соляной кислоты. Полученную смесь нагревают до полного распада полисахаридов:
Кислоту нейтрализуют мелом или фарфором, после чего раствор фильтруют и выпаривают. Образовавшиеся кристаллы – глюкоза.
В лабораториях декстрозу выделяют из формальдегида в присутствии катализатора – Ca(OH)2:
В пищеварительном тракте полисахариды, полученные с пищей, быстро расщепляются на фруктозу и глюкозу, которые участвуют в клеточном метаболизме.
Физические свойства
Гексоза – это кристаллическое бесцветное вещество, не имеющее запаха, но обладающее сладким вкусом. Однако сахароза (привычный сахар) в два раза слаще глюкозы.
Вещество хорошо растворимо не только в воде, но и других растворителях – аммиачном растворе гидроксида меди (реактив Швейцера), серной кислоте, хлориде цинка.
Химические свойства
Реакция
Описание
Уравнение
Распадается под действием ферментов, выделяемых бактериями, грибками, дрожжами. Существует три типа в зависимости от природы фермента: спиртовое, маслянокислое, молочнокислое брожение
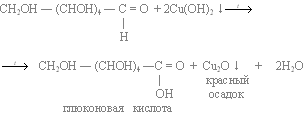
Качественная реакция с аммиачным раствором оксида серебра (I) с образованием глюконовой кислоты
Окисление азотной кислотой
Глюкоза окисляется до сахарной (глюкаровой) кислоты
Окисление гидроксидом меди (II)
Голубой гидроксид меди (II) превращается в красный оксид меди (I). Образуется глюконовая кислота
Реакция с водородом в присутствии катализатора (никеля) при высокой температуре. Образуется шестиатомный спирт (сорбит)
Глюкоза используется в медицине, пищевой, текстильной промышленности. Вещество присутствует во всех пищевых продуктах, используется для получения пива, вина, молочнокислых продуктов.
Что мы узнали?
Строение глюкозы как многоатомного альдегидоспирта
Строение глюкозы
Структурная формула глюкозы имеет вид: 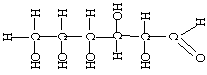
Сокращённая формула имеет вид:
Молекула глюкозы может существовать в трех изомерных формах, причем две из них являются циклическими, одна – линейной.
Химические свойства глюкозы:
Свойства, обусловленные наличием альдегидной группы:
2.Реакция восстановления:
c водородом H2:
В этой реакции может принимать участие лишь линейная форма глюкозы.
Свойства обусловленные наличием нескольких гидроксильных групп (ОН):
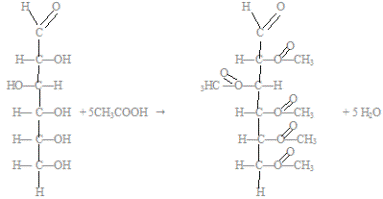
1. Реагирует с карбоновыми кислотами с образованием сложных эфиров (пять гидроксильных групп глюкозы вступают в реакцию с кислотами):
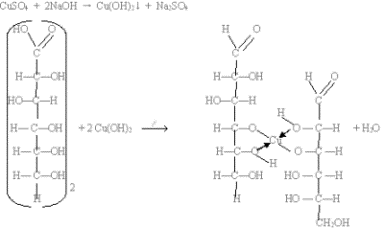
2. Как многоатомный спирт реагирует с гидроксидом меди (II) c образованием алкоголята меди (II):
Специфические свойства глюкозы
Большое значение имеют процессы брожения глюкозы, происходящие под действием органических катализаторов-ферментов (они вырабатываются микроорганизмами).
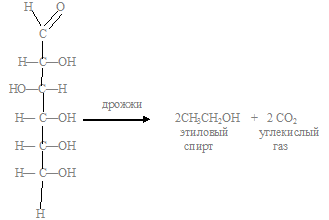
а) спиртовое брожение (под действием дрожжей):
б) молочнокислое брожение (под действием молочнокислых бактерий):
в) уксуснокислое брожение:
г) лимоннокислое брожение:
д) ацетон-бутанольное брожение:
Получение глюкозы
1.Синтез глюкозы из формальдегида в присутствии гидроксида кальция (ре-акция Бутлерова):
2. Гидролиз крахмала (реакция Киргофа):
Биологическое значение глюкозы, её применение
Глюкоза, свойства, получение и применение
Глюкоза, свойства, получение и применение.
Глюкоза – один из самых распространённых углеводов и источников энергии в живых организмах на планете, имеющий формулу C6H12O6.
Глюкоза, формула, молекула, строение, изомерия, вещество:
Глюкоза (виноградный сахар, декстроза или D-глюкоза) – органическое соединение, естественный моносахарид (шестиатомный гидроксиальдегид, гексоза), имеющий формулу C6H12O6.
Глюкоза (от греч. γλυκύς – «сладкий» и суффикса «оза») – один из самых распространённых углеводов и источников энергии в живых организмах на планете.
В быту глюкоза именуется также виноградным сахаром по причине того, что она содержится в винограде и впервые в 1747 году её получил немецкий химик Андреас Маргграф из виноградного сока. Глюкоза также встречается в листьях и других частях растений, соке многих фруктов, овощей и ягод: вишне, черешне, тыкве, малине, сливе, арбузах, яблоках, груше, дыне, персиках, мандаринах, землянике, томатах, капусте, смородине, свекле, финиках, картофеле, крыжовнике, абрикосах, огурцах, клюкве, апельсинах и пр., а также в мёде. Мед в основном состоит из смеси глюкозы с фруктозой. Кроме того, она (глюкоза) содержится во многих бобовых и злаках: пшенице, рисе, овсе, кукурузе, гречке и пр.
Глюкоза – это моносахарид, т.е. простейший углевод, состоящий из одной молекулы или одной структурной единицы.
Химическая формула глюкозы C6H12O6.
Глюкоза принадлежит к классу альдогексоз, то есть является полигидроксиальдегидом.
Глюкоза представляет собой моносахарид, содержащий шесть атомов углерода, одну альдегидную (-CHO) и пять гидроксильных (-OH) групп.
Молекула глюкозы может существовать:
– в виде двух пиранозных циклических форм (α-D-глюкоза и β-D-глюкоза, также именуемые α-D-глюкопираноза и β-D-глюкопираноза), отличающихся пространственным расположением одной гидроксильной группы. Пиранозы – моносахариды, находящиеся в циклической форме и содержащие шестичленное (пирановое) кольцо,
– в виде двух фуранозных циклических форм (α-D-глюкофураноза и β-D-глюкофураноза), отличающихся пространственным расположением одной гидроксильной группы. Фуранозы – моносахариды, находящиеся в циклической форме и содержащие пятичленное (фурановое) кольцо,
– и в виде линейной – открытой цепной (ациклической) форме (D-глюкоза, также именуемая декстроза).
Циклическая форма глюкозы является результатом внутримолекулярной реакции между атомом альдегида C и гидроксильной группой C-5 линейной формы глюкозы (D-глюкозы). ОН-группа при углероде С-5 присоединяется к альдегидной группе с образованием внутримолекулярного полуацеталя. Циклические α- и β-формы глюкозы представляют собой пространственные изомеры, отличающиеся положением полуацетального гидроксила относительно плоскости кольца. В α-D-глюкозе этот гидроксил находится в транс-положении к гидроксиметильной группе –СН2ОН, в β-D-глюкозе – в цис-положении.
В циклической форме глюкоза находится в кристаллическом, твердом состоянии. Обычная кристаллическая глюкоза – это α-форма (α-D-глюкопираноза).
При растворении в воде глюкоза частично переходит в открытую цепную форму, где устанавливается состояние подвижного равновесия между указанными тремя формами. В растворе более устойчива β-форма (β-D-глюкопираноза). Линейная форма глюкозы составляет менее 0,02% молекул глюкозы в водном растворе, остальное приходится – на циклические формы. Равновесная доля α-D-глюкопиранозы при 31 °C составляет 38 %, а более устойчивой β-D-глюкопираноза – 62 %. В растворах α-D-глюкопираноза и β-D-глюкопираноза взаимопревращаются друг в друга через образование открытой цепной формы.
Наряду с наиболее распространённой в природе открытой цепной (ациклической) формой – D-глюкозой существует также её энантиомер L-глюкоза, которая в природе практически не встречается и получается искусственным путем. L-глюкоза не имеет значительного применения.
Строение молекулы глюкозы, структурная формула глюкозы:
Рис. 1. α-D-глюкопираноза
Рис. 2. β-D-глюкопираноза
Рис. 3. D-глюкоза (декстроза)
Рис. 4. D-глюкоза (слева) и L-глюкоза (справа)
Систематическое химическое наименование глюкозы: (2R,3S,4R,5R)-2,3,4,5,6-пентагидроксигексаналь (для ациклической формы – D-глюкозы). Используются также и другие химические названия глюкозы: декстроза (для ациклической формы – D-глюкозы).
Глюкоза очень хорошо растворяется в воде. Растворимость в воде составляет 32,3 г на 100 г воды (при 0 °C), 82 г/100 г (при 25 °C), 562 г/100 г (при 90,8 °C). Хорошо растворима также в аммиачном растворе гидроксида меди (реактив Швейцера), серной кислоте, хлориде цинка. Малорастворима в этаноле и метаноле.
Температура плавления α-D-глюкозы составляет 146 °C, β-D-глюкозы – 148-150 °C.
Калорийность глюкозы – 388,7 ккал на 100 г сухого вещества.
Биологическая роль глюкозы:
В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспечения метаболических процессов. Глюкоза является ценным питательным веществом. При окислении глюкозы в тканях человека и животных освобождается энергия, необходимая для нормальной жизнедеятельности организмов.
Глюкоза депонируется у человека и животных в виде гликогена, который хранится преимущественно в клетках печени (гепатоцитах) и скелетных мышцах. В крови человека также содержится порядка 5-6 г глюкозы. Уровень глюкозы в крови человека постоянен. Данного количества глюкозы достаточно для покрытия энергетических затрат организма в течение 15 минут его жизнедеятельности.
Физические свойства глюкозы:
| Наименование параметра: | Значение: |
| Цвет | белый, бесцветный |
| Запах | без запаха |
| Вкус | сладкий |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое кристаллическое вещество |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), г/см 3 | 1,562 |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), кг/м 3 | 1562 |
| Температура разложения, °C | — |
| Температура плавления α-D-глюкозы, °C | 146 |
| Температура плавления β-D-глюкозы, °C | 148–150 |
| Температура кипения, °C | — |
| Молярная масса глюкозы, г/моль | 180,16 |
Получение и производство глюкозы:
В природе глюкоза образуется в результате реакции фотосинтеза и содержится в различных частях растений: листьях и плодах. У животных глюкоза образуется в результате расщепления гликогена.
Глюкоза образуется в ходе следующих химических реакций:
1. реакции сахарозы с водой (гидролиз сахарозы):
При гидролизе (при нагревании в присутствии ионов водорода ) сахароза расщепляется на составляющие ее моносахариды – глюкозу и фруктозу за счёт разрыва гликозидных связей между ними. Данная реакция является обратной процессу образования сахарозы из моносахаридов.
2. реакции мальтозы с водой (гидролиз мальтозы):
При гидролизе (при нагревании в присутствии ионов водорода ) мальтоза расщепляется на составляющие ее моносахариды – две молекулы глюкозы за счёт разрыва гликозидных связей между ними. Данная реакция является обратной процессу образования мальтозы из моносахаридов.
Аналогичная реакция происходит в кишечнике у живых организмов при попадании в него мальтозы. В кишечнике сахароза под действием ферментов быстро гидролизуется на две молекулы глюкозы.
3. реакции крахмала с водой (гидролиз крахмала):
Важнейшее свойство крахмала – способность подвергаться гидролизу под действием ферментов или при нагревании с кислотами.
Гидролиз протекает ступенчато. Из крахмала сначала образуется декстрин ((C6H10O5)n), который гидролизуется до мальтозы (C12H22O11). Затем в результате гидролиза мальтозы образуется глюкоза (С6Н12O6).
Данная реакция используется в качестве промышленного способа получения глюкозы.
4. реакции А.М. Бутлерова – альдольной конденсации формальдегида:
Первый синтез углеводов из формальдегида в щелочной среде осуществил А.М. Бутлеров в 1861 году.
Формальдегид под действием гидроксидов щелочноземельных металлов вступает в реакцию самоконденсации, образуя при этом смесь углеводов («формозу»), в т.ч. глюкозу.
5. реакции фотосинтеза:
В природе глюкоза образуется в растениях в результате фотосинтеза из углекислого газа и воды под действием солнечного света в листьях растений. В ходе реакции помимо глюкозы образуется кислород.
6. реакции гидролиза гликогена в кислой среде:
Важнейшее свойство гликогена – способность подвергаться гидролизу в водных растворах кислот.
Гидролиз протекает ступенчато. Из гликогена ((C6H10O5)n) сначала образуется декстрин ((C6H10O5)y, при этом y Химические свойства глюкозы. Химические реакции (уравнения) глюкозы:
Основные химические реакции глюкозы следующие:
1. реакции ферментативного брожения глюкозы:
Важнейшим химическим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожение происходит в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента соответственно различают реакции следующих видов:
1.1. реакцию спиртового брожения глюкозы:
Реакция происходит под действием дрожжевых грибков.
1.2. реакцию молочнокислого брожения глюкозы:
В результате данной реакции образуется молочная кислота.
Реакция происходит под действием бактерий.
1.3. реакцию маслянокислого брожения глюкозы:
В результате данной реакции образуются масляная кислота, водород и углекислый газ.
Реакция происходит под действием бактерий.
Благодаря брожению получают продукты питания – кефир, сыр, алкоголь.
2. реакция глюкозы с водородом:
3. качественная реакция на глюкозу (реакция глюкозы с гидроксидом меди):
4. качественная реакция «серебряного зеркала» – реакция глюкозы с аммиачным раствором оксида серебра (I):
В молекуле глюкозы имеется альдегидная группа. Поэтому она при нагревании с аммиачным раствором оксида серебра окисляется и дает реакцию «серебряного зеркала».
В результате образуются глюконовая кислота и серебро, которое выпадает в осадок. Если реакция проводится в сосуде с чистыми и гладкими стенками, то серебро осаждается на них в виде тонкой плёнки, образуя зеркальную поверхность. При наличии малейших загрязнений серебро выделяется в виде серого рыхлого осадка.
Таким образом, глюкоза обладает восстанавливающими свойствами, т.к. она восстанавливает Ag2O и Cu(OH)2.
5. в организме человека глюкоза подвергается сложным биохимическим превращениям:
В результате сложных биохимических превращений образуется углекислый газ и вода, при это выделяется энергия 2800 кДж на 1 моль глюкозы.
6. глюкоза не вступает в некоторые реакции, характерные для альдегидов, например, в реакцию с гидросульфитом натрия.
Применение глюкозы:
Глюкоза используется в различных отраслях промышленности и быту:
– в медицине в качестве лечебного средства, для приготовления лечебных препаратов и пр.;
– в пищевой промышленности при выпечке хлеба, а также при производстве сгущённого молока и мороженого, в кондитерском деле при изготовлении мармелада, карамели, пряников и т.д.;
– в сельском хозяйстве в пчеловодстве для подкормки пчёл;
– в текстильной промышленности при крашении и печатании рисунков;
– в химической промышленности в качестве исходного продукта при производстве аскорбиновых и глюконовых кислот, для синтеза ряда производных сахаров и т.д.;
– в производстве зеркал и елочных игрушек (серебрение);
– в микробиологической промышленности как питательная среда для получения кормовых дрожжей;
– в приготовлении пищи и кормов для животных используются процессы молочнокислого, спиртового и маслянокислого брожения.