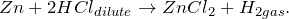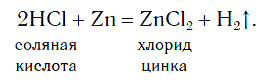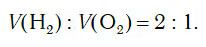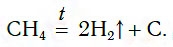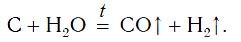Как проверить водород на чистоту
Подскажите, как проверить водород на чистоту. Перечислите последовательность действий, необходимые реактивы, химическую посуду и приборы, которые требуются для этого в лабораторных условиях.
При изучении в курсе школьной программы по химии темы «водород» в качестве лабораторной работы ученикам поручают самостоятельно получить водород, а затем проверить его на чистоту. В лабораторных условиях водород обычно получают действием цинка на соляную или серную кислоту.
Простейший лабораторный способ получения водорода это – взаимодействие разбавленной соляной или серной кислот с металлическим цинком, железом или каким-либо другим неблагородным металлом:
В штативе закрепляют пробирку, в которую предварительно налили несколько миллилитров разбавленной серной кислоты. Опускаем в неё кусочек металлического цинка и закрываем пробкой с газоотводной трубкой, конец которой помещаем в другую пробирку. Визуально будет наблюдаться выделение пузырьков газа. Это — водород. Для того, чтобы правильно собрать этот га, пробирку необходимо перевернуть вверх дном. Поскольку, водород легче воздуха, то он будет накапливаться в верхней части сосуда, однако, в ней также будет присутствовать и воздух, а значит и кислород. Известно, что эти два газа образуют друг с другом взрывоопасную смесь. Чтобы проверить полученный водород на чистоту (как проверить водород на чистоту), необходимо его поджечь с помощью тлеющей лучинки. Вы услышите хлопок. Чем звук хлопка тише, тем чище водород (меньше кислорода находится в пробирке).
Как проверить водород на чистоту
В промышленности технический водород производится согласно ГОСТ 3022-80, газообразный чистый — по ГОСТ Р 51673-2000, особо чистый по — ТУ 2114-016-78538315-2008. Для каждого из этих видов водорода и для каждой марки газа, предусмотренной указанными нормативными документами, установлены конкретные нормы на массовую долю водорода в выпускаемом газе и допустимые значения различных примесей.
Также в указанных ГОСТах и ТУ дается описание методик проведения анализа по определению объемной доли водорода и примесей в производимом продукте.
Объемная доля технического водорода в пересчете на сухой газ определяется в процентах по формуле:
X— объемная доля водорода в %;
X1— объемная доля кислорода в %;
X2— объемная доля азота в %.
Для чистого газообразного водорода объемную долю водорода определяют по формуле:
X— объемная доля водорода в %;
X1— суммарная объемная доля кислорода и аргона в %;
X2— объемная доля азота в %;
X3 — объемная доля метана в %.
Суммарная объемная доля кислорода и аргона, объемные доли азота и метана определяются хроматографическим методом, основанном на извлечении и концентрировании примесей из исследуемого газа посредством низкотемпературной адсорбции с их последующим газохроматографическим разделением и детектированием по теплопроводности. Анализируемый водород используется как газ носитель.
Объемная доля кислорода в водороде определяется колориметрическим методом, в основе которого лежит окисление кислородом, содержащимся в водороде, бесцветного медноаммиачного комплекса одновалентной меди, который при этом окрашивается в синий цвет.
Объемная доля водяных паров в водороде определяется конденсационным методом, заключающимся в измерении температуры насыщения водорода парами воды при появлении инея на холодной зеркальной поверхности.
Стандарты допускают применение других методик, при условии, что они метрологически аттестованы и суммарная погрешность результатов не превышает предусмотренных стандартом норм.
Чистота водорода, полученного методом электролиза, и наличие примеси кислорода в нем может быть определена с помощью стационарных газоанализаторов различных типов, если их погрешность не превышает допускаемую соответствующим стандартом.
В лабораторных условиях
Водород — горючий газ, а соединившись с воздухом или кислородом, образует взрывоопасную смесь. Поэтому работать с водородом нужно в маске или в очках.
Если заполненный водородом прибор требуется нагреть или же нужно поджечь выходящий из него водород, необходимо проверить водород на чистоту.

Если водород загорается с еле слышным хлопком, то он чистый. Если его загорание сопровождается резким «лающим» звуком, то газ содержит воздух и он опасен.Следует проводить пробу со второй пробиркой и т.д., пока проба не будет загораться почти без звука.
Важно! Нельзя пользоваться одной и той же пробиркой.
Проверка водорода на чистоту
Очистка водорода
Если при получении водорода используется соляная кислота, то выделяющийся газ содержит две основные примеси – хлороводород и пары воды. От них избавляются, последовательно пропуская газ из аппарата Киппа через промывную склянку с водой (поглощает HCl) и с концентрированной серной кислотой (поглощает пары воды) (рис.29).
 |
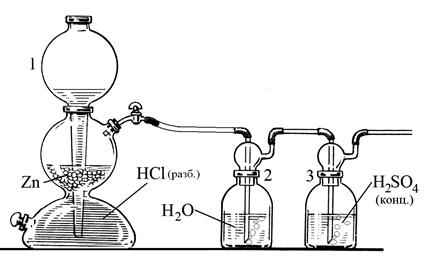 |
Смеси водорода с кислородом (2 : 1) или воздухом очень опасны. Они взрываются с большой силой при поджигании, при пропускании электрического разряда или при контакте с платиной. Поэтому водород, выделяющийся из аппарата Киппа, перед использованием всегда нужно очень тщательно проверять на чистоту следующим образом:
1. Зажечь спиртовку на расстоянии не ближе 1 м к аппарату Киппа.
2. Методом вытеснения воды заполнить пробирку выделяющимся газом и закрыть её под водой указательным пальцем.
3. Поднести закрытую пробирку отверстием вниз к пламени спиртовки, не переворачивая открыть и быстро внести в пламя. Чистый водород сгорает с лёгким, еле слышным хлопком вроде «п-па». Однако для обеспечения безопасности при работе с водородом всегда нужно окончательно убедиться в его чистоте. Водород можно использовать только после трёхкратной положительной пробы на чистоту. Если же при поджигании газа раздаётся резкий «лающий» звук, то выделяющийся газ содержит примесь воздуха и очень опасен. В этом случае нужно дождаться выделения чистого газа, периодически проводя пробу на чистоту. При этом нельзя использовать одну и ту же пробирку.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Урок 26. Получение водорода и его применение
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.
Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
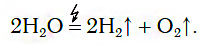
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
Существуют и другие промышленные способы получения водорода.
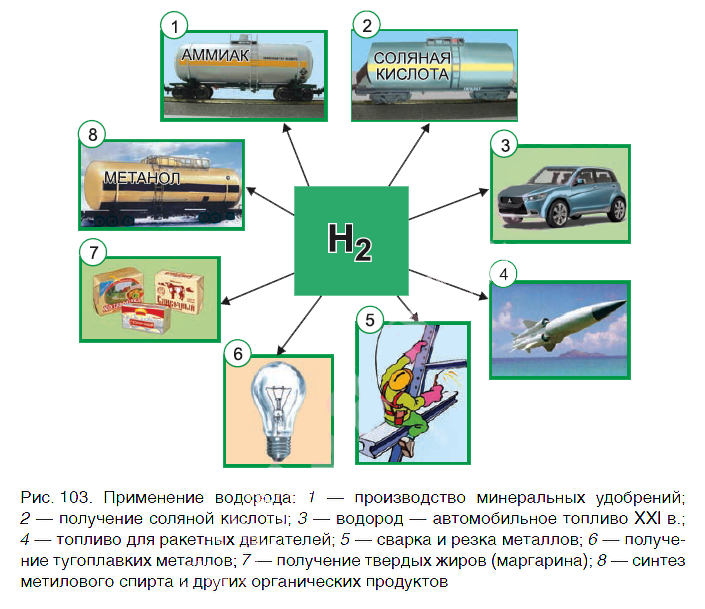
Применение водорода
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 о С. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.
В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Класс: 8
Презентации к уроку
Место урока: 8 класс. Тема II: Кислород, водород, вода как растворитель.
Тип урока: практическая работа
Задачи:
Планируемые результаты обучения:
Оборудование:
Методы и приемы:
Ход урока
(курсивом описаны действия учеников и учителя, особенности методики урока; обычным шрифтом – речь учителя)
I. Организационный момент (1 мин.)
отметить наличие халатов у всех учеников, проверить свободны ли от сумок проходы, убраны ли волосы у девочек. На столах оставить только ручки, калькуляторы и тетради.
II. Активизация знаний, необходимых для выполнения практической работы (13 мин.)
Слайд 1:
На этом уроке мы получим водород в лабораторных условиях. Это газообразное вещество; является взрывоопасным, если загрязнено воздухом, и поэтому требует к себе повышенного внимания.
Ученики одновременно с обсуждением расписываются в журнале техники безопасности.
Слайд 2:

На предыдущем уроке была проведена подготовка учеников к данной практической работе (Презентация 1) и задано домашнее задание:
Слайд 3:
Слайд проявляется постепенно, в соответствии с беседой
Вопросы:
Слайд 4:
Слайд проявляется постепенно, в соответствии с беседой
Вопросы:
Просмотр двух видеороликов.
При проверке водорода на чистоту сжигают небольшой его объем (около 15 мл).
Возможный микровзрыв к травме привести не может.
Правило ТБ: пока нет убежденности, что газ из прибора выделяется чистый, держать отверстие газоотводной трубки подальше от пламени спиртовки.
Слайд 5:
Демонстрация результатов нарушений правил ТБ: пробирка с растресканным дном
Правило ТБ: нагревать пробирку необходимо в том месте, где находится твердое вещество, а не выше – где воздух. От неравномерного нагрева пробирка треснет.
пробирка со следами соляной кислоты в смеси с оксидом меди (II)
Правило ТБ: при зарядке автоматического прибора соляной кислотой нужно следить, чтобы не перелить кислоту (max 2 мл), иначе избыток от экзотермичности и бурного течения процесса попадет в газоотводную трубку.
III. Демонстрация эксперимента учителем (7 мин.)
Слайд 6
Слово учителя с элементами беседы
1. Взять ложкой-дозатором небольшое количество черного порошка оксида меди (II), поместить в пробирку, оставить в штативе для пробирок до проведения опыта по изучению восстановительных свойств водорода.
2. Закрепить автоматический прибор для получения газов в лапке штатива. Зарядить прибор исходными веществами: 4-5 гранул цинка поместить на резиновый кружок, через воронку прилить соляную кислоту так, чтобы ее слой над цинком был не более 2 мл. Прибор закрыть максимально герметично.
3. Для проверки газа на чистоту, мне приходится приготовить спиртовку заранее. Вы работаете вдвоем и зажжете спиртовку после того, как наберете газ в пробирку- приемник.
Правила ТБ: работа со спиртовкой
а) прежде чем зажечь спиртовку, нужно проверить плотно ли диск прилегает к отверстию резервуара (иначе искра может попасть в резервуар и весь объем спирта воспламенится)
б) зажигать только спичкой (нельзя использовать зажигалку, другую спиртовку)
в) спичку класть в лоток следует, убедившись, что она затушена (демонстрация нарушения правил ТБ – прожженный лоток)
г) чтобы погасить пламя, ее следует закрыть колпачком (задувать нельзя)
Выделяющийся водород собрать методом вытеснения воздуха, держа пробирку-приёмник вверх дном. Проверить газ на чистоту: зажать отверстие пробирки пальцем и поднести пробирку к пламени спиртовки, открыть ее.
4. Затем выделяющийся водород собрать методом вытеснения воды: набрать полную пробирку воды, перевернуть ее в кристаллизаторе и подвести к отверстию газоотводную трубку. Когда пробирка-приемник полностью заполнится водородом, зажать отверстие пальцем под водой. Убедиться в чистоте газа.
5. Закрепить пробирку с оксидом меди (II) в держателе.
Правила ТБ: закрепление пробирки в держателе
а) пробирку закрепляют в верхней третьей части ближе к отверстию
б) пробирка не должна выпадать, но проворачиваться (иначе при нагревании стекло расширяется и пробирка может лопнуть)
в) чтобы вынуть пробирку из держателя, нужно ослабить зажим.
Прогреть пробирку на пламени спиртовки 2-3 раза, далее нагревать ее в верхней части пламени, в том месте, где находится оксид меди (II). Внести газоотводную трубку с выделяющимся водородом.
После окончания опыта дать пробирке остыть, затем поставить в штатив для пробирок.
6. Потушить спиртовку, перекрыть зажимом выделение водорода.
Основное правило ТБ: работать уверенными руками!
IV. Выполнение практической работы, оформление результатов, уборка рабочего места (23 мин.)
Слайд 6
1. Ученики выполняют практическую работу самостоятельно. Учитель следит за правиль-ностью выполнения техники эксперимента и соблюдением правил ТБ.
2. Уборка рабочего места: после окончания опыта по изучению восстановительных свойств водорода:
1-й ученик: потушить спиртовку, дать пробирке-реактору остыть, затем поставить ее в штатив для пробирок.
2-й ученик: перекрыть выделение газа в автоматическом приборе, вынуть воронку, остатки цинка поместить на фильтровальную бумагу. Вынуть прибор из лапки штатива, слить отра-ботанный раствор в «СКЛЯНКУ ДЛЯ СЛИВА», сдать прибор учителю.
учитель: собирает лотки и кристаллизаторы с водой.
3. Демонстрационный опыт: изучение продукта реакции цинка с соляной киcлотой
Отработанный раствор слить в стакан и несколько капель с помощью стеклянной палочки перенести на стеклянную пластинку. Укрепить пластинку в тигельных щипцах и упарить раствор на пламени
4. Оформить результаты эксперимента: сформулировать и записать наблюдения, вывод (что узнали про газообразное вещество водород на практической работе), сдать тетрадь.
Проведение урока (Фото-фильм)
Использованные электронные пособия:
Оформление работы в тетради ученика:
Практическая работа 5: Получение водорода и изучение его свойств
1. Способ получения водорода – взаимодействие активных металлов с кислотами.
2. Приборы для получения и собирания водорода
Рис. Прибор для получения водорода – автоматический, который позволяет в любой момент остановить реакцию с помощью зажима (прибор Кирюшкина).
Собирание газа методом вытеснения воды – возможно, т.к. водород малорастворим в ней.
Рис. Собирание газа методом вытеснения воздуха – держа пробирку-приемник вверх дном, т.к.

3. Обнаружение водорода – проверка его на чистоту
4. Свойство водорода – активный восстановитель
Вывод:
Одним из способов получения водорода в лаборатории является взаимодействие цинка с разб. соляной кислотой, при этом образуется соль (хлорид цинка) и водород. Водород – бесцветный газ, без запаха, малорастворим в воде, легче воздуха, в смеси с воздухом взрывоопасен, восстанавливает металлы из их оксидов.