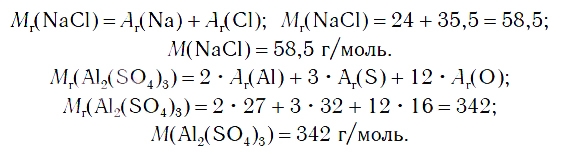Урок 25. Соли
В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.
Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4 и др. Это представители класса широко распространенных в химии соединений — солей (рис. 102).
Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4 c формулами солей ZnCl2 и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2 и FeSO4, относят к классу солей.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4 равна III.
Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
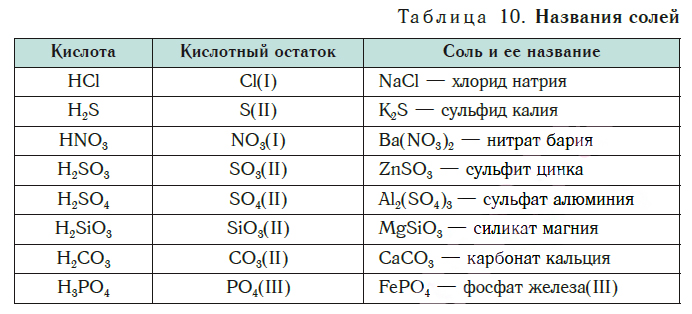
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Поваренная соль
Поваренная соль, или пищевая соль (хлорид натрия, NaCl; употребляются также названия «хлористый натрий», «столовая соль», «каменная соль», «пищевая соль» или просто «соль»), — пищевой продукт. Представляет собой бесцветные кристаллы. Соль природного (морского) происхождения практически всегда имеет примеси других минеральных солей, которые могут придавать ей оттенки разных цветов (как правило, серого или бурого). Производится в разных видах: крупного и мелкого помола, чистая, йодированная, нитритная и так далее. В зависимости от чистоты делится на сорта: экстра, высший, первый и второй.
Содержание
Биологическая роль
Соль жизненно необходима для жизнедеятельности человека, равно как всех прочих живых существ. Ион хлора в соли является основным материалом для выработки соляной кислоты — важного компонента желудочного сока. Ионы натрия вместе с ионами других элементов участвуют в передаче нервных импульсов, сокращении мышечных волокон, поэтому недостаточная их концентрация в организме приводит к общей слабости, повышенной утомляемости и другим нервно-мышечным расстройствам. При этом переизбыток натрия вызывает задержку жидкости и повышение кровяного давления.
О необходимом количестве соли в рационе существуют разные данные. Всемирная организация здравоохранения рекомендует ограничивать потребление натрия 2 граммами в день для взрослых, что соответствует 5 граммам поваренной соли. Американские медики рекомендуют ограничивать потребление соли чайной ложкой в день для здоровых людей (около 6 г), или даже меньшим количеством (менее 4 г) из расчёта, что в поваренной соли содержится примерно 40 % натрия (рекомендуемое количество может увеличиваться при занятиях, связанных с тепловым стрессом, повышенным потоотделением или некоторых болезнях). При этом следует учитывать, что в это количество входит соль в полуфабрикатах, соусах, консервах и тому подобном, а источниками натрия могут являться и другие продукты сами по себе или пищевые добавки.
Признаками нехватки соли являются головная боль и слабость, головокружение, тошнота. Улучшение самочувствия после добавления соли в пищу, а также отличные консервационные свойства соли в эпохи, когда иные методы длительного сохранения пищевых продуктов были неизвестны, породили к ней особое отношение как к самому ценному продукту.
Издревле племена охотников и скотоводов удовлетворяли потребность в соли, используя в пищу мясопродукты, иногда в сыром виде. Земледельческие же народы потребляют в основном растительную пищу, бедную хлористым натрием.
ПОВАРЕННАЯ СОЛЬ
Раньше говаривали: «Соль всему голова, без соли и жито – трава»; «Один глаз на полицу (где хлеб), другой – в солоницу (солонку)», и еще: «Без хлеба не сытно, без соли не сладко». Бурятская народная мудрость гласит: «Собираясь пить чай, клади в него щепотку соли; от нее быстрее усваивается пища, исчезнут болезни желудка».
Вряд ли мы узнаем, когда впервые наши далекие предки вкусили соль: нас отделяют от них десять-пятнадцать тысяч лет. Тогда еще не было посуды для приготовления пищи, все растительные продукты люди вымачивали в воде и подпекали на тлеющих углях, а мясо, насаженное на палки, обжаривали в пламени костра. «Поваренной солью» первобытных людей наверняка была зола, которая неизбежно попадала в пищу во время ее приготовления. Зола содержит поташ – карбонат калия K2CO3, который в местах, удаленных от морей и соленых озер, долгое время служил пищевой приправой.
Возможно, однажды, за неимением пресной воды, мясо либо корни и листья растений были замочены в соленой морской или озерной воде, и еда оказалась вкуснее обычной. Может быть, добытое впрок мясо, чтобы защитить его от хищных птиц и насекомых, люди спрятали в морскую воду, а потом обнаружили, что оно приобрело приятный вкус. Наблюдательные охотники первобытных племен могли заметить, что животные любят лизать солонцы – белые кристаллы каменной соли, выступающие кое-где из-под земли, и попробовали добавлять соль в пищу. Могли быть и другие случаи первого знакомства людей с этим удивительным веществом.
Чистая поваренная соль, или хлорид натрия NaCl – бесцветное негигроскопичное (не поглощающее влагу из воздуха) кристаллическое вещество, растворимое в воде и плавящееся при 801° С. В природе хлорид натрия встречается в виде минерала галита – каменной соли. Слово «галит» происходит от греческого «галос», означающего и «соль», и «море». Основная масса галита чаще всего находится на глубине 5 км под поверхностью земли. Однако давление слоя горных пород, расположенных над пластом соли, превращает ее в вязкую, пластичную массу. «Всплывая» в местах пониженного давления кроющих пород, пласт соли образует соляные «купола», выходящие в ряде мест наружу.
Природный галит редко бывает чисто белого цвета. Чаще он буроватый или желтоватый из-за примесей соединений железа. Встречаются, но очень редко, кристаллы галита голубого цвета. Это означает, что они долгое время в глубинах земли находились по соседству с породами, содержащими уран, и подверглись радиоактивному облучению.
При охлаждении кристалла некоторые вакансии объединяются, это и служит причиной появления синей окраски. Кстати, при растворении в воде синего кристалла соли образуется бесцветный раствор – совсем как из обычной соли.
Соль издавна была символом чистоты и дружбы. «Вы – соль земли» – говорил Христос своим ученикам, имея в виду их высокие нравственные качества. Соль употреблялась при жертвоприношениях, новорожденных детей у древних евреев посыпали солью, а в католических церквах при крещении в ротик младенца клали кристаллик соли.
В обычае арабов было при утверждении торжественных договоров подавать сосуд с солью, из которого в знак доказательства и гарантии постоянной дружбы лица, заключившие договор – «завет соли» – съедали по несколько ее крупинок. «Съесть вместе пуд соли» – у славян значит хорошо узнать друг друга и подружиться. По русскому обычаю, когда подносят гостям хлеб-соль, то тем самым желают им здоровья.
Поваренная соль – не только пищевой продукт, но издавна распространенный консервант, ее применяли при обработке кожевенного и мехового сырья. А в технике она до сих пор является исходным сырьем для получения практически всех соединений натрия, в том числе соды.
Поваренная соль входила и в состав самых древних лекарств, ей приписывали целебные свойства, очищающее и дезинфицирующее действие, причем с давних пор подмечено, что поваренная соль разных месторождений имеет разные биологические свойства: самая в этом отношении полезная – морская. В Лечебнике-травнике, изданном в России в 17 в., написано: «Две сути соли, одну копали из горы, а другую находили в море, а которая из моря, та лутчи, а кроме морской соли та лутчи, которая бела».
Однако в употреблении соли надо соблюдать меру. Известно, что средний европеец ежедневно поглощает с пищей до 15 г соли, в то время как средний японец – около 40 г. Как раз японцы и держат мировое первенство по числу больных гипертонией – болезнью, одна из причин которой состоит в том, что в организме задерживается больше жидкости, чем ему необходимо. Клетки разбухают от ее излишка, сжимают кровеносные сосуды, поэтому повышается кровяное давление, от чего и сердце начинает работать с перегрузкой. Трудно становится и почкам, очищающим организм от избытка катионов натрия.
Ни одно растение не может расти на почве, покрытой солью, солончаки всегда были символом земли бесплодной и необитаемой. Когда властитель Священной Римской империи Фридрих I Барбаросса разрушил в 1155 Милан в Италии, то велел посыпать руины поверженного города солью в знак его полного уничтожения. У разных народов во все времена рассыпать соль значило накликать беду и потерять здоровье.
В древности люди использовали несколько способов добычи поваренной соли: естественное испарение морской воды в «соляных садках», где выпадал хлорид натрия NaCl – «морская» соль, вываривание воды соленых озер с получением «выварочной» соли, и выламывание «каменной» соли в подземных рудниках. Все эти способы дают соль с примесями хлорида магния MgCl2·6 H2O, сульфатов калия K2SO4 и магния MgSO4·7H2O и бромида магния MgBr2·6H2O, содержание которых достигает 8–10 %.
В морской воде в среднем на 1 л приходится до 30 г различных солей, на долю поваренной соли приходится 24 г. Технология получения хлорида натрия NaCl из морской и озерной воды всегда была довольно примитивной.
Например, в конце «бронзового века» – за три, три с половиной тысячи лет до нашей эры – древние солевары обливали бревна морской водой, а потом сжигали их и из золы выбирали соль. Позднее соленые воды стали выпаривать на больших противнях, а для удаления примесей добавляли кровь животных, собирая образующуюся пену. Примерно с конца 16 в. растворы соли очищали и концентрировали, пропуская через башни, заполненные соломой и ветками кустарников. Выпаривание раствора соли на воздухе производили и совсем примитивным способом, сливая рассол по стене, сложенной из связок хвороста и соломы.
Солеварение, старейшее из химических ремесел, возникло на Руси, по-видимому, в начале 7 века. Соляные промыслы принадлежали монахам, которым благоволили русские цари, с них даже не взимался налог на продаваемую соль. Выварка соли приносила монастырям огромные прибыли. Рассолы добывали не только из озер, но и из подземных соляных источников; буровые скважины, которые для этого строили, в 15 в. достигали длины 60–70 м. В скважины опускали трубы, изготовленные из цельного дерева, а упаривали рассолы в железных противнях на дровяной топке. В 1780 в России таким способом было выварено более ста тысяч тонн соли…
В настоящее время поваренную соль добывают из отложений соляных озер и на месторожденияхкаменной соли – галита.
Поваренная соль – не только важная пищевая приправа, но и химическое сырье: из нее получают гидроксид натрия, соду, хлор.
Степин Б.Д., Аликберова Л.Ю. Книга по химии для домашнего чтения, 2-е изд. М., Химия, 1995
Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов / Р.А. Лидин, В.А. Молочко, Л.Л.Андреева; под ред. Р.А.Лидина. М., Химия, 1996
Аликберова Л.Ю. Занимательная химия: Книга для учащихся, учителей и родителей. М., АСТ-ПРЕСС, 1999
Степин Б.Д., Аликберова Л.Ю., Рукк Н.С. Домашняя химия. Химия в быту и на каждый день. М., РЭТ, 2001
Общие сведения
Все соли имеют сложный химический состав и в зависимости от него могут быть органическими или неорганическими. В теоретической химии существует несколько определений этой группы веществ:
Кроме металлов, к кислотным остаткам могут присоединяться ионы аммония (NH4)+, гидроксония (Н3О)+, фосфония (РН4)+ и некоторые другие. С физической точки зрения чаще всего соли — это твердые кристаллические вещества. Встречаются вещества разной окраски. Прозрачные единичные кристаллы в большом количестве имеют белый цвет, например, поваренная соль NaCl.
Их строение представляет собой кристаллическую решетку, в узлах которой находятся анионы, а катионы занимают пространство между узлами. Другое распространенное строение — анионные фрагменты из кислотных остатков, соединенные в бесконечную цепочку, в трехмерных полостях которых находятся катионы. Такую структуру имеют силикаты, что отражается и на их свойствах: высокая температура плавления и неспособность проводить электрический ток.
Кроме ионных, в молекулах солей встречаются и молекулярные ковалентные связи, и промежуточные между ковалентными и ионными. В особую группу солей выделяются так называемые ионные жидкости, температура плавления которых ниже 100 °C, отличающиеся повышенной вязкостью.
Для изучения химических и физических свойств этой группы соединений важным критерием служит их растворимость в воде: полностью, частично или нерастворимые.
Классификация и номенклатура
Основные классы этой группы веществ были описаны французским химиком и аптекарем Г. Руэлем еще в 1754 году, а по мере развития химии к ним добавились новые. Главный принцип классификации солей основан на том, что при взаимодействии металла и кислоты в ней происходит частичное или полное замещение атомов водорода.
Общие характеристики
Формулы солей всегда образуются одним или несколькими металлами, кислотными остатками и гидроксильными группами. В зависимости от этого все солевые соединения делят на такие классы:
Средними считаются те, у которых все атомы водорода образующей кислоты заменены атомами металла. К такому типу соединений относятся и те, в которых водород замещается одновалентной группой аммония NH4. Согласно принятой номенклатуре, названия этих веществ образуются из латинского названия кислотного остатка и русского названия металла. Кислородосодержащие остатки оканчиваются на «ат», бескислородные — на «ид». Например:
Если одному химическому элементу соответствует не одна кислота, то может использоваться и окончание «ит». Это относится к таким кислотам, как серная H2SO4 (сульфаты) и сернистая H2SO3 (сульфиты).
Кислые вещества образуются только от двух- или полиосновных кислот: серной, фосфорной, угольной. Они относятся к неустойчивым соединениям и при нагревании происходит их разложение на составляющие элементы. В названии таких веществ всегда используют приставку «гидро», а если незамещенных атомов водорода осталось два — приставку «ди»:
Образование основных солей происходит при частичном замещении гидроксильных групп кислотными остатками, причем валентность основного остатка всегда будет равна числу замещенных гидроксильных групп. Номенклатура названий таких химических соединений образуется в зависимости от количества гидроксогрупп приставками «гидроксо» и «дигидроксо»:
В двойных солях атомы водорода замещаются двумя разными металлами, соответственно и образовываться могут только от двух и более основных кислот: MgK (SO4)2, NaKCO3, KAl (SO4)2.
Комплексные соединения и кристаллогидраты
Этот класс химических соединений отличается большим разнообразием. В изучении комплексных солей (КС) большую роль сыграли швейцарский ученый А. Вернер и русский химик немецкого происхождения В. Освальд. КС состоят из комплексных частиц. Центральный элемент в комплексе называется комплексообразователем, а связанные с ним элементы — лигандами. Их число — это координационное число соединения. Лигандами могут быть как нейтральные молекулы, так и разнообразные ионы и катион водорода H+.
КС так и классифицируются на нейтральные, анионные и катионные. Разными лигандами образуются такие группы химических веществ:
Кристаллы, образующиеся в водном растворе при выпадении в осадок солей, называются кристаллогидратами. При этом между молекулами воды и солевыми ионами формируются прочные связи, образующие кристаллическую решетку. Химические формулы кристаллогидратов записывают в виде количественного соотношения соли и воды, разделенных точкой — Na2SO4⋅10H2O. В номенклатуре для обозначения количества воды употребляются греческие числа — ди, три, тетра, гекса и так далее, с которых и начинается название. Число выступает приставкой к слову «гидро», а затем следует стандартное название соли: CaSO4⋅2H2O — дигидрат сульфата кальция.
Исторические наименования
Названия химических веществ соответствуют международной системе правил, позволяющей давать им названия, по которым можно правильно составить их формулу. Многие соединения солевой группы давно и хорошо известны, и в процессе их использования химики много лет назад уже как-то называли их. Традиционные или тривиальные названия полезно знать любому человеку. Их список приведен в таблице:
| Соль | Номенклатурное название | Тривиальное название |
| CuSO4⋅5H2O | Пентагидрат сульфата меди | Медный купорос |
| CaCO3 | Карбонат кальция | Известняк |
| AgNO3 | Нитрат серебра | Ляпис |
| NaHCO3 | Гидрокарбонат натрия | Питьевая сода |
| K2СO3 | Карбонат калия | Поташ |
| HgCl2 | Хлорид ртути | Сулема |
| Na2SiO3 | Силикат натрия | Жидкое стекло |
Это далеко не полный перечь общеизвестных наименований. Какой-либо системе они не подчиняются, и тем, кто изучает химию, их надо просто запомнить.
Химические свойства
Соли как химические соединения проявляют разные свойства в зависимости от их структурного состава. В водных растворах могут диссоциировать на анион металла и катион кислотного остатка. Степень диссоциации зависит от того, какую способность растворяться имеют разные виды солей: растворимые диссоциируют полностью, нерастворимые — частично или не диссоциируют. Ход такой реакции зависит от вида соли: средние, двойные и комплексные распадаются на ионы одномоментно, а кислые и основные — ступенчато. Примеры:
Некоторые соли под действием температуры могут разлагаться. Например, при нагревании из карбоната кальция СаСO3 получается оксид кальция СаO и кислотный оксид СО2. Солевые вещества, образованные от бескислородных кислот, разлагаются на простые элементы: хлорид серебра AgCl распадается на серебро Ag с выделением хлора Cl. Если солеобразующим соединением выступает кислота с сильными окислительными свойствами, то разложения до простых элементов не происходит: 2КNO3 → 2КNO2 + O2.
Взаимодействие с оксидами и кислотами
Соли реагируют путем сплавления с кислотными или амфотерными оксидами. При этом образуется новое солевое соединение, а оксиды замещаются менее летучими. С основными оксидами такая реакция не происходит. Например, карбонат калия K2CO3 сплавляется с оксидом кремния (IV) SiO2 с образованием силиката калия KSiO3 и выделением углекислого газа CO2: K2CO3 + SiO2 → KSiO3 + CO2↑. K2CO3 может взаимодействовать и с оксидом алюминия, при этом получается алюминат калия KAlO2 и углекислый газ CO2: K2CO3 + Al2O3 → 2KAlO2 + CO2↑.
Взаимодействие с кислотами может происходить только в том случае, если в реакцию вступает кислота и соль, образованная более слабой кислотой. Показателем возможного совместного реагирования солей с кислотами могут быть предполагаемые:
Например, нерастворимое соединение угольной кислоты карбонат магния MgCO3 вступает в реакцию с сильной серной кислотой: MgCO3 + H2SO4 → MgSO4 + 2H2O + CO2. Растворимый силикат калия как производное кремниевой кислоты может взаимодействовать с соляной кислотой, потому что в ходе реакции ожидается получение нерастворимой кремниевой кислоты: K2SiO3 + 2HCl → H2SiO3↓ + 2KCl.
Реакции с основаниями и другими солями
Со щелочами взаимодействуют в основном только соли аммония и тяжелых металлов, если при этом они относятся к растворимым. В результате получают новое солевое вещество и новое основание. Например, в реакцию с гидроксидом калия KOH вступает сульфат меди (II) CuSO4, в результате чего образуется сульфат калия K2SO4, а гидроксид меди Cu (OH) выпадает в осадок: 2KOH + CuSO4 → K2SO4 + Cu (OH)2.
Взаимодействие хлорида аммония с гидроксидом натрия описывается таким уравнением (NH4)2SO4 + 2KOH → 2H2O + K2SO4 + 2NH3↑. Если воздействовать основанием на кислую соль, то в результате получится средняя соль и вода. Например, гидрокарбонат натрия NaHCO3 взаимодействует с гидроксидом натрия NaOH: NaHCO3 + NaOH → Na3CO3 + H2O.
Реакции между солями возможны только в случае хорошей растворимости обоих веществ, при этом образуются две новые соли. С нерастворимым соединением взаимодействие не случается. Некоторые вещества, относящиеся к кислым, реагируют со слабокислыми солями и со своими средними соединениями.
Получение и применение
Многие соединения солей всех видов встречаются в виде залежей минеральных пород и рассолов. Например: известняк, разные виды селитры, поваренная и калийная соли, сильвин, карналлит, натрон, мирабилит и многие другие. Условно все способы получения солевых веществ разделяют на физическую переработку сырья (выпаривание, кристаллизация, флотация и тому подобное) и извлечение их из полупродуктов, отходов других производств и минералов химическими способами, основанными на свойствах солей.
Больше всего химическая промышленность выпускает солей для сельского хозяйства, причем они используются как в качестве удобрений для хорошего роста растений и повышения урожайности, так и для их защиты от сорняков и вредителей. Минеральные соли используют и как сырье для производства самых разнообразных химических веществ, применяемых в таких отраслях:
В качестве присадок и плавней соли применяются в металлургии для обогащения руд и при выплавке металлов. Производство цемента, одного из самых важных для строительной промышленности компонента, невозможно без известняка. Соли хрома используются при изготовлении огнеупорных материалов. Весь спектр разновидностей солей применяется и в фармацевтической промышленности.