Фосфат кальция
| Фосфат кальция | |
| Общие | |
|---|---|
| Систематическое наименование | Фосфат (ортофосфат) кальция |
| Химическая формула | Ca3(PO4)2 |
| Физические свойства | |
| Состояние (ст. усл.) | твердое |
| Молярная масса | 310,18 г/моль |
| Плотность | 2,81 г/см³ |
| Термические свойства | |
| Температура плавления | >1200 °C |
| Молярная теплоёмкость (ст. усл.) | 231,6 Дж/(моль·К) |
| Энтальпия образования (ст. усл.) | -4112,9 кДж/моль |
Содержание
Свойства
Ортофосфат кальция ещё называется фосфорнокислый кальций. Ортофосфат кальция представляет собой бесцветное кристаллическое вещество. Существует в двух модификациях — α (моноклинная сингония) и β (гексагональная сингония). В воде растворяется плохо — 0,0025 % (масс.) при 20 °C.
При действии кислот переходит в более растворимые гидрофосфаты.
Нахождение в природе
Ортофосфат кальция широко распространён в природе. Входит в состав минералов фосфорита, апатита, гидроксилапатита.
Биологическая роль
Является основным строительным материалом для костей и зубов позвоночных.
Применение
Применяется как источник кальция для подкормки скота и птиц. В составе фосфоритной муки используется как удобрение для кислых почв. Применяют в производстве керамики и стекла, абразивов. Является исходным сырьём для получения фосфорной кислоты и фосфора.
См. также
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Фосфат кальция» в других словарях:
ФОСФАТ — ФОСФАТ, фосфата, муж. (от слова фосфор). 1. Соль фосфорной кислоты, применяемая в технике, медицине и (как составная часть удобрения) в агрономии (хим.). Фосфат кальция. Фосфат алюминия. 2. Минерал, содержащий фосфорную кислоту (минер.). Толковый … Толковый словарь Ушакова
кальция вторичный кислый фосфат — kalcio hidrofosfatas statusas T sritis chemija formulė CaHPO₄ atitikmenys: angl. calcium biphosphate; calcium hydrogen phosphate rus. кальций вторичный кислый фосфорнокислый; кальция биросфат; кальция вторичный кислый фосфат; кальция гидрофосфат… … Chemijos terminų aiškinamasis žodynas
кальция биросфат — kalcio hidrofosfatas statusas T sritis chemija formulė CaHPO₄ atitikmenys: angl. calcium biphosphate; calcium hydrogen phosphate rus. кальций вторичный кислый фосфорнокислый; кальция биросфат; кальция вторичный кислый фосфат; кальция гидрофосфат… … Chemijos terminų aiškinamasis žodynas
кальция гидрофосфат — kalcio hidrofosfatas statusas T sritis chemija formulė CaHPO₄ atitikmenys: angl. calcium biphosphate; calcium hydrogen phosphate rus. кальций вторичный кислый фосфорнокислый; кальция биросфат; кальция вторичный кислый фосфат; кальция гидрофосфат… … Chemijos terminų aiškinamasis žodynas
Фосфат алюминия — Фосфат алюминия … Википедия
КАЛЬЦИЯ ФОСФАТ — Calcii phosphas. Синоним: фосфорнокислый кальций. Свойства. Мелкокристаллический, легкий, белый, без запаха и вкуса порошок. Почти нерастворимый в воде и спирте, трудно растворим в уксусной кислоте, легко в разбавленных соляной и азотной кислота … Отечественные ветеринарные препараты
кальция первичный кислый фосфат — kalcio dihidrofosfatas statusas T sritis chemija formulė Ca(H₂PO₄)₂ atitikmenys: angl. calcium acid phosphate; calcium dihydrogen phosphate; calcium dihydrophosphate rus. кальций первичный кислый фосфорнокислый; кальция дигидрофосфат; кальция… … Chemijos terminų aiškinamasis žodynas
кальция дигидрофосфат — kalcio dihidrofosfatas statusas T sritis chemija formulė Ca(H₂PO₄)₂ atitikmenys: angl. calcium acid phosphate; calcium dihydrogen phosphate; calcium dihydrophosphate rus. кальций первичный кислый фосфорнокислый; кальция дигидрофосфат; кальция… … Chemijos terminų aiškinamasis žodynas
Фосфат — Фосфаты соли и эфиры фосфорных кислот, основное применение фосфорные удобрения. Фосфаты широко используются в синтетических моющих средствах для связывания ионов кальция и магния. Важное место фосфаты занимают и в биохимии, а именно в синтезе… … Википедия
Фосфат кальция
Характеристики и физические свойства фосфата кальция
Существует в виде двух полиморфных модификаций: моноклинной и гексагональной.
Рис. 1. Фосфат кальция. Внешний вид.
Основные характеристики фосфата кальция приведены в таблице ниже:
Молярная масса, г/моль
Температура плавления, o С
Растворимость в воде (20 o С), % (масс.)
Получение фосфата кальция
Лабораторные способы получения фосфата кальция предполагают действие ортофосфорной кислоты на соли кальция (1) или гидроксид кальция (2):
Химические свойства фосфата кальция
Фосфат кальция – это средняя соль, образованная сильным основанием – гидроксидом кальция (Ca(OH)2) и слабой кислотой – ортофосфорной (H3PO4). В водном растворе гидролизуется. Гидролиз протекает по аниону (теоретически возможны вторая и третья ступень). Наличие анионов ОН — свидетельствует о щелочном характере среды.
3Ca 2+ + 2PO4 3- + HOH ↔ HPO4 2- + 3Ca 2+ + OH — ;
Для фосфата кальция характерны все свойства солей:
— взаимодействие с сильными минеральными кислотами
— взаимодействие с солями, в результате которого одним из продуктов реакции является нерастворимое в воде соединение
— разложение при нагревании
Применение фосфата кальция
Фосфат кальция нашел применение в качестве добавки при производстве кормов для КРС и домашних птиц. Его используют при производстве минеральных удобрений, керамики и стекла. В пищевой промышленности фосфат кальция известен как добавка Е341 – разрыхлитель.
Примеры решения задач
| Задание | Вычислите массу фосфата кальция, который может прореагировать с концентрированным раствором соляной кислоты объемом 100 мл (массовая доля HCl 34%, плотность 1,168 кг/л). |
| Решение | Запишем уравнение реакции: |
Найдем массу раствора соляной кислоты, а также массу растворенного вещества HCl в нем:
msolution =0,1 × 1,168 = 0,1168 кг = 116,8г.
msolute (HCl) = ω (HCl) / 100% ×msolution;
msolute (HCl) = 34 / 100% × 116,8 = 39,712 г.
Рассчитаем количество моль соляной кислоты (молярная масса равна 36,5 г/моль):
n(HCl) = m (HCl) / M (HCl);
n (HCl) = 39,712 / 36,5 = 1,088 моль.
Согласно уравнению реакции n (HCl) :n (Ca3(PO4)2) =6: 1. Значит,
Тогда масса фосфата кальция, вступившего в реакцию будет равна (молярная масса – 310 г/моль):
| Задание | Какая масса оксида фосфора (V) образуется в ходе реакции термического разложения фосфата кальция массой 46 г? |
| Решение | Запишем уравнение реакции термического разложения фосфата кальция: |
Рассчитаем количество вещества фосфата кальция (молярная масса – 310 г/моль):
Найдем массу образовавшегося оксида фосфора (V) (молярная масса – 284 г/моль):
Структура фосфата кальция (Ca3 (PO4) 2), свойства, образование и использование
С другой стороны, фосфат кальция относится к ряду солей, которые варьируются в зависимости от соотношения Ca / P, а также от степени гидратации и pH. На самом деле существует много типов фосфатов кальция, которые существуют и могут быть синтезированы. Однако, буквально следуя номенклатуре, фосфат кальция относится только к трикальцию, упомянутому выше..
Все фосфаты кальция, включая Са3(РО4)2, Они однотонные с легкими сероватыми тонами. Они могут быть зернистыми, мелкими, кристаллическими и иметь размеры частиц около микрометров; и даже были получены наночастицы этих фосфатов, с помощью которых были разработаны биосовместимые материалы для костей..
Эта биосовместимость связана с тем, что эти соли находятся в зубах и, короче, в костных тканях млекопитающих. Например, гидроксиапатит представляет собой кристаллический фосфат кальция, который, в свою очередь, взаимодействует с аморфной фазой той же соли.
Это означает, что существуют аморфные и кристаллические фосфаты кальция. По этой причине разнообразие и множество вариантов не удивительны при синтезе материалов на основе фосфатов кальция; материалы, свойства которых исследователи интересуются каждый день во всем мире, чтобы сосредоточиться на восстановлении костей.
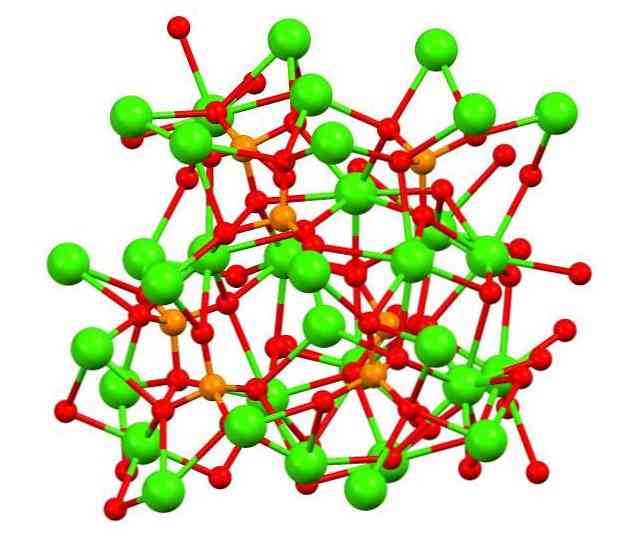
Структура фосфата кальция
Верхнее изображение показывает структуру трехосновного каликофосфата в странном минерале whitlockite, который может содержать магний и железо в качестве примесей.
Хотя на первый взгляд это может показаться сложным, необходимо уточнить, что модель предполагает ковалентное взаимодействие между атомами кислорода фосфатов и металлическими центрами кальция.
В результате истинная структура АШП становится более сложной, состав ее ионов которой представлен формулой: Ca9(РО4)6-х(HPO4)х(ОН)х. «Х» указывает на степень гидратации, так как если х = 1, то формула будет такой: Ca9(РО4)5(HPO4) (ОН).
Различные структуры, которые могут иметь PCA, зависят от молярных отношений Ca / P; то есть относительного количества кальция и фосфата, которые изменяют весь их результирующий состав.
Остальная часть семьи
На самом деле фосфаты кальция представляют собой семейство неорганических соединений, которые, в свою очередь, могут взаимодействовать с органической матрицей..
Ниже приведены некоторые фосфаты и их соответствующие структуры и химические формулы:
-Водород кальций фосфат дигидрат, CaHPO4H 2H2O: моноклинный.
-Кальция дигидрофосфат моногидрат, Ca (H)2ПО4)2∙ H2O: триклиника.
-Безводный кислый фосфат, Ca (H)2ПО4)2: триклиника.
-Ocalcium гидрофосфат (OCP), Ca8H2(РО4)6: триклиника Является предшественником в синтезе гидроксиапатита.
Фосфат кальция
Характеристики и физические свойства фосфата кальция
Существует в виде двух полиморфных модификаций: моноклинной и гексагональной.
Рис. 1. Фосфат кальция. Внешний вид.
Основные характеристики фосфата кальция приведены в таблице ниже:
Молярная масса, г/моль
Температура плавления, o С
Растворимость в воде (20 o С), % (масс.)
Получение фосфата кальция
Лабораторные способы получения фосфата кальция предполагают действие ортофосфорной кислоты на соли кальция (1) или гидроксид кальция (2):
Химические свойства фосфата кальция
Фосфат кальция – это средняя соль, образованная сильным основанием – гидроксидом кальция (Ca(OH)2) и слабой кислотой – ортофосфорной (H3PO4). В водном растворе гидролизуется. Гидролиз протекает по аниону (теоретически возможны вторая и третья ступень). Наличие анионов ОН — свидетельствует о щелочном характере среды.
3Ca 2+ + 2PO4 3- + HOH ↔ HPO4 2- + 3Ca 2+ + OH — ;
Для фосфата кальция характерны все свойства солей:
— взаимодействие с сильными минеральными кислотами
— взаимодействие с солями, в результате которого одним из продуктов реакции является нерастворимое в воде соединение
— разложение при нагревании
Применение фосфата кальция
Фосфат кальция нашел применение в качестве добавки при производстве кормов для КРС и домашних птиц. Его используют при производстве минеральных удобрений, керамики и стекла. В пищевой промышленности фосфат кальция известен как добавка Е341 – разрыхлитель.
Примеры решения задач
| Задание | Вычислите массу фосфата кальция, который может прореагировать с концентрированным раствором соляной кислоты объемом 100 мл (массовая доля HCl 34%, плотность 1,168 кг/л). |
| Решение | Запишем уравнение реакции: |
Найдем массу раствора соляной кислоты, а также массу растворенного вещества HCl в нем:
msolution =0,1 × 1,168 = 0,1168 кг = 116,8г.
msolute (HCl) = ω (HCl) / 100% ×msolution;
msolute (HCl) = 34 / 100% × 116,8 = 39,712 г.
Рассчитаем количество моль соляной кислоты (молярная масса равна 36,5 г/моль):
n(HCl) = m (HCl) / M (HCl);
n (HCl) = 39,712 / 36,5 = 1,088 моль.
Согласно уравнению реакции n (HCl) :n (Ca3(PO4)2) =6: 1. Значит,
Тогда масса фосфата кальция, вступившего в реакцию будет равна (молярная масса – 310 г/моль):
| Задание | Какая масса оксида фосфора (V) образуется в ходе реакции термического разложения фосфата кальция массой 46 г? |
| Решение | Запишем уравнение реакции термического разложения фосфата кальция: |
Рассчитаем количество вещества фосфата кальция (молярная масса – 310 г/моль):
Найдем массу образовавшегося оксида фосфора (V) (молярная масса – 284 г/моль):
Структура фосфата кальция (Ca3 (PO4) 2), свойства, образование и использование
С другой стороны, фосфат кальция относится к ряду солей, которые варьируются в зависимости от соотношения Ca / P, а также от степени гидратации и pH. На самом деле существует много типов фосфатов кальция, которые существуют и могут быть синтезированы. Однако, буквально следуя номенклатуре, фосфат кальция относится только к трикальцию, упомянутому выше..
Все фосфаты кальция, включая Са3(РО4)2, Они однотонные с легкими сероватыми тонами. Они могут быть зернистыми, мелкими, кристаллическими и иметь размеры частиц около микрометров; и даже были получены наночастицы этих фосфатов, с помощью которых были разработаны биосовместимые материалы для костей..
Эта биосовместимость связана с тем, что эти соли находятся в зубах и, короче, в костных тканях млекопитающих. Например, гидроксиапатит представляет собой кристаллический фосфат кальция, который, в свою очередь, взаимодействует с аморфной фазой той же соли.
Это означает, что существуют аморфные и кристаллические фосфаты кальция. По этой причине разнообразие и множество вариантов не удивительны при синтезе материалов на основе фосфатов кальция; материалы, свойства которых исследователи интересуются каждый день во всем мире, чтобы сосредоточиться на восстановлении костей.
Структура фосфата кальция
Верхнее изображение показывает структуру трехосновного каликофосфата в странном минерале whitlockite, который может содержать магний и железо в качестве примесей.
Хотя на первый взгляд это может показаться сложным, необходимо уточнить, что модель предполагает ковалентное взаимодействие между атомами кислорода фосфатов и металлическими центрами кальция.
В результате истинная структура АШП становится более сложной, состав ее ионов которой представлен формулой: Ca9(РО4)6-х(HPO4)х(ОН)х. «Х» указывает на степень гидратации, так как если х = 1, то формула будет такой: Ca9(РО4)5(HPO4) (ОН).
Различные структуры, которые могут иметь PCA, зависят от молярных отношений Ca / P; то есть относительного количества кальция и фосфата, которые изменяют весь их результирующий состав.
Остальная часть семьи
На самом деле фосфаты кальция представляют собой семейство неорганических соединений, которые, в свою очередь, могут взаимодействовать с органической матрицей..
Ниже приведены некоторые фосфаты и их соответствующие структуры и химические формулы:
-Водород кальций фосфат дигидрат, CaHPO4H 2H2O: моноклинный.
-Кальция дигидрофосфат моногидрат, Ca (H)2ПО4)2∙ H2O: триклиника.
-Безводный кислый фосфат, Ca (H)2ПО4)2: триклиника.
-Ocalcium гидрофосфат (OCP), Ca8H2(РО4)6: триклиника Является предшественником в синтезе гидроксиапатита.